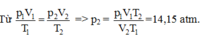Khi đung nóng một bình kín chứa khí để nhiệt độ tăng 1 o C thì áp suất khí tăng thêm 1/360 áp suất ban đầu. Nhiệt độ ban đầu của khí là
A. 73 o C
B. 37 o C
C. 87 o C
D. 78 o C
Khi đung nóng một bình kín chứa khí để nhiệt độ tăng 1 thì áp suất khí tăng 1 ° C thêm 1/ 360 áp suất ban đầu. Nhiệt độ ban đầu của khí là
A. 73 ° C
B. 37 ° C
C. 87 ° C
D. 78 ° C
Khi đung nóng một bình kín chứa khí để nhiệt độ tăng 1 ° C thì áp suất khí tăng thêm 1 360 áp suất ban đầu. Nhiệt độ ban đầu của khí là:
A. 73 ° C
B. 37 ° C
C. 87 ° C
D. 78 ° C
Đáp án: C
Ta có:
- Trạng thái 1: p 1 = p , T 1 = t + 273
- Trạng thái 2: p 2 = p 1 + 1 360 , T 2 = t + 1 + 273
Do thể tích không đổi, theo định luật Sáclơ, ta có:
p 1 T 1 = p 2 T 2 ↔ p t + 273 = p 1 + 1 360 t + 1 + 273 → t = 87 0 C
Một bình chứa một lượng khí ở nhiệt độ 27 ° C và áp suất p. Để áp suất tăng gấp đôi thì nhiệt độ phải tăng đến
A. 54 ° C
B. 300 ° C
C. 600 ° C
D. 327 ° C .
Chọn D.
Do V không đổi nên ta có
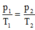
Với p1 = p; p2 = 2p; T1 = 27 + 273 = 300 K
Do đó T2 = T1 p 2 p 1 = 2T1 = 600 K ⟹ t2 = 327 ° C .
Một bình chứa một lượng khí ở nhiệt độ 27 o C và áp suất p. Để áp suất tăng gấp đôi thì nhiệt độ phải tăng đến
A. 54 o C
B. 300 o C
C. 600 o C
D. 327 o C
Một bình thép chứa khí ở nhiệt độ 27 ° C và áp suất 40 atm. Nếu tăng áp suất thêm 10 atm thì nhiệt độ của khí trong bình là
A. 102 ° C
B. 375 ° C
C. 34 ° C
D. 402 ° C
Chọn A.
Quá trình biến đổi là đẳng tích, ta có:
![]()
Với p1 = 40 atm; p2 = p1 + 10 = 50 atm; T1 = t1 + 273 = 27 + 273 = 300 K.
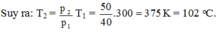
Một bình thép chứa khí ở nhiệt độ 27 o C và áp suất 40 atm. Nếu tăng áp suất thêm 10 atm thì nhiệt độ của khí trong bình là
A. 102 o C
B. 375 o C
C. 34 o C
D. 402 o C
Chọn A.
Quá trình biến đổi là đẳng tích, ta có:
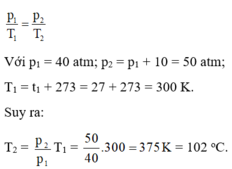
Nếu nung nóng khí trong một bình kín lên thêm 423 ° C thì áp suất khí tăng lên 2,5 lần. Nhiệt độ của khí trong bình là
A. 100 ° C
B. - 173 ° C
C. 9 ° C
D. 282 ° C
Chọn C.
C. Vì bình kín nên V không đổi, ta có
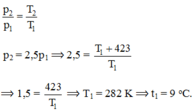
Đun nóng NH3 trong bình kín không có không khí một thời gian, rồi đưa về nhiệt độ ban đầu thì thấy áp suất trong bình tăng gấp 1,5 lần. Vậy % NH3 bị phân hủy trong thời gian này bằng :
A.25% B.50% C.75% D.100%
Vì nhiệt độ không đổi nên độ tăng áp suất = độ tăng thể tích = độ tăng số mol.
2 NH3 --> N2 + 3 H2
Từ 1 mol NH3 ban đầu thì sau phản ứng thu 2 mol hỗn hợp sản phẩm.
Nếu a là số mol NH3 ban đầu thì sau khi phản ứng phân hủy kết thúc thu 1,5a mol sản phẩm tức là số mol tăng lên 0,5a mol.
Như vậy, đã có 0,5a/2 mol NH3 bị phân hủy.
Hiệu suất = 0,25a/a = 0,25 = 25%
Chọn A. 25%
Một bình chứa một lượng khí ở nhiệt độ 27 và áp suất 30 atm. Nếu giảm nhiệt độ xuống còn 10 và để một nửa lượng khí thoát ra ngoài thì áp suất khí còn lại trong bình bằng
A. 2 atm.
B. 14,15 atm.
C. 15 atm.
D. 1,8 atm.
Chọn B.
Xét lượng khí còn lại trong bình:
Trạng thái 1: V1 = V/2; T1 = 300 K; p1 = 30 atm.
Trạng thái 2: V2 = V; T2 = 283 K; p2 = ?