Thực hiện phản ứng giữa H 2 và N 2 (tỉ lệ mol 4 : 1) trong bình kín có xúc tác, thu được hỗn hợp khi có áp suất giảm 9% so với ban đầu (trong cùng điều kiện). Hiệu suất phản ứng là
A. 20%
B. 22,5%.
C. 25%.
D. 27%.
Thực hiện phản ứng giữa H 2 v à N 2 (tỉ lệ mol 4 : 1) trong bình kín có xúc tác, thu được hỗn hợp khi có áp suất giảm 9% so với ban đầu (trong cùng điều kiện). HIệu suất phản ứng là
A. 20%.
B. 22,5%.
C. 25%.
D. 27%.
Chọn B
nH2 = 4 mol; nN2 = 1 mol
Hỗn hợp khí có áp suất giảm 9%
→ Số mol sau phản ứng = 91%.5 = 4,55 mol
3H2 + N2 ⇆ 2NH3 do số mol H2 : N2 = 4 : 1 nên hiệu suất tính theo N2
Pư: 3x x 2x
n hỗn hợp sau pư = n H2 dư + n N2 dư + n NH3 = 4 -3x + 1 – x + 2x = 5 -2x = 4,55
ð x = 0,225 => H% = 22,5%
Thực hiện phản ứng giữa N2 và H2 (tỉ lệ mol 1:4) trong bính kín có xúc tác, thu được hỗn hợp có áp suất giảm 10% so với ban đầu (cùng đk). Hiệu suất phản ứng là
A. 25%
B. 50%
C. 75%
D. 60%
Câu 1: Thực hiện phản ứng giữa H2 và N2 (tỉ lệ mol 4:1), trong bình kín có xúc tác, thu được hỗn hợp khí có áp suất giảm 9% so với ban đầu ( trong cùng điều kiện). Tính Hiệu suất phản ứng.
Câu 2: Trộn 3 dung dịch HCl 0,3M; H2SO4 0,2M; và H3PO4 0,1M với những thể tích bằng nhau thu được dung dịch A. Để trung hòa 300ml dung dịch A cần vừa đủ V ml dung dịch B gồm NaOH 0,2M và Ba(OH)2 0,1M. Tính giá trị của V.
Câu 3: Hòa tan hoành toàn m gam Al trong dung dịch HNO3, thấy tạo ra 4,48 lít hỗn hợp 3 khí NO, N2, N2O (tỉ lệ mol nNO : nN2 : nN2O = 1:2:2) Thể tích dung dịch HNO3 1M cần bao nhiêu lít?
Câu 3: Gọi số mol NO là a . Có: n\(_{N_2}\) = n\(_{N_2O}\) = 2a => 5a = \(\dfrac{4,48}{22,4}\) = 0,2
=> a = 0,04 . Vậy: n\(HNO_3\) = a.4+2a.10+2a.12 = 1,92 (mol)
=> V\(_{HNO_3}\) = 1,92 (lít)
Trong bình kín dung tích 2,24 lít chứa 1 ít bột Ni làm xúc tác và hỗn hợp khí có tỉ khối so với H2 là 7,56 gồm H2, C2H4, và C3H6 (đktc). Hỗn hợp khí trong bình sau khi nung có tỉ khối hơi so với hidro là 8,4. Hãy tính áp suất sau khi nung, nếu áp suất ban đầu là 1 atm và nhiệt độ bình không thay đổi sau phản ứng
Ta có :
\(m_{hỗn\ hợp} = n.M = \dfrac{2,24}{22,4}.2.7,56 = 1,521(gam)\)
Bảo toàn khối lượng , sau khi nung : m = 1,521(gam)
\(\Rightarrow n_{hỗn\ hợp\ sau} = \dfrac{1,521}{2.8,4} = 0,09(mol)\)
Ta có :
\(\dfrac{p_{trước}}{p_{sau}} = \dfrac{n_{trước}}{n_{sau}}\)
⇔ \(\dfrac{1}{p_{sau}} = \dfrac{0,1}{0,09}\\ \Rightarrow p_{sau} = 0,9\ atm\)
Trong bình kín chứa hỗn hợp X gồm 1 ankin, 1 anken, 1 ankan và H2 với áp suất 4 atm. Đun nóng bình với Ni xúc tác để thực hiện phản ứng cộng, sau đó đưa bình về nhiệt độ ban đầu thu được hỗn hợp Y, thấy áp suất trong bình là 3 atm. Tỉ khối của hỗn hợp X và Y so với H2 lần lượt là 24 và x. Giá trị của x là:
A. 32
B. 24
C. 34
D. 18
Hỗn hợp X gồm N2 và H2 có tỉ khối hơi so với H2 là 3,6. Cho hỗn hợp X vào bình kín với xúc tác thích hợp rồi thực hiện phản ứng tổng hợp NH3 thấy thu được hỗn hợp Y gồm N2, H2 và NH3. Biết tỉ khối hơi của Y so với H2 bằng 4. Hiệu suất phản ứng tổng hợp NH3 trong phản ứng trên là
A. 30%.
B. 15%.
C. 20%.
D. 25%.
Xét cân bằng trong bình kín có dung tích không đổi Xkhí ⇔ 2Ykhí
Ban đầu cho 1 mol khí X vào bình; khi đạt cân bằng thì thấy:
- Ở 400C trong bình kín có 0,75mol X
- Ở 450C trong bình kín có 0,65 mol X
Có các phát biếu sau :
(1) Phản ứng thuận là phản ứng thu nhiệt
(2) Khi tăng áp suất, cân bằng chuyển dịch theo chiều nghịch
(3) Thêm tiếp Y vào hỗn hợp cân bằng thì cân bằng chuyển dịch theo chiều nghịch
(4) Thêm xúc tác thích hợp vaò hỗn hợp cân bằng thì cân bằng vẫn không chuyển dịch
Số phát biểu đúng là:
A. 3
B. 2
C. 1
D. 4
Đáp án D
Xét các phát biểu:
(1) Khi tăng nhiệt độ số mol X giảm, nghĩa là chuyển dịch theo chiều thuận → phản ứng thuận là phản ứng thu nhiệt → (1) đúng.
(2) Khi tăng áp suất thì cân bằng chuyển dịch theo chiều làm giảm áp suất → cân bằng chuyển dịch theo chiều nghịch →(2) đúng
(3) Thêm Y vào thì cân bằng chuyển dịch theo chiều giảm Y nghĩa là cân bằng chuyển dịch theo chiều nghịch → (3) đúng
(4) Xúc tác không làm ảnh hưởng đến chuyển dịch mà chỉ làm thay đổi tốc độ phản ứng →(4) đúng
Chọn đáp án D.
Thực hiện phản ứng giữa H 2 và N 2 trong bình kín có xúc tác thu được 1,7 gam NH 3 với hiệu suất phản ứng là 80%. Thể tích H 2 (đktc) cần dùng cho phản ứng là (Cho: N = 14, H = 1)
A. 4,2 lít.
B. 2,4 lít.
C. 4 lít.
D. 5lít.
Chọn A
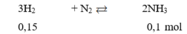
Do hiệu suất phản ứng là 80% nên thể tích H 2 cần dùng là:
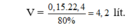
Hỗn hợp X gồm N2 và H2 có tỉ khối so với H2 bằng 3,6. Sau khi tiến hành phản ứng tổng hợp amoniac trong bình kín (có xúc tác bột Fe) thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 4. Tính Hiệu suất phản ứng tổng hợp NH3
Ta có MX = 3,6.2 =7,2.
Áp dụng qui tắc đường chéo :
=> nH2 : nN2 = 4 : 1
Đặt nH2 = 4 mol => nN2 = 1 mol
N2 + 3H2 ---> 2NH3
x----->3x-------->2x
=> nY = 5 – 2x mol
Bảo toàn khối lượng :
mX = mY = 4.2 + 1.28 = 36g
=> MY = 4.2 = \(\dfrac{36}{5-2x}\)
=> x = 0,25 mol
Tính hiệu suất theo N2 => H = \(\dfrac{0,25}{1}\)= 25%