Để điều chê kali clorua KCl (dùng làm phân bón), người ta cho kim loại kali K tác dụng với khí clo C l 2 . Viết phương trình hóa học của phản ứng.

Những câu hỏi liên quan
Để điều chê kali clorua KCl (dùng làm phân bón), người ta cho kim loại kali K tác dụng với khí clo
C
l
2
. Nếu có
6
,
02
.
10
23
nguyên tử K, cần lấy vào phản ứng bao nhiêu phân tử
C
l
2
và thu được bao nhiêu phân tử KCl?
Đọc tiếp
Để điều chê kali clorua KCl (dùng làm phân bón), người ta cho kim loại kali K tác dụng với khí clo C l 2 . Nếu có 6 , 02 . 10 23 nguyên tử K, cần lấy vào phản ứng bao nhiêu phân tử C l 2 và thu được bao nhiêu phân tử KCl?
Theo PTHH, ta có tỉ lệ:
Cứ 2 nguyên tử K tác dụng với 1 phân tử C l 2 tạo thành 2 phân tử KCl.
Vậy số Clo lấy vào phản ứng khi có 6 , 02 . 10 23 phân tử K:
Số phân tử
C
l
2
=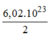 =
3
,
01
.
10
23
(phân tử)
=
3
,
01
.
10
23
(phân tử)
Số phân tử KCl được tạo ra:
Số phân tử KCl =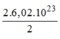 =
6
,
02
.
10
23
(phân tử)
=
6
,
02
.
10
23
(phân tử)
Đúng 0
Bình luận (1)
Bài 1: Để điều chế Kali Clorua ( KCl ) người ta cho Kali tác dụng với khí Clo.
a) Nếu có 3.1023 nguyên tử K, cần lấy vào phản ứng bao nhiêu phân tử Cl2 và thu được bao nhiêu KCl ?
b)Giả sử có 1,8.1023 nguyên tử Kali phản ứng. Hãy tính:
+khối lượng theo gam của khí clo phản ứng.
+khối lượng theo gam kcl thu được( theo 2 cách)
c)Tính số nguyên tử Kali có trong 39 gam kim loại Kali. Từ đó tính khối lượng khí clo Để tác dụng vừa đủ với 39 gam kim loại Kali.
d)tính khối lượng Kali Clorua thu đư...
Đọc tiếp
Bài 1: Để điều chế Kali Clorua ( KCl ) người ta cho Kali tác dụng với khí Clo.
a) Nếu có 3.1023 nguyên tử K, cần lấy vào phản ứng bao nhiêu phân tử Cl2 và thu được bao nhiêu KCl ?
b)Giả sử có 1,8.1023 nguyên tử Kali phản ứng. Hãy tính:
+khối lượng theo gam của khí clo phản ứng.
+khối lượng theo gam kcl thu được( theo 2 cách)
c)Tính số nguyên tử Kali có trong 39 gam kim loại Kali. Từ đó tính khối lượng khí clo Để tác dụng vừa đủ với 39 gam kim loại Kali.
d)tính khối lượng Kali Clorua thu được (theo 2 cách) khi cho 39 gam kim loại Kali phản ứng hết với khí clo.
GIẢI NHANH LÊN VỚI!!!
Để điều chế kali clorua KCl( dùng làm phân bón),người ta cho kim loại kali K tác dụng với khí clo Cl2
a) Viết PTHH của phản ứng.
b)Nếu có 6,02.1023 nguyên tử K, cần lấy vào phản ứng bao nhiêu phân tử Cl2 và thu được bao nhiêu phân tử KCl?
b) Theo đề bài, ta có: \(n_K=\dfrac{6,02.10^{23}}{6.10^{23}}=\dfrac{301}{300}\left(mol\right)\)
PTHH: \(2K+Cl_2\rightarrow2KCl\)
pư..........\(\dfrac{301}{300}\)......\(\dfrac{301}{600}\).....\(\dfrac{301}{300}\) (mol)
\(\Rightarrow\left\{{}\begin{matrix}SPT_{Cl2}=6.10^{23}.\dfrac{301}{300}=6,02.10^{23}\left(ptử\right)\\SPT_{KCl}=6.10^{23}.\dfrac{301}{600}=3,01.10^{23}\left(ptử\right)\end{matrix}\right.\)
Vậy...............
Đúng 0
Bình luận (7)
CHÚC BẠN HỌC TỐT!!![]()
a) PTHH: \(2K+Cl_2\rightarrow2KCl\)
Đúng 0
Bình luận (0)
Để điều chế Oxi trong phòng thí nghiệm, một em học sinh nhiệt phân 24,5g kali clorat ( KClO3) thu được 9,6g khí Oxi và muối kali clorua ( KCl). a) Viết phương trình hóa học của phản ứng trên b) Viết công thức về khối lượng của phản ứng xảy ra c) Tính khối lượng muối kali clorua tạo ra.d) Cho biết lệ số phân tử Oxi với các chất còn lại trong phản ứngMọi người giúp mình.Cẻm ơn!
Đọc tiếp
Để điều chế Oxi trong phòng thí nghiệm, một em học sinh nhiệt phân 24,5g kali clorat ( KClO3) thu được 9,6g khí Oxi và muối kali clorua ( KCl).
a) Viết phương trình hóa học của phản ứng trên
b) Viết công thức về khối lượng của phản ứng xảy ra
c) Tính khối lượng muối kali clorua tạo ra.
d) Cho biết lệ số phân tử Oxi với các chất còn lại trong phản ứng
Mọi người giúp mình.Cẻm ơn!
\(a,PTHH:2KClO_3\rightarrow\left(^{t^o}_{MnO_2}\right)2KCl+3O_2\\ b,m_{KClO_3}=m_{KCl}+m_{O_2}\\ c,m_{KCl}=m_{KClO_3}-m_{O_2}=14,9\left(g\right)\\ d,\text{Số phân tử }O_2:\text{Số phân tử }KCl=3:2\\ \text{Số phân tử }O_2:\text{Số phân tử }KClO_3=3:2\)
Đúng 3
Bình luận (0)
Khi phân hủy hoàn toàn 24,5 gam muối Kali clorat KClO3, thu được 9,6 gam khí oxi và muối Kali clorua KCl a. Lập phương trình hóa học của phản ứng b. Viết công thức về khối lượng của phản ứng c. Tính khối lượng muối kali clorua KCl thu được?
\(2KClO_3\rightarrow3O_2+2KCl\)
\(m_{KClO_3}=m_{O_2}+m_{KCl}\)
\(\Rightarrow m_{KCl}=m_{KClO_3}-m_{KCl}=24,5-9,6=14,9\left(g\right)\)
Đúng 2
Bình luận (1)
Bài 1: Để điều chế Kali Clorua ( KCl ) người ta cho Kali tác dụng với khí Clo
a) Nếu có 6,02.1023 nguyên tử K, cần lấy vào phản ứng bao nhiêu phân tử Cl2 và thu được bao nhiêu KCl ?
b) Tính khối lượng bằng gam của:
+ 6,02.1023 nguyên tử K
+ 6,02.1023 phân tử Cl2
+ 6,02.1023 phân tử KCl
Câu 1: Lập phương trình hóa học cúa các sơ đồ phản ứng sau đây và cho biết chúng thuộc loại phản ứng hóa học nào:
a) Kali clorat (KClO3) ------- Kali clorua (KCl) + ........?.......
b) Photpho + Khí oxi ------- .............?............
c) Sắt (II) oxit + Khí hiđro ---------. .........?........ + ........?........
d) Magie + Axitsunfuric (H2SO4) -------. ............?........ + ...........?..........
e) Kali pemanganat (KMnO4) ------ Kali ma...
Đọc tiếp
Câu 1: Lập phương trình hóa học cúa các sơ đồ phản ứng sau đây và cho biết chúng thuộc loại phản ứng hóa học nào: a) Kali clorat (KClO3) -------> Kali clorua (KCl) + ........?....... b) Photpho + Khí oxi -------> .............?............ c) Sắt (II) oxit + Khí hiđro ---------.> .........?........ + ........?........ d) Magie + Axitsunfuric (H2SO4) -------.> ............?........ + ...........?.......... e) Kali pemanganat (KMnO4) ------> Kali magant (K2MnO4) + Mangan đioxit (MnO2) + …?… f) …?… + axit sunfuric (H2SO4) loãng ------> nhôm sunfat (Al2(SO4)3) + …?… g) Đồng (II) oxit + khí hiđro ------> …?… + …?… Câu 2: Cho 4,05 gam kim loại nhôm tác dụng với dung dịch có chứa 14,6 gam axit clohiđric. a) Chất nào dư sau phản ứng và dư bao nhiêu gam ? b) Tính thể tích khí hiđro thu được ở điều kiện tiêu chuẩn ? Câu 3: Cho 2,7 gam Al tác dụng với 19,6 gam dung dịch H2SO4. a) Chất nào còn dư sau phản ứng? Khối lượng dư là bao nhiêu? c) Tính khối lượng muối thu được sau phản ứng? Câu 4: Cho 2,8 gam Fe tác dụng với 5,475 gam dung dịch HCl vừa đủ. a) Chất nào còn dư sau phản ứng? Khối lượng dư là bao nhiêu? c) Tính thể tích khí thu được sau phản ứng? Câu 5: Đốt cháy hoàn toàn 2,48 gam photpho trong bình chứa khí oxi, tạo thành điphotpho pentaoxit. a) Tính khối lượng hợp chất tạo thành? b) Nếu trong bình chứa 4 gam khí oxi. Hỏi sau khi phản ứng kết thúc chất nào còn dư và dư bao nhiêu gam? Câu 6: Xem lại 2 thí nghiệm điều chế oxi (tr 92) và hiđro (tr 115). Xem và gọi tên các dụng cụ, hóa chất, cho biết phương pháp dùng thu khí ở mỗi thí nghiệm.
Câu4: Cho kim loại magie tác dụng với dung dịch axit clohđric (HCl) người ta thu được muối magie clorua ( MgCl2) và 44,8 l khí hiđro H2. a. Viết phương trình hóa học của phản ứng. b. Tính khối lượng axit clohiđric cần dùng cho phản ứng? c. Tính khối lượng muối magie clorua thu được sau phản ứng?
\(a.Mg+2HCl\rightarrow MgCl_2+H_2\\ n_{H_2}=\dfrac{44,8}{22,4}=2\left(mol\right)\\ n_{HCl}=2n_{H_2}=4\left(mol\right)\\ \Rightarrow m_{HCl}=4.36,5=146\left(g\right)\\ c.n_{MgCl_2}=n_{H_2}=2\left(mol\right)\\ \Rightarrow m_{MgCl_2}=2.95=190\left(g\right)\)
Đúng 3
Bình luận (0)
Đốt cháy 7,8 g kim loại Kali trong khí Oxi sinh ra Kali oxit. Viết phương trình hóa học của phản ứng. Tính khối lượng Kali oxit sinh ra. Tính thể tích của khí Oxi đã phản ứng ở điều kiện tiêu chuẩn. Tính thể tích không khí cần dùng biết khí oxi chiếm...
Xem chi tiết
nK=0,2(mol)
PTHH: 4K + O2 -to-> 2 K2O
nK2O= 0,1(mol) => mK2O=0,1.94=9,4(g)
nO2=0,05(mol) -> V(O2,đktc)=0,05.22,4=1,12(l)
V(kk,dktc)=5.V(O2,dktc)=5.1,12=5,6(l)
Đúng 1
Bình luận (0)


















