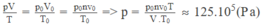Một bình kín có thể tích là 0,5 lít chứa 0,5 mol H 2 và 0,5 mol N 2 , ở nhiệt độ t ° C . Khi ở trạng thái cân bằng có 0,2 mol N H 3 tạo thành. Hằng số cân bằng K C của phản ứng tổng hợp N H 3 là :
A. 1.278
B. 3,125
C. 4.125
D. 6,75
Một bình kín có thể tích là 0,5 lít chứa 0,5 mol H 2 và 0,5 mol N 2 , ở nhiệt độ ( t ° C ). Khi ở trạng thái cân bằng có 0,2 mol NH 3 tạo thành. Hằng số cân bằng K C của phản ứng tổng hợp NH 3 là :
A. 1.278
B. 3,125
C. 4.125
D. 6,75
Một bình kín có thể tích 0,5 lít chứa 0,5 mol H2 và 0,5 mol N2 ở nhiệt độ thích hợp, khi đạt tới trạng thái cân bằng có 0,2 mol NH3 được tạo thành. Hiệu suất của phản ứng là bao nhiêu?
A. 20%
B. 30%
C. 60%
D. 50%
Đáp án C.
N2+ 3H2 ⇌ 2NH3
Vì  nên hiệu suất tính theo H2
nên hiệu suất tính theo H2
N2+ 3H2 ⇌ 2NH3
Ban đầu 0,5 0,5 mol
Phản ứng x/3 x 2x/3 mol
Sau pứ 0,2 mol
Ở trạng thái cân bằng có 0,2 mol NH3 tạo thành nên 2x/3= 0,2
→x=0,3

Một bình kín có thể tích là 0,5 lit chứa 0,5 mol H2 và 0,5 molN2 , ở nhiệt độ toC . Khi ở trạng tháu cân bằng có 0,2 mol NH3 tạo thành. Hằng số cân bằng Kc của phản ứng tổng hợp NH3 là
A. 1,278
B. 3,125
C. 6,750
D. 4,125
Đáp án B
Theo gải thiết ban đầu ta thấy [H2]=[N2]=1M
Thực hiện phản ứng tổng hợp NH3đến thời điểm cân bằng [NH3] = 0,4 m
Ta có: N2+3H2 ⇌2NH3
Bdau: 1………1………….0
p.ung:0,2…….0,6……….0,4
Sau: 0,8………0,4……….0,4
Tại thời điểm cân bằng [N2]=0,8;[H2]=0,4M;[NH3]=0,4M
→Kc = 3,125
Một bình kín có thể tích là 0,5 lit chứa 0,5 mol H2 và 0,5 molN2 , ở nhiệt độ toC . Khi ở trạng tháu cân bằng có 0,2 mol NH3 tạo thành. Hằng số cân bằng Kc của phản ứng tổng hợp NH3 là
A. 1,278
B. 3,125
C. 6,750
D. 4,125
Đáp án B
Theo gải thiết ban đầu ta thấy [H2]=[N2]=1M
Thực hiện phản ứng tổng hợp NH3đến thời điểm cân bằng [NH3] = 0,4 m
Ta có: N2+3H2 ⇌2NH3
Bdau: 1………1………….0
p.ung:0,2…….0,6……….0,4
Sau: 0,8………0,4……….0,4
Tại thời điểm cân bằng [N2]=0,8;[H2]=0,4M;[NH3]=0,4M →Kc = 3,125
Một bình có thể tích 5,6l chứa 0,5 mol ở 0 ° C . Áp suất khí trong bình là?
A. 1 atm
B. 2 atm
C. 3 atm
D. 4 atm
Một bình có thể tích 5,6l chứa 0,5 mol ở 0 ° C. Áp suất khí trong bình là?
A. 1 atm
B. 2 atm
C. 3 atm
D. 4 atm
Trong bình kín dung dịch 17,92 lít (thể tích không đổi) chứa một ít bột Ni (thể tích không đáng kể) và hỗn hợp X gồm H2 và C2H2 (ở 0oC, 1 atm). Nung nóng bình một thời gian sau đó làm lạnh về 0oC thì áp suất trong bình là 0,5 atm và thu được hỗn hợp khí Y có tỉ khối hơi so với H2 bằng 14. Số mol H2 trong Y là
A. 0,1
B. 0,2
C. 0,3
D. 0
Thể tích của hỗn hợp khí X gồm: 0,2 mol CO 2 ; 0,5 mol H 2 và 0,3 mol 0 2 ở 0 0 C, 1 atm là: A. 22,4 lít. B. 3,36 lít. C. 6,72 lít. D. 15,68 lít.
nhh = 0,2 + 0,5 + 0,3 = 1 (mol)
0oC, 1atm là đktc => Vhh = 1 .22,4 = 22,4 (l)
=>A
Trong một bình kín dung tích 20 lít có chứa 4,4 kg khí cacbonic ở nhiệt độ 27 ° C. Tính áp suất của khí trong bình. Biết thể tích của một mol khí ở điều kiện chuẩn là V 0 = 22,4 lít.
Gọi n là số mol khí cacbonic chứa trong bình: n = m/ μ , trong đó M là khối lượng khí cacbonic có trong bình, μ là khối lượng mol của khí cacbonic.
Ta có n = 100 mol
Nếu gọi V 0 là thể tích của lượng khí cacbonic ở điều kiện chuẩn ( p 0 = 1,013. 10 5 Pa; T 0 = 273 K) thì V 0 = n v 0
Áp dụng phương trình trạng thái của khí lí tưởng cho lượng khí cacbonic: