Nguyên tử R có cấu hình electron lớp ngoài cùng là ns 2 np 4 . Trong công thức hợp chất với H của nó có chứa 5,88% H về khối lượng. Nguyên tố R là
A. O.
B. Se.
C. Te.
D. S.
Mọi người giúp với. Nguyên tố r có cấu hình electron ngoài cùng là ns²np⁴. Hãy tìm công thức hợp chất của K với H và công thức oxit tương ứng với hóa trị cao nhất của R
Nguyên tố R có cấu hình electron lớp ngoài cùng là ns2np4. Công thức hợp chất của R với H và công thức oxit tương ứng với hóa trị cao nhất của R lần lượt là
A. RH2 và RO
B. RH2 và RO2
C. RH4 và RO2
D. RH2 và RO3
Đáp án D
R có 6e lớp ngoài cùng, hóa trị cao nhất với oxi = 6, hidro = 2.
Nguyên tố R có cấu hình electron lớp ngoài cùng là n s 2 n p 4 . Công thức hợp chất của R với H và công thức oxit tương ứng với hóa trị cao nhất của R lần lượt là
A. R H 2 và RO
B. R H 2 và R O 2
C. R H 4 và R O 2
D. R H 2 và R O 3
Chọn D
Nguyên tố R có cấu hình electron lớp ngoài cùng là ns2np4 → R thuộc nhóm VIA.
→ Công thức oxit cao nhất của R là RO3; công thức hợp chất khí với H của R là RH2.
Nguyên tử R có cấu hình e lớp ngoài cùng là ns²np⁴ trong công thức hợp chất với H của nó có chứa 5,88% H về khối lượng. Tìm nguyên tố R.
R có cấu hình e lớp ngoài cùng là ns2 np4\(\Rightarrow\) R thuộc nhóm VI A
\(\Rightarrow\) ct h/c khí với H: RH2
có: \(\frac{2}{R+2}\)= 0,0588
\(\Rightarrow\) R= 32
vậy R là lưu huỳnh
Nguyên tử của nguyên tố X có cấu hình electron lớp ngoài cùng là 3 s 2 , nguyên tử của nguyên tố Y có cấu hình electron lớp ngoài cùng là 2 s 2 2 p 3 . Công thức phân tử của hợp chất tạo bởi X và Y có dạng
![]()
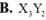
![]()
![]()
Nguyên tử của nguyên tố X có cấu hình electron lớp ngoài cùng là 3s2, nguyên tử của nguyên tố Y có cấu hình electron lớp ngoài cùng là 2s22p3. Công thức phân tử của hợp chất tạo bởi X và Y có dạng
A. X2Y3.
B. X3Y2.
C. X5Y2.
D. X2Y2.
Đáp án B
X là nguyên tố nhóm IIA (hóa trị II)
Y là nguyên tố nhóm VA (hóa trị III)
Như vậy, công thức hợp chất phải là X3Y2
nguyên tử của nguyên tố x có cấu hình electron lớp ngoài cùng là ns2 np4. trong hợp chất hydride (hợp chất của X với Hydrogen) nguyên tố x chiếm 94,12% về khối lượng a.Xác định phần trăm khối lượng của X trong oxide cao nhất b.Viết công thức oxide ứng với hóa trị cao nhất của x, hydroxide tương ứng và nêu tính chất acid - base của chúng
Câu 1: nguyên tử nguyên tố X có cấu hình electron lớp ngoài cùng là ns2 np3, trong hợp chất khí của X với Hidro x chiếm 82,35% về khối lượng. Nguyên tố X là: A. N(M=14) B. P(M=31) C. S(M=31) D. Si(M=28)
Câu 2: công thức hợp chất khí với Hidro của 2 nguyên tố phi kim x, y lần lượt là HX và H2Y. vị trí x và y trong bảng tuần hoàn là gì?
giúp mình gấp với ạ
Nguyên tử của nguyên tố M tạo được anion M2- có cấu hình electron ở phân lớp ngoài cùng là 3p6. Vị trí của nguyên tố M trong bảng tuần hoàn và công thức hợp chất có hóa trị cao nhất với oxi là:
A. ô số 8 chu kì 2 nhóm VIA, SO2
B. ô số 15 chu kì 3 nhóm VIA, SO3
C. ô số 16 chu kì 3 nhóm VIA, SO3
D. ô số 16 chu kì 3 nhóm IVA, SO2
Đáp án C
Hướng dẫn Vì M + 2e → M2- do đó cấu hình electron của M là 1s22s22p43s23p4 và ở ô số 16 chu kì 3 nhóm VIA. CT hợp chất có hóa trị cao nhất với oxi là SO3