Oxit cao nhất của một đơn chất R có dạng RO3. Trong hợp chất khí với hiđro thì R chiếm 97,531% về khối lượng. Nguyên tố R là
A. S
B. Se
C. P
D. Te
Oxit cao nhất của một đơn chất R có dạng RO3. Trong hợp chất khí với hiđro thì R chiếm 97,531% về khối lượng. Nguyên tố R là
A. S.
B. Se.
C. P.
D. Te.
Đáp án B
Oxit cao nhất của một đơn chất X có dạng RO3.
=> Hợp chất khí với Hidro là H2R.
Ta có:
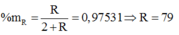
Vậy R là Se
1. Oxit cao nhất của R có công thức là RO3 , trong đó nguyên tố O chiếm 60 % về khối lượng . Xác định công thức của R , RO3 , hợp chất khí của R với H. 2.Hợp chất khí với hydro của R có công thức là RH 4 , trong đó nguyên tố H chiếm 25 % về khối lượng . Xác định công thức R , RH4 , oxit cao nhất của R 3.Trong hợp chất khí với hydro RH3 , nguyên tố R chiếm 82,35 % về khối lượng . Xác định công thức R , oxit cao nhất , hợp chất khí của R với H.
Oxit cao nhất của nguyên tố R có công thức RO3. Hợp chất khí của R với hiđro có 94,12 % R về khối lượng. R là
RO3 -> RH3
\(\%m_R=94,12\%\Rightarrow\%m_H=5,88\%\\ \Rightarrow M_{RH_2}=\dfrac{2}{5,88\%}\approx34\left(đ.v.C\right)\\ \Rightarrow M_R=32\left(đ.v.C\right)\\ \Rightarrow R:Lưu.huỳnh\left(S\right)\)
Oxit cao nhất của một nguyên tố R là RO3, trong hợp chất của nó với hiđro có 5,88% hiđro về khối lượng. Xác định nguyên tố R
Nguyên tố 'R' có oxit cao nhất là R2O3, => Hóa trị cao nhất của 'R' là 6
Hóa trị thấp nhất của R trong hợp chất với oxygen + Hóa trị của R trong hợp chất
thi với hydrogen = 8
=> Hóa trị của R trong hợp chất thi với hydrogen = 8 - 6 = 2
=> Công thức hợp chất thi với hydrogen là RH2
Ta có: %MH(R+H2) = (2/(R+2)) * 100
=> 5,88 = (2/(R+2)) * 100
=> R = 32
=> R là Sulfur (S)
Hợp chất khí của R với hiđro có công thức phân tử là RH3. Trong hợp chất oxit cao nhất của nguyên tố R, oxi chiếm 56,34% về khối lượng. Tổng số electron p trong nguyên tử nguyên tố R là: A. 9. B. 5. C. 3. D. 6.
Giúp mình với ạ mình k biết cách làm,mình cần gấp huhu:((
Hợp chất khí của R với hiđro có công thức phân tử là RH3.
Hợp chất oxit cao nhất của nguyên tố R là R2O5
Ta có \(\%O=\dfrac{16.5}{2R+16.5}.100=56,34\\ \Rightarrow R=31\left(Photpho-P\right)\\ \Rightarrow Z_R=SốE=15\)
Công thức phân tử hợp chất khí tạo bởi nguyên tố R và hiđro là RH3. Trong oxit mà R có hóa trị cao nhất thì oxi chiếm 74,07% về khối lượng. Nguyên tố R là
A. S. B. As. C. N. D. P.
Oxit cao nhất của một nguyên tố R là RO2. Trong công thức hợp chất khí với hiđro, H chiếm 25% về khối lượng . Nguyên tố R là
CT hợp chất khí với hidro là RH4
Có \(\dfrac{4}{M_R+4}.100\%=25\%=>M_R=12\left(C\right)\)
Một nguyên tố có công thức oxit cao nhất là R2O7, nguyên tố này tạo với hiđro một chất khí trong đó hiđro chiếm 0,78% về khối lượng. Xác định nguyên tố R; công thức hợp chất khí với Hidro; hợp chất với oxi.
Công thức phân tử của hợp chất khí tạo bởi nguyên tố R và hiđro là RH3. Trong oxit mà R có hoá trị cao nhất thì oxi chiếm 74,07% về khối lượng. Nguyên tố R là
A. S
B. N
C. P
D. As
Đáp án : B
Qui tắc bát tử : Do số hóa trị trong hợp chất với H là 3
=> Số hóa trị trong hợp chất oxit cao nhất là 8 – 3 = 5
=> R2O5 => %mO(oxit) = 5 . 16 2 R + 5 . 16 . 100 % = 74 , 07 %
=> R = 14 (N)
=> B