Hòa tan hoàn toàn hỗn hợp FeS và FeCO3 bằng dung dịch HNO3 đặc nóng thu được hỗn hợp khí A gồm hai khí X và Y có tỉ khối so với H2 là 22,805. Công thức hóa học của X và Y là:
A. H2S và CO2
B. SO2 và CO2
C. NO2 và CO2
D. NO2 và SO2
Hòa tan hoàn toàn hỗn hợp FeS và FeCO3 bằng dung dịch HNO3 đặc nóng thu được hỗn hợp khí A gồm hai khí X và Y có tỉ khối so với H2 là 22,805. Công thức hóa học của X và Y là
A. H2S và CO2
B. SO2 và CO2
C. NO2 và CO2
D. NO2 và SO2
Đáp án C
Vì hỗn hợp ban đầu có chứa FeCO3 nên khí thoát ra chắc chắn chứa CO2.
Có (hỗn hợp khí) = 22,805.2 = 45,61
Mà
Nên khí còn lại trong hỗn hợp cần có khối lượng mol lớn hơn 45,61.
Mặt khác, trong hỗn hợp chất phản ứng ban đầu có chứa FeS nên khí còn lại có thế là SO2 hoặc sản phẩm khử của
Do nên thỏa mãn.
Tuy nhiên vì dung dịch HNO3 sử dụng là đặc nóng nên sản phẩm khử chỉ có thể là NO2 (khi đó sản phẩm sau phản ứng không có SO2 mà thay vào đó là S hoặc H2SO4). Do đó hỗn hợp khí chứa NO2 và CO2.
Hòa tan hoàn toàn hỗn hợp FeS và FeCO3 bằng một lượng dung dịch H2SO4 đặc nóng thu được hỗn hợp gồm hai khí X, Y. Công thức hóa học của X, Y lần lượt là
A. H2S và SO2
B. H2S và CO2
C. SO2 và CO
D. SO2 và CO2
Hòa tan hoàn toàn hỗn hợp FeS và FeCO 3 bằng một lượng dung dịch H 2 SO 4 đặc nóng thu được hỗn hợp gồm hai khí X, Y. Công thức hóa học của X, Y lần lượt là:
A. H 2 S và SO 2
B. H 2 S và CO 2
C. SO 2 và CO
D. SO 2 và CO 2
Hòa tan hoàn toàn hỗn hợp FeS và FeCO3 bằng dung dịch HNO3 đặc, nóng, dư thu được hỗn hợp gồm 2 khí CO2 và NO2 (NO2 là sản phẩm khử duy nhất của HNO3) có tỉ khối hơi so với hiđro bằng 22,909. Phần trăm khối lượng của FeS trong hỗn hợp ban đầu là
A. 43,14%.
B. 44,47%.
C. 56,86%.
D. 83,66%.
Chia hỗn hợp X gồm Fe, Fe3O4, Fe(OH)3 và FeCO3 thành hai phần bằng nhau. Hòa tan hoàn toàn một phần trong dung dịch HCl dư, thu được 0,1 mol hỗn hợp hai khí có tỉ khối so với H2 bằng 9,4 và dung dịch Y. Cho hai phần tác dụng với lượng dư dung dịch H2SO4 đặc, nóng. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Z và 0,2075 mol hỗn hợp khí T gồm CO2 và SO2 (sản phẩm khử duy nhất của S+6). Khối lượng của FeCl2 có trong dung dịch Y là
A. 25,307 gam.
B. 27,305 gam.
C. 23,705 gam.
D. 25,075 gam.
Cho 0,2 mol hỗn hợp khí Y gồm CO và H 2 (có tỉ khối so với H 2 bằng 4,25) tác dụng với 20 gam hỗn hợp X gồm Fe, F e C O 3 , F e 2 O 3 sau một thời gian thu được hỗn hợp rắn X 1 và hỗn hợp khí Y 1 . Cho Y 1 hấp thụ vào dung dịch dư, sau phản ứng thu được 7 gam kết tủa và thoát ra 0,06 mol hỗn hợp khí Y 2 (có tỉ khối so với H 2 bằng 7,5). Hòa tan X 1 bằng lượng dư dung dịch H N O 3 thu được dung dịch Z và 0,62 mol hỗn hợp hai khí trong đó có một khí màu nâu đỏ là sản phẩm khứ duy nhất của N + 5 Nếu cho 20 gam X tác dụng với dung dịch H 2 S O 4 (đặc, nóng, dư) thì thu được 0,225 mol hỗn hợp S O 2 và C O 2 Phần trăm khối lượng của F e 2 O 3 trong X là
A. 32%
B. 48%
C. 16%
D. 40%
Hòa tan hoàn toàn 12,15 gam Al bằng dung dịch HNO3 loãng (dư) thu được dung dịch X và 1,344 lít (đktc) hỗn hợp khí Y gồm hai khí là N2O và N2. Tỉ khối của hỗn hợp khí Y so với khí H2 là 18. Cô cạn dung dịch X, thu được m gam chất rắn khan. Giá trị của m là:
A. 103,95
B. 106,65
C. 45,63
D. 95,85
Ta có nhhY= x+y= 1,344/ 22,4= 0,06 mol
mhhY=44x + 28y= 0,06.18.2
Giải hệ trên được x= 0,03 và y= 0,03
nAl= 0,45 mol= nAl(NO3)3
Quá trình cho e:
Al→ Al3++ 3e (1)
0,45→ 1,35 mol
Quá trình nhận e:
2NO3-+ 10e+ 12H+ → N2 + 6H2O (2)
0,3 ← 0,03 mol
2NO3-+ 8e+ 10H+ → N2O + 5H2O (3)
0,24 ← 0,03 mol
Tổng số mol e nhận ở (2) và (3) là ne nhận= 0,3+ 0,24= 0,54 mol <1,35 mol
Do đó còn xảy ra quá trình nhận e: ne nhận ở (4)= 1,35- 0,54= 0,81 mol
NO3-+ 8e+ 10H+ → NH4++ 3H2O (4)
0,81 → 0, 10125 mol
Dung dịch X chứa 0,45 mol Al(NO3)3 và 0,10125 mol NH4NO3
→m=103,95 gam
Đáp án A
Cho 0,2 mol hỗn hợp khí Y gồm CO và H 2 (có tỉ khối so với H 2 bằng 4,25) tác dụng với 20 gam hỗn hợp X gồm F e , F e C O 3 , F e 2 O 3 sau một thời gian thu được hỗn hợp rắn X 1 và hỗn hợp khí Y 1 . Cho Y 1 hấp thụ vào dung dịch C a ( O H ) 2 dư, sau phản ứng thu được 7 gam kết tủa và thoát ra 0,06 mol hỗn hợp khí Y 2 (có tỉ khối so với H 2 bằng 7,5). Hòa tan X 1 bằng lượng dư dung dịch H N O 3 thu được dung dịch Z và 0,62 mol hỗn hợp hai khí trong đó có một khí màu nâu đỏ là sản phẩm khứ duy nhất của N + 5 Nếu cho 20 gam X tác dụng với dung dịch H 2 S O 4 (đặc, nóng, dư) thì thu được 0,225 mol hỗn hợp S O 2 v à C O 2 Phần trăm khối lượng của F e 2 O 3 trong X là
A. 32%
B. 48%
C. 16%
D. 40%
Đáp án D
Sơ đồ quá trình phản ứng
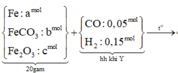
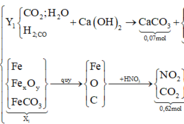

Hướng tư duy 1:
+ Xét khí Y1 có ![]()
![]()
+Xét hỗn hợp X1(sau khi quy đổi) có:
![]()
![]()
Do đó, trong 0,62 mol hỗn hợp khí có (0,67-b) mol NO (khí hóa nâu)
Bảo toàn nguyên tố Fe có:
![]()
= a + b = 2c mol
Bảo toàn O: ![]()
![]()
![]()
Bảo toàn e:
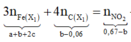
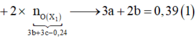
+ Xét hỗn hợp khí sau khi tác dụng H 2 S O 4 ta có:
![]()
![]()
Mà ![]()
=> giải hệ (1), (2), (3) ta được
![]()
Hướng tư duy 2:
Gọi x là số mol F e C O 3 bị nhiệt phân
Bảo toàn C ta có: ![]() = 0,05 mol
= 0,05 mol
=>
n
C
O
(
p
h
ả
n
ứ
n
g
)
= ![]()
![]()
+ Gọi a là số mol
F
e
C
O
3
phản ứng với
H
N
O
3
có ngay ![]()
+ Cho X phản ứng với H 2 S O 4 (đặc, nóng): (X chứa a+0,05 mol F e C O 3 )
Bảo toàn nguyên tố C có: ![]()
![]()
Bảo toàn e trong phản ứng với H N O 3 và H 2 S O 4 đặc nóng, có hệ:
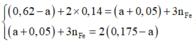
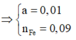
![]()
![]()
Hòa tan hoàn toàn 12,42 gam Al bằng dung dịch HNO 3 loãng (dư), thu được dung dịch X và 1,344 lít (đktc) hỗn hợp khí Y gồm hai khí là N 2 O và N 2 . Tỉ khối của hỗn hợp khí Y so với khí H 2 là 18, cô cạn dug dịch X , thu được m gam chất rắn khan. Giá trị của m là
A. 34,08
B. 38,34
C. 106,38
D. 97,98.
Đáp án C
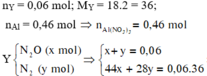
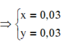

![]()
Þ m = 0,46.213 + 0,105.80 = 106,38 ( gam)