Một loại phân ure có chứa 95% (NH2)2CO, còn lại là (NH4)2CO3. Độ dinh dưỡng của loại phân này là:
A. 46,00%
B. 43,56%
C. 44,33%
D. 45,79%
Ure là loại phân đạm có hàm lượng dinh dưỡng cao nhất và được sử dụng phổ biến nhất trên thế giới do có khả năng phát huy tác dụng trên nhiều loại đất khác nhau (kể cả đất nhiễm phèn) và đối với nhiều loại cây trồng khác nhau. Trong quá trình bảo quản, ure dễ bị hút ẩm và chuyển hóa một phần thành (NH4)2CO3. Một loại phân ure chứa 95% (NH2)2CO, còn lại là (NH4)2CO3. Độ dinh dưỡng của loại phân này là
A. 44,33%
B. 46,00%
C. 45,79%
D. 43,56%
Ure là loại phân đạm có hàm lượng dinh dưỡng cao nhất và được sử dụng phổ biến nhất trên thế giới do có khả năng phát huy tác dụng trên nhiều loại đất khác nhau (kể cả đất nhiễm phèn) và đối với nhiều loại cây trồng khác nhau. Trong quá trình bảo quản, ure dễ bị hút ẩm và chuyển hóa một phần thành (NH4)2CO3. Một loại phân ure chứa 95% (NH2)2CO, còn lại là (NH4)2CO3. Độ dinh dưỡng của loại phân này là
A. 44,33%
B. 46,00%
C. 45,79%
D. 43,56%
Đáp án C
→ % N 2 = 95 . 28 60 + 5 28 96 = 45 , 79 %
Tính độ dinh dưỡng của một loại phân đạm ure (NH2)2CO có lẫn 16% tạp chất trơ(biết tạp chất trơ ko chứa nguyên tố Nitơ)
\(GS:\)
\(m_{ure}=100\left(g\right)\)
\(\Rightarrow m_{\left(NH_2\right)_2CO}=84\left(g\right)\)
\(n_{\left(NH_2\right)_2CO}=\dfrac{84}{60}=1.4\left(mol\right)\)
\(\Rightarrow n_N=1.4\cdot2=2.8\left(mol\right)\)
\(\%N=\dfrac{2.8\cdot14}{100}\cdot100\%=39.2\%\)
Các nhận xét sau:
(a) Thành phần chính của phân đạm ure là (NH2)2CO
(b) Phân đạm amoni nên bón cho các loại đất chua
(c) Tro thực vật cũng là một loại phân kali vì có chứa K2CO3
(d) Độ dinh dưỡng của phân lân được đánh giá bằng phần trăm khối lượng photpho
(e) NPK là một loại phân bón hỗn hợp
(f) Người ta dùng loại phân bón chứa nguyên tố kali để tăng cường sức chống bệnh , chống rét và chịu hạn cho cây
Số nhận xét sai là
A. 1
B. 2
C. 4
D. 3
Đáp án B
Các nhận xét sai:
(b) sai: Phân đạm không nên bón cho loại đất chua vì phân đạm có tính axit do NH4+ thủy phân ra
(d) sai vì độ dinh dưỡng của phân lân được đánh giá bằng phần trăm khối lượng P2O5.
Một loại phân kali có chứa 87% K2SO4 còn lại là các tạp chất không chứa kali, độ dinh dưỡng của loại phân bón này là:
A. 44,8%.
B. 54,0%.
C. 39,0%.
D. 47,0%.
Đáp án D
Độ dinh dưỡng của phân kali tính bằng %mK2O trong tổng khối lượng phân bón.
Giả sử mphân = 100g => mK2SO4 = 87g
174g K2SO4 qui về thành 94g K2O
=>87g K2SO4 qui về thành 47g K2O
=> Độ dinh dưỡng = 47%
Một loại phân kali có chứa 87% K2SO4 còn lại là các tạp chất không chứa kali, độ dinh dưỡng của loại phân bón này là
A. 44,8%
B. 54,0%
C. 39,0%
D. 47,0%
Một loại phân kali có chứa 68,56% KNO3, còn lại là gồm các chất không chứa kali. Độ dinh dưỡng của loại phân kali này là
A. 43,3%.
B. 35,9%.
C. 31,9%.
D. 86,5%.
Đáp án C
Độ dinh dưỡng của phân kali là tỉ lệ %K2O so với khối lượng phân
Độ dinh dưỡng 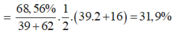
Một loại phân supephotphat kép có chứa 55,9% muối canxi đihidrophotphat, còn lại gồm các chất không chứa photpho. Độ dinh dưỡng của loại phân này là
A. 33,92%
B. 39,76%
C. 42,25%
D. 45,75%
Đáp án A
Giả sử khối lượng của mẫu phân này là 100 gam.
mCa(H2PO4)2=55,9 gam => nCa(H2PO4)2 = 55,9/234 = 0,239 mol
BTNT P: => nP2O5 = nCa(H2PO4)2 = 0,239 mol
=>%mP2O5 = 0,239.142/100 = 33,92%
Một loại phân supephotphat kép có chứa 55,9% muối canxi đihidrophotphat, còn lại gồm các chất không chứa photpho. Độ dinh dưỡng của loại phân này là
A. 33,92%
B. 39,76%
C. 42,25%
D. 45,75%
Đáp án A
Giả sử khối lượng của mẫu phân này là 100 gam.
mCa(H2PO4)2=55,9 gam => nCa(H2PO4)2 = 55,9/234 = 0,239 mol
BTNT P: => nP2O5 = nCa(H2PO4)2 = 0,239 mol
=>%mP2O5 = 0,239.142/100 = 33,92%