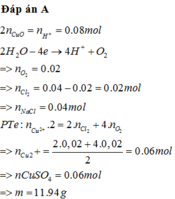Điện phân (điện cực trơ, màng ngăn xốp) một dung dịch chứa m gam hỗn hợp CuSO 4 và NaCl cho tới khi nước bắt đầu bị điện phân ở cả hai điện cực thì dừng lại, thu được dung dịch X và 0,56 lít khí (đktc) ở anot. Dung dịch X có thể hoà tan tối đa 0,85 gam Al 2 O 3 . Khối lượng của m là :
A. 5,5916
B. 6,2125
C. 5,5916 hoặc 7,4625
D. 5,5916 hoặc 6,2125