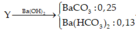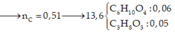Hòa tan CaO bằng A thu được dung dịch B. Thổi khí D vào dung dịch B thấy xuất hiện kết tủa E. D được sinh ra khi hòa tan Cu bằng dung dịch axit đặc nóng. A, B, D, E theo đúng thứ tự là dãy chất nào sau đây?
A. HCl, CaCl2, CO2, CaCO3
B. H2O, Ca(OH)2, CO2, CaCO3
C. H2SO4, Ca(OH)2, SO2, CaSO4
D. H2O, Ca(OH)2, SO2, CaSO3

Những câu hỏi liên quan
Cho các phát biểu sau: (a) Mg cháy trong khí CO2 ở nhiệt độ cao. (b) Thổi khí NH3 qua CrO3 đun nóng thấy chất rắn chuyển từ màu đỏ sang màu đen. (c) Ở nhiệt độ cao, tất cả các kim loại kiềm thổ đều phản ứng được với nước. (d) Hỗn hợp KNO3 và Cu (tỉ lệ mol 1 : 1) tan hết trong dung dịch NaHSO4 dư. (e) Cho NH3 dư vào dung dịch AlCl3 thu được kết tủa trắng keo, sau đó kết tủa tan dần. Số phát biểu đúng là A. 2. B. 5. ...
Đọc tiếp
Cho các phát biểu sau:
(a) Mg cháy trong khí CO2 ở nhiệt độ cao.
(b) Thổi khí NH3 qua CrO3 đun nóng thấy chất rắn chuyển từ màu đỏ sang màu đen.
(c) Ở nhiệt độ cao, tất cả các kim loại kiềm thổ đều phản ứng được với nước.
(d) Hỗn hợp KNO3 và Cu (tỉ lệ mol 1 : 1) tan hết trong dung dịch NaHSO4 dư.
(e) Cho NH3 dư vào dung dịch AlCl3 thu được kết tủa trắng keo, sau đó kết tủa tan dần.
Số phát biểu đúng là
A. 2.
B. 5.
C. 4.
D. 3
Đốt cháy hoàn toàn 13,36 gam hỗn hợp X gồm axit metacrylic, axit adipic, axit axetic và glixerol (trong đó số mol axit metacrylic bằng số mol axit axetic) bằng dư, thu được hỗn hợp Y gồm khí và hơi. Dẫn Y vào dung dịch chưa 0,38 mol thu được 49,25 gam kết tủa và dung dịch Z. Đun nóng Z lại xuất hiện kết tủa. Cho 13,36 gam hỗn hợp X tác dụng với 140 ml dung dịch KOH 1M, sau khi các phản ứng xảy ra hoàn toàn, cô cạn dung dịch thu được chất rắn kh...
Đọc tiếp
Đốt cháy hoàn toàn 13,36 gam hỗn hợp X gồm axit metacrylic, axit adipic, axit axetic và glixerol (trong đó số mol axit metacrylic bằng số mol axit axetic) bằng dư, thu được hỗn hợp Y gồm khí và hơi. Dẫn Y vào dung dịch chưa 0,38 mol thu được 49,25 gam kết tủa và dung dịch Z. Đun nóng Z lại xuất hiện kết tủa. Cho 13,36 gam hỗn hợp X tác dụng với 140 ml dung dịch KOH 1M, sau khi các phản ứng xảy ra hoàn toàn, cô cạn dung dịch thu được chất rắn khan có khối lượng là:
A. 18,68 gam
B. 14,44 gam
C. 19,04 gam
D. 13,32 gam
Đốt cháy hoàn toàn m gam FeS2 bằng một lượng O2 vừa đủ, thu được khí X. Hấp thụ hết X vào 1 lít dung dịch chứa Ba(OH)2 0,15M và KOH 0,1M, thu được dung dịch Y và 21,7 gam kết tủa. Cho Y vào dung dịch NaOH, thấy xuất hiện thêm kết tủa. Giá trị của m là: A. 23,2 B. 12,6 C. 18,0 D. 24,0
Đọc tiếp
Đốt cháy hoàn toàn m gam FeS2 bằng một lượng O2 vừa đủ, thu được khí X. Hấp thụ hết X vào 1 lít dung dịch chứa Ba(OH)2 0,15M và KOH 0,1M, thu được dung dịch Y và 21,7 gam kết tủa. Cho Y vào dung dịch NaOH, thấy xuất hiện thêm kết tủa. Giá trị của m là:
A. 23,2
B. 12,6
C. 18,0
D. 24,0
Đáp án C
Pt pư:
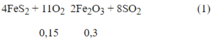
Ta có: nBaC03 = 0,15 mol
nKOH = 0,1 mol ⇒ nBa2+ = 0,15 mol ; nOH- = 0,4 mol
Khi cho SO2 vào dung dịch Y thu được 21,7 (g) BaSO3. Cho Y tác dụng với dung dịch NaOH thấy xuất hiện thêm kết tủa, chứng tỏ trong dung dịch Y có ion HSO3-.
Vì: Ba2+ + HSO3- + OH- " BaSO3 + H2O
Ta có: nBaC03 = 0,1 mol
Ptpứ:
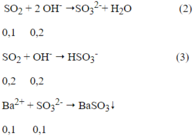
Ta có: nOH- = 0,4 - 0,2 = 0,2 mol
Theo ptpư (2), (3) ta có: n SO2= 0,1 + 0,2 = 0,3 mol
Theo ptpư (1) ta có: n FeS2 = ½ n SO2= 0,15 mol ⇒ m FeS2 = 120.0,15 = 18(g)
Đúng 0
Bình luận (0)
ygHòa tan hết 19, 1 gam hỗn hợp A gồm 2 muối Na2CO3 và K2CO3 bằng dung dịch HNO3 12,6% đủ được 3,36 lít 1 chất khí ở đktc và dung dịch B . Cho 600ml dung dịch axit clohidric 1M vào dung dịch B , dung dịch thu được có khả năng hòa tan bao nhiêu gam bột Cu ? tính thể tích khí NO ( sản phẩm duy nhất ) thu được ở đktc
Cho 6,4g hỗn hợp A gồm Fe và Mg phản ứng với 100g dung dịch H2SO4 loãng vừa đủ được 3,584 lít (đkc) và dung dịch B a, tính % theo khối lượng mỗi chất có trong A b, tính C% của từng muối trong dung dịch B c, đốt cháy 6,4g hỗn hợp A ở trên với hỗn hợp khí X gồm Cl2 và O2, sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua (không có khí dư). Hòa tan Y bằng 1 lượng vừa đủ 120ml dung dịch HCl 2M thu được dung dịch Z. Cho AgNO3 dư v...
Đọc tiếp
Cho 6,4g hỗn hợp A gồm Fe và Mg phản ứng với 100g dung dịch H2SO4 loãng vừa đủ được 3,584 lít (đkc) và dung dịch B a, tính % theo khối lượng mỗi chất có trong A b, tính C% của từng muối trong dung dịch B c, đốt cháy 6,4g hỗn hợp A ở trên với hỗn hợp khí X gồm Cl2 và O2, sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua (không có khí dư). Hòa tan Y bằng 1 lượng vừa đủ 120ml dung dịch HCl 2M thu được dung dịch Z. Cho AgNO3 dư vào dung dịch Z thu được 56,69g kết tủa. Tính % theo thể tính của Cl2 trong hỗn hợp X
Hòa tan hỗn hợp gồm: K2O, BaO, Al2O3, Fe3O4 vào nước (dư) thu được dung dịch X và chất rắn Y. Sục khí CO2 đến dư vào dung dịch X, sau khi các phản ứng xảy ra hoàn toàn thu được kết tủa là: A. K2CO3 B. Fe(OH)3 C. Al(OH)3 D. BaCO3
Đọc tiếp
Hòa tan hỗn hợp gồm: K2O, BaO, Al2O3, Fe3O4 vào nước (dư) thu được dung dịch X và chất rắn Y. Sục khí CO2 đến dư vào dung dịch X, sau khi các phản ứng xảy ra hoàn toàn thu được kết tủa là:
A. K2CO3
B. Fe(OH)3
C. Al(OH)3
D. BaCO3
Đáp án C
Phương trình phản ứng:
K2O + H2O → 2KOH
BaO + 2H2O → Ba(OH)2
Al2O3 + OH- → 2AlO2- + H2O
⇒Chất rắn Y: Fe3O4, dung dịch X chứa ion AlO2-
AlO2- + CO2 + H2O → Al(OH)3 + HCO3-
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 20,88 gam một oxit sắt bằng dung dịch H2SO4 đặc, nóng thu được dung dịch X và 3,248 lít khí SO2 (sản phầm khử duy nhất, ở đktc). Cô cạn dung dịch X, thu được m gam muối sunfat khan. Giá trị của m là:
A. 52,2
B. 48,4
C. 54,0
D. 58,0
Đáp án D
Ta có: = 0,145 mol
Quy đổi 20,88 g oxit sắt FexOy thành 20,88 g Fe và O
Gọi nFe = x mol; nO = y mol
Quá trình nhường electron:
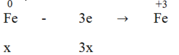
Quá trình nhận electron:
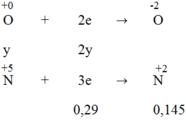
Áp dụng định luật bảo toàn electron, ta có:
3x = 2y + 0,29 → 3x - 2y = 0,29 (1)
Mặt khác: 56x + 16y = 20,88 (2)
Từ (1) và (2) → x = 0,29 và y = 0,29
Muối sinh ra là muối Fe2(SO4)3. Áp dụng ĐL bảo toàn nguyên tố ta có:
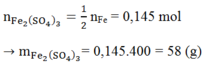
Đúng 0
Bình luận (0)
Hòa tan hết 0,81 gam bột nhôm vào 550ml dung dịch HCl 0,2M thu được dung dịch A. Tính thể tích dung dịch NaOH 0,5M cần thêm vào dung dịch A để thu được lượng kết tủa lớn nhất.
A. 0,22l
B. 0.2l
C. 0,15l
D. 0,12l
Đáp án A
Số mol Al = 0.81/27= 0,03 (mol); số mol HCl = 0,55.0,2 = 0,11 (mol)
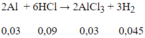
Dung dịch A thu được gồm AlCl3 = 0,03 mol; HCl = 0,11 - 0,09 = 0,02 mol.
Để có lượng kết tủa lớn nhất:
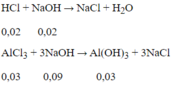
Thể tích dung dịch NaOH cần dùng
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn m gam Fe bằng dung dịch HNO3 thu được dung dịch X và 1,12 lít NO (đktc). Thêm dung dịch chứa 0,1 mol HCl vào dung dịch X thì thấy khí NO tiếp tục thoát ra và thu được dung dịch Y. Để phản ứng hết với các chất trong dung dịch Y cần 115 ml dung dịch NaOH 2M. Giá trị của m là A. 3,36 B. 4,2 C. 3,92 D. 3,08
Đọc tiếp
Hòa tan hoàn toàn m gam Fe bằng dung dịch HNO3 thu được dung dịch X và 1,12 lít NO (đktc). Thêm dung dịch chứa 0,1 mol HCl vào dung dịch X thì thấy khí NO tiếp tục thoát ra và thu được dung dịch Y. Để phản ứng hết với các chất trong dung dịch Y cần 115 ml dung dịch NaOH 2M. Giá trị của m là
A. 3,36
B. 4,2
C. 3,92
D. 3,08
Đáp án : C
Fe được hòa tan hoàn toàn bởi dd HNO3 thu được dd X, khi thêm HCl vào X có khí NO thoát ra → trong X có ion Fe2+ → HNO3 đã phản ứng hết
n(NO) = 1,12/22,4 = 0,05 mol
Fe + 4HNO3 → Fe(NO3)3 + NO + 4H2O
0,05 -> 0,2 -> 0,05
Fe + 2Fe(NO3)3 → 3Fe(NO3)2
x -> 3x
Theo ĐL bảo toàn nguyên tố, số mol NO3- có trong muối:
n(NO3- trong muối) = n(HNO3) - n(NO) = 0,15 mol
n(NaOH) = 0,115.2 = 0,23 mol
Sau khi NaOH pư hoàn toàn với các chất trong dd Y, dung dịch thu được có:
n(Na+) = n(NaOH) = 0,23 mol; n(Cl-) = n(HCl) = 0,1 mol → n(NO3-) = n(Na+) - n(Cl-) = 0,23 - 0,1 = 0,13 mol → Số mol NO3- bị Fe2+ khử: 0,15 - 0,13 = 0,02 mol
NO3- + 3Fe2+ + 4H+ → 3Fe3+ + NO + 2H2O
0,02 -> 0,06 -> 0,08
NO3- và H+ đều dư (H+ dư 0,02mol) → Fe2+ đã phản ứng hết
→ 3x = 0,06 → x = 0,02 mol
Tổng số mol Fe: n(Fe) = 0,05 + x = 0,07 mol
Khối lượng Fe đã sử dụng: m(Fe) = 0,07.56 = 3,92g
Đúng 0
Bình luận (0)