Giá trị pH của dung dịch HCl 0,001M là
A. 3
B. 2
C. 1
D. 4
Giá trị pH của dung dịch HCl 0,001M là
A. 3.
B. 2.
C. 1.
D. 4.
Giá trị pH của dung dịch HCl 0,001M là
A. 3.
B. 2.
C. 1.
D. 4.
pH = -lg[H+] = -lg(0,001) = 3
Đáp án A
Trộn lẫn 300ml dung dịch NaOH 0,001M vào 300ml dung dịch HCl 0,003M thu được dung dịch X có giá trị pH là?
A. 1
B. 2
C. 3
D. 4
Tính pH của các dung dịch sau :
a/ 100 ml dung dịch X có hòa tan 2,24 lít khí HCl ( đktc )
b/ Dung dịch HNO3 0,001M
c/ Dung dịch H2SO4 0,0005M
d/ Dung dịch NaOH 0,001M
e/ Dung dịch Ba(OH)2 0,005M
f/ Dung dịch CH3COOH 0,01M ( độ điện li \(\alpha=4,25\%\))
HELP ME !!!!!
Tính pH của các dung dịch sau khi trộn:
a. Trộn 100 ml dung dịch HCl 0,002M với 400 ml dung dịch H2SO4 0,0025M
b.Pha thêm 200 ml H2O vào 300 ml dung dịch HCl có pH=3
c. Trộn 200 ml dung dịch KOH 0,001M với 300 ml dung dịch NaOH 0,001M
Có 5 dung dịch NH3, HCl, NH4Cl, Na2CO3, CH3COOH được đánh ngẫu nhiên là A, B, C, D, E. Giá trị pH và khả năng dẫn điện của dung dịch theo bảng sau:
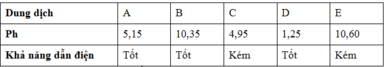
Các dung dịch A, B, C, D, E lần lượt là?
A. NH4Cl, NH3, CH3COOH, HCl, Na2CO3
B. NHp, Na2CO3, CH3COOH, HCl, NH3
C. CH3COOH, NH3, NH4Cl, HCl, Na2CO3
D. Na2CO3, HCl, NH3, NH4Cl, CH3COOH
Chọn đáp án B.
Một chất dẫn điện được khi tan trong nước phân ly thành các ion âm và ion dương. Số ion càng nhiều thì khả năng dẫn điện càng tốt, cũng như chất phân ly mạnh dẫn điện tốt hơn chất phân ly kém.
ü Các chất dẫn điện tốt là: HCl, NH4Cl, Na2CO3 (đây là những chất điện ly mạnh).
ü Các chất dẫn điện kém là: NH3, CH3COOH.
· Trong các chất dẫn điện tốt, HCl là axit mạnh nên dung dịch có pH thấp nhất => D là HCl.
Na2CO3 là muối của kim loại mạnh, axit yếu nên dung dịch có tính bazơ, pH > 7 => B là Na2CO3.
Còn lại chất A dẫn điện tốt là NH4Cl.
· Trong các chất dẫn điện kém, NH3 có tính bazơ (pH > 7), CH3COOH có tính axit (pH < 7)
=> E là NH3, C là CH3COOH.
Có 5 dung dịch NH3, HCl, NH4Cl, Na2CO3, CH3COOH được đánh ngẫu nhiên là A, B, C, D, E. Giá trị pH và khả năng dẫn điện của dung dịch theo bảng sau:
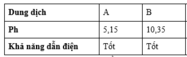
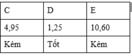
Các dung dịch A, B, C, D, E lần lượt là?
A. N H 4 C l , N H 3 , C H 3 C O O H , HCl, N a 2 C O 3
B. NHp, N a 2 C O 3 , C H 3 C O O H , HCl, N H 3
C. C H 3 C O O H , N H 3 , N H 4 C l , HCl, N a 2 C O 3
D. N a 2 C O 3 , HCl, N H 3 , N H 4 C l , C H 3 C O O H
Đáp án B
Một chất dẫn điện được khi tan trong nước phân ly thành các ion âm và ion dương. Số ion càng nhiều thì khả năng dẫn điện càng tốt, cũng như chất phân ly mạnh dẫn điện tốt hơn chất phân ly kém.
Các chất dẫn điện tốt là: HCl, NH4Cl, Na2CO3 (đây là những chất điện ly mạnh).
Các chất dẫn điện kém là: NH3, CH3COOH.
• Trong các chất dẫn điện tốt, HCl là axit mạnh nên dung dịch có pH thấp nhất => D là HCl.
Na2CO3 là muối của kim loại mạnh, axit yếu nên dung dịch có tính bazơ, pH > 7 => B là Na2CO3.
Còn lại chất A dẫn điện tốt là NH4Cl.
• Trong các chất dẫn điện kém, NH3 có tính bazơ (pH > 7), CH3COOH có tính axit (pH < 7)
=> E là NH3, C là CH3COOH.
Có 5 dung dịch NH3, HCl, NH4Cl, Na2CO3, CH3COOH được đánh ngẫu nhiên là A, B, C, D, E. Giá trị pH và khả năng dẫn điện của dung dịch theo bảng sau
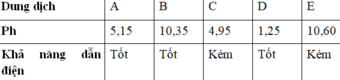
Các dung dịch A, B, C, D, E lần lượt là?
A. NH4Cl, NH3, CH3COOH, HCl, Na2CO3
B. NHp, Na2CO3, CH3COOH, HCl, NH3
C. CH3COOH, NH3, NH4Cl, HCl, Na2CO3
D. Na2CO3, HCl, NH3, NH4Cl, CH3COOH
Chọn đáp án B.
Một chất dẫn điện được khi tan trong nước phân ly thành các ion âm và ion dương.
Số ion càng nhiều thì khả năng dẫn điện càng tốt, cũng như chất phân ly mạnh dẫn điện tốt hơn chất phân ly kém.
ü Các chất dẫn điện tốt là: HCl, NH4Cl, Na2CO3 (đây là những chất điện ly mạnh).
ü Các chất dẫn điện kém là: NH3, CH3COOH.
· Trong các chất dẫn điện tốt, HCl là axit mạnh nên dung dịch có pH thấp nhất => D là HCl.
Na2CO3 là muối của kim loại mạnh, axit yếu nên dung dịch có tính bazơ, pH > 7
=> B là Na2CO3.
Còn lại chất A dẫn điện tốt là NH4Cl.
· Trong các chất dẫn điện kém, NH3 có tính bazơ (pH > 7), CH3COOH có tính axit (pH < 7)
=> E là NH3, C là CH3COOH
Sau phản ứng, \(V_{dd}= V_1 + V_2(lít)\)
Ta có : [H+] = 10-3 ⇒ \(n_{H_2SO_4} = 5.10^{-4}V_1(mol)\)
Lại có: \(n_{NaOH} = V_2.\dfrac{10^{-14}}{10^{-12}} = 0,01V_2(mol)\)
pH = 4 < 7 Chứng tỏ axit dư
2NaOH + H2SO4 → Na2SO4 + 2H2O
0,01V2.......5.10-3V2..................................(mol)
Suy ra : \(\dfrac{5.10^{-4}V_1-5.10^{-3}V_2}{V_1+V_2}.2 = 10^{-4}\\ \Rightarrow \dfrac{V_1}{V_2} = \dfrac{101}{9}\)
Đáp án B