Cho 1,35 gam hỗn hợp Cu, Mg, Al tác dụng với HNO3 dư được 896 ml (đktc) hỗn hợp gồm NO và NO2 có Mtrung bình = 42. Biết không thu được muối amoni. Tính tổng khối lượng muối nitrat sinh ra
A. 9,41 gam.
B. 10,08 gam.
C. 5,07 gam.
D. 8,15 gam.
Cho 1,35 gam hỗn hợp Cu, Mg, Al tác dụng với HNO3 dư được 896 ml (đktc) hỗn hợp gồm NO và NO2 có Mtrung bình = 42. Biết không thu được muối amoni. Tính tổng khối lượng muối nitrat sinh ra
A. 9,41 gam.
B. 10,08 gam.
C. 5,07 gam.
D. 8,15 gam.
Chọn đáp án C
Đặt số mol của NO = x và NO2 = y mol
Ta có hệ
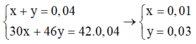
Luôn có mmuối = mkl + mNO3- = 1,35 + 62.∑ne trao đổi = 1,35 + 62. (0,01. 3 + 0,03) = 5,07 gam
⇒ Chọn C
Cho 1,35 gam hỗn hợp Cu, Mg, Al tác dụng với HNO3 dư được 896ml hỗn hợp gồm NO và NO2 có M = 42 . Tính tổng khối lượng muối nitrat sinh ra (khí ở đktc).
Gọi \(n_{NO} = a ; n_{NO_2} = b\)
Ta có :
\(a + b = \dfrac{896}{1000.22,4} = 0,04\\ 30a + 46b = 0,04.42\)
Suy ra a = 0,01 ; b = 0,03
Giả sử không có muối amoni tạo thành.
\(n_{NO_3^-} = n_{e\ trao\ đổi} = 3n_{NO} + n_{NO_2} = 0,06(mol)\)
\(m_{muối} = m_{kim\ loại} + m_{NO_3^-} = 1,35 + 0,06.62 = 5,07(gam)\)
Cho 1,35 gam hỗn hợp gồm Cu, Mg, Al tác dụng với dung dịch HNO3 dư, thu được 1,12 lít (đktc) hỗn hợp khí NO và NO2 có tỉ khối so với hiđro bằng 20. Tổng khối lượng muối nitrat sinh ra là
A. 66,75 gam.
B. 33,35 gam.
C. 6,775 gam.
D. 3,335 gam.
Đáp án C
Gọi n N O = a n N O 2 = b
Có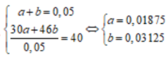
Vậy
m m u ố i = m k i m l o ạ i + m N O 3 -
=1 1,35+62.0,0875 = 6,775 (gam)
Cho 1,35 gam hỗn hợp gồm Cu, Mg, Al tác dụng với dung dịch HNO3 dư, thu được 1,12 lít (đktc) hỗn hợp khí NO và NO2 có tỉ khối so với hiđro bằng 20. Tổng khối lượng muối nitrat sinh ra là
A. 66,75 gam.
B. 33,35 gam.
C. 6,775 gam.
D. 3,335 gam.
Câu 2: Cho 1,35 gam hỗn hợp A gồm Cu, Mg, Al tác dụng với HNO3 dư được 1,12 lít NO và NO2 có khối lượng mol trung bình là 42,8. Biết thể tích khí đo ở đktc. Tổng khối lượng muối nitrat sinh ra là?
Theo gt ta có: $n_{NO}=0,01(mol);n_{NO_2}=0,04(mol)$
Bảo toàn e ta có: $n_{e}=n_{NO_3^-/trongmuoi}=0,07(mol)$
$\Rightarrow m_{muoi}=1,35+62.0,07=5,69(g)$
\(n_{No}=a\left(mol\right),n_{NO_2}=b\left(mol\right)\)
\(\Rightarrow a+b=0.05\)
\(m=30a+46b=0.05\cdot42.8=2.14\left(g\right)\)
\(\Rightarrow a=0.01,b=0.04\)
\(m_{Muối}=m_{kl}+m_{NO_3^-}=1.35+62\cdot\left(0.01\cdot3+0.04\right)=5.69\left(g\right)\)
cho 1,35 gam hh Cu, Mg , Al td với HNO3 dư được 896 ml (ở đktc) hh gồm NO và NO2 có\(\overline{M}\) = 42 . tính tổng kl muối nitrat sinh ra ( khí ở đktc)
Cho 1,35 gam hỗn hợp gồm Cu, Mg, Al tác dụng hết với dung dịch HNO 3 thu được hỗn hợp khí gồm 0,01 moi NO và 0,04 mol NO 2 . Tính khối lượng muối tạo ra trong dung dịch.
Đặt x, y, z lần lượt là số mol Cu, Mg, Al.
Quá trình nhường e :
Cu → Cu 2 + + 2e
x → x → 2x
Mg → Mg 2 + + 2e
y → y → 2y
Al → Al 3 + + 3e
z → z → 3z
Quá trình thu e :
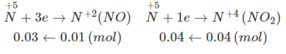
Ta có : 2x + 2y + 3z = 0,03 + 0,04 = 0,07 và 0,07 cũng chính là số mol NO 3 - tạo muối.
Khối lượng muối nitrat là : 1,35 + 62 × 0,07 = 5,69 (gam).
cho 1,35 gam hỗn hợp A gồm Cu, Mg, Al tác dụng với HNO3 dư được 1,12 lit NO và NO2 có khối lượng trung bình là 42,8 . Biết thể tích khí đo ở đktc. Tổng khối lượng muối nitrat sinh ra là bao nhiêu
nNO = a; nNO2 = b.
Ta có: a+b = 0,0530a + 46b = 0,05.42,8 = 2,14
\(\Rightarrow\) a= 0,01; b=0,04
mMuối= mKL + mNO3= 1,35 + 62( 0,01.3+0,04) = 5,69 gam
Ta dễ dàng tính được nNO = 0,01 mol; nNO2 = 0,04 mol
m muối = mKL + 62( 3nNO + nNO2)
= 1,35 + 62( 3. 0,01 + 0,04)
= 5,69 (g)
ta có hệ: nNO+nNO2= 0,05
30nNO+46nNO2= 0,05x42,8
nNO= 0,01 mol
nNO2= 0,04 mol
= > m muối= m kim loại+ m gốc axit=1,35+62x( 0,01x3+0,04)= 5,69 gam
Cho 1,35 gam hỗn hợp gồm Mg, Al, Cu tác dụng hết với HNO3 thu được hỗn hợp khí gồm 0,01 mol NO và 0,04 mol NO2. Cô cạn dung dịch sau phản ứng thu được hỗn hợp muối với khối lượng là:
A. 5,69 gam
B. 5,5 gam
C. 4,98 gam
D. 4,72 gam