Khử hoàn toàn m gam hỗn hợp X gồm FeO và Fe2O3 bằng H2 (dư), thu được 9 gam H2O và 22,4 gam chất rắn. Phần trăm số mol của FeO trong hỗn hợp X là:
A. 66,67.
B. 20,56.
C. 26,67.
D. 40,67.
Cho a gam hỗn hợp X gồm Fe2O3, Fe3O4, Cu vào dung dịch HCl dư thấy có 1 mol axit phản ứng và còn lại 0,256a gam chất rắn không tan. Mặt khác, khử hoàn toàn a gam hỗn hợp X bằng H2 dư, thu được 42 gam chất rắn. Tính phần trăm khối lượng Cu trong hỗn hợp X?
A. 25,6%.
B. 50%.
C. 44,8%.
D. 32%.
một hỗn hợp X gồm Fe2O3 , Fe3O4 và FeO ( ỉ lệ mol FeO và Fe2O3 là 1:1 ) . khử hoàn toàn m gam X bằng khí H2 dư , kết thúc thì nghiệm thấy khối lượng chất rắn giảm 0,96g . viết phương trình hóa học
cacs pthh :
Fe2O3 + 3H2 --t--> 2Fe + 3H2O
FeO+ H2 -t--> Fe+H2O
Fe3O4 +4H2 --t--> 3Fe + 4H2O
Cho a gam hỗn hợp X gồm Fe2O3, Fe3O4 và Cu vào dung dịch HCl dư, thấy có 1 mol axit phản ứng và còn lại 0,256a gam chất rắn không tan. Mặt khác, khử hoàn toàn a gam hỗn hợp X bằng CO dư thu được 42 gam chất rắn. Phần trăm khối lượng của Cu trong hỗn hợp X là
A. 25,6%
B. 32,0%
C. 50,0%
D. 44,8%
Đáp án D
Các phản ứng xảy ra:
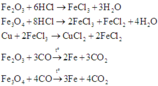
Nhận thấy: nO giảm = n O ( X ) = 1 2 n H C l = 0 , 5
⇒ a = m r ắ n s a u p h ả n ứ n g + m O g i ả m = 50 ( g a m )
Để tính được phần trăm khối lượng của Cu trong hỗn hợp X ta cần biết thêm khối lượng của Cu trong X.
Khi cho X vào dung dịch HCl dư thì chất rắn không tan còn lại sau phản ứng là Cu dư.
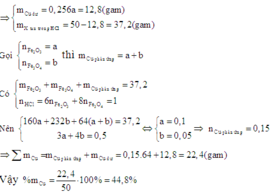
Khử hoàn toàn 8,72gam hỗn hợp X gồm Fe2O3 và FeO bằng CO thì thu được m gam chất rắn Y và khí CO2 . Hấp thụ hoàn toàn khí CO2 bằng nước vôi trong dư thu được 6 gam kết tủa . Gía trị của m là
A. 6,08g
B. 7,76g
C. 9,68g
D. 11,36g
Đáp án : B
Hấp thụ CO2 vào Ca(OH)2 dư => chỉ tạo muối CaCO3
n CaCO3 = 6/100 = 0,06 mol
CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,06 0,06
Ta có : n CO p/ứ = n CO2 = 0,06 mol
Áp dụng ĐLBTKL ta có :
m hX + mCO = mY + m CO2
=> mY = 8,73 + 0,06.28 - 0,06.44 = 7,76g
Tiến hành phản ứng nhiệt nhôm hỗn hợp rắn X gồm Al, FeO và Fe2O3 ( trong điều kiện không có không khí) thu được hỗn hợp chất rắn Y. Chia Y thành hai phần bằng nhau.
+ Cho phần một vào dung dịch NaOH dư, thu được 0,45 mol H2 và còn m gam chất rắn không tan.
+ Cho phần hai vào dung dịch HNO3 dư, thu được 0,7 mol NO ( sản phẩm khử duy nhất).
Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 28,00.
B. 22,40.
C. 11,20.
D. 20,16.
Giải thích:
Các phản ứng xảy ra hoàn toàn. Hỗn hợp rắn Y + NaOH thấy có H2 thoát ra => Al dư sau phản ứng nhiệt nhôm
Vậy hỗn hợp Y gồm Al2O3, Fe và Al dư
Phần 1: Bảo toàn e => nAl dư = 2/3nH2 = 2/3. 0,45 = 0,3 (mol)
Phần 2: Bảo toàn e: 3nFe + 3nAl dư = 3nNO => nFe = (3.0,7 – 3.0,3)/3 = 0,4 (mol)
=> m = mFe = 0,4. 56 = 22,4 (g)
Đáp án B
Cho a gam hỗn hợp A gồm Fe2O3, Fe3O4 và Cu vào dung dịch HCl dư thấy có 1 mol axit phản ứng và còn lại 0,256a gam chất rắn không tan. Mặt khác khử hoàn toàn a gam hỗn hợp A bằng H2 thu được 42g chất rắn. Tính phần trăm khối lượng Cu trong hỗn hợp A.
A.44,8%
B.50%
C.32%
D.25,6%
Đáp án A:
Còn lại 1 phần chất rắn không tan => Cu dư

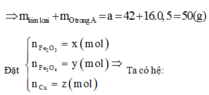
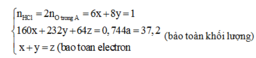
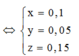
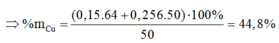
Nung 30,4 gam hỗn hợp X gồm FeO và Fe2O3 trong một bình kín có chứa 22,4 lít khí CO (đktc). Sau phản ứng xảy ra hoàn toàn thu được 36 gam hỗn hợp khí. Biết rằng X bị khử hoàn toàn thành Fe.
a. Xác định thành phần các chất trong hỗn hợp khí.
b. Tính khối lượng Fe thu được và khối lượng 2 oxit sắt ban đầu.
\(Đặt:n_{FeO}=a\left(mol\right),,n_{Fe_2O_3}=b\left(mol\right)\)
\(m_X=72a+160b=30.4\left(g\right)\left(1\right)\)
\(FeO+CÒ\underrightarrow{t^0}Fe+CO_2\)
\(Fe_2O_3+3CO\underrightarrow{t^0}2Fe+3CO_2\)
\(X:COdư,CO_2\)
\(m_X=m_{CO\left(dư\right)}+m_{CO_2}=\left(1-a-3b\right)\cdot28+\left(a+3b\right)\cdot44=36\left(g\right)\)
\(\Leftrightarrow16a+48b=8\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.2,b=0.1\)
\(m_{Fe}=\left(0.2+0.1\cdot2\right)\cdot56=22.4\left(mol\right)\)
\(m_{FeO}=0.2\cdot72=14.4\left(g\right)\)
\(m_{Fe_2O_3}=0.1\cdot160=16\left(g\right)\)
Cho a gam hỗn hợp A gồm Fe2O3, Fe3O4, Cu vào dung dịch HCl dư thấy có 1 mol axit phản ứng và còn lại 0,256a gam chất rắn không tan. Mặt khác, khử hoàn toàn a gam hỗn hợp A bằng H2 dư thu được 42 gam chất rắn. Tính phần trăm về khối lượng Cu trong hỗn hợp A?
A. 50%
B. 25,6%
C. 32%
D. 44,8%
Cho a gam hỗn hợp A gồm Fe2O3, Fe3O4. và Cu vào dung dịch HCl dư thấy có 1 mol axit phản ứng và còn lại 0,256a gam chất rắn không tan. Mặt khác, khử hoàn toàn a gam hỗn hợp A bằng H2 dư thu được 42g chất rắn. Tính phần trăm khối lượng Cu trong hỗn hợp A:
A. 44,8%.
B.50%.
C.32%.
D.25,6%.
Đáp án A
Vì còn lại một phần chất rắn không tan nên Cu dư và trong dung dịch chứa FeCl2 và CuCl2
Có nO(A) = 0,5nHCl = 0,5
a = mkim loại + mO(A) = 42 + 16.0,5 = 50 (gam)
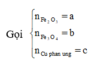
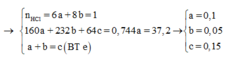
![]()