Cho 16,8 gam Fe vào 200 ml dung dịch CuSO4 1M, sau phản ứng kết thúc thu được m gam chất rắn. Giá trị của m là
A. 12,8.
B. 18,4
C. 16,8.
D. 16.
Cho 16,8 gam Fe vào 200 ml dung dịch CuSO4 1M, sau phản ứng kết thúc thu được m gam chất rắn. Giá trị của m là
A. 12,8
B. 18,4
C. 16,8
C. 16,8
Chọn đáp án B.
n F e = 16 , 8 56 = 0 , 3 m o l
n C u 2 + = 0 , 2 m o l
⇒ Fe phản ứng dư.
Áp dụng tăng giảm khối lượng có:
m = 64 - 56 . 0 , 2 + 16 , 8 = 18 , 4 g a m
Cho m gam bột Fe vào 50 ml dung dịch Cu(NO3)2 1M, sau phản ứng thu được dung dịch X và 4,88 gam chất rắn Y. Cho 4,55 gam bột Zn vào dung dịch X, kết thúc phản ứng thu được 4,1 gam chất rắn Z và dung dịch chứa một muối duy nhất. Giá trị của m là
A. 4,48.
B. 2,80.
C. 5,60.
D. 8,40.

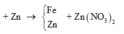
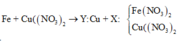
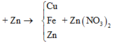
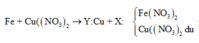
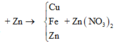
Theo định luật bảo toàn khối lượng, ta có:

![]()
![]()
tìm được m = 4,48 (g)
Đáp án A
Cho 2,24 gam Fe vào 200 ml dung dịch AgNO3 0,5M đến khi kết thúc phản ứng thu được m gam chất rắn. Giá trị của m là
A. 5,40
B. 4,32
C. 8,64
D. 10,80
Cho 2,24 gam Fe vào 200 ml dung dịch AgNO3 0,5M đến khi kết thúc phản ứng thu được m gam chất rắn. Giá trị của m là
A. 5,40.
B. 4,32.
C. 8,64.
D. 10,80.
Cho 2,24 gam Fe vào 200 ml dung dịch AgNO3 0,5M đến khi kết thúc phản ứng thu được m gam chất rắn. Giá trị của m là
A. 5,40.
B. 4,32.
C. 8,64.
D. 10,80.
Cho 200 ml dung dịch AgNO3 2,5a mol/l tác dụng với 200 ml dung dịch Fe(NO3)2 a mol/l. Sau khi phản ứng kết thúc thu được 17,28 gam chất rắn và dung dịch X. Cho dung dịch HCl dư vào dung dịch X thu được m gam kết tủa. Giá trị của m là
A. 34,44
B. 28,7
C. 40,18
D. 43,05
Cho 200 ml dung dịch AgNO3 2,5a mol/l tác dụng với 200 ml dung dịch Fe(NO3)2 a mol/l. Sau khi phản ứng kết thúc thu được 17,28 gam chất rắn và dung dịch X. Cho dung dịch HCl dư vào dung dịch X thu được m gam kết tủa. Giá trị của m là
A. 34,44
B. 28,7
C. 40,18
D. 43,05
Cho m gam bột Fe vào 200 ml dung dịch hỗn hợp A chứa H2SO4 1M, Fe(NO3)3 0,5M và CuSO4 0,25M. Khuấy đều cho đến khi phản ứng kết thúc thoát ra khí NO và 0,75m gam hỗn hợp chất rắn. Giá trị của m là
A. 32
B. 56.
C. 33,6
D. 43,2
Đáp án D
Hỗn hợp kim loại ⇒ không thể có muối Fe3+. Sơ đồ ta có:
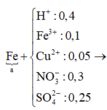
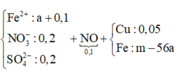
⇒ mCu + mFedư = m – 0,25m = 0,75m.
⇒ 0,05×64 + (m–56a)×56 = 0,25m (*)
+ Áp dụng định luật bảo toàn e cho cả quá trình ta có:
2nFepứ = nFe3+ + 2nCu + 3nNO.
⇒ nFepứ = 0,25 mol ⇒ mFepứ = 56a = 14 gam
+ Thế vào (*) ⇒ m = 43,2 gam
Cho m gam bột Fe vào 200 ml dung dịch hỗn hợp A chứa H2SO4 1M, Fe(NO3)3 0,5M và CuSO4 0,25M. Khuấy đều cho đến khi phản ứng kết thúc thoát ra khí NO và 0,75m gam hỗn hợp chất rắn. Giá trị của m là
A. 32.
B. 56.
C. 33,6.
D. 43,2.
Hỗn hợp kim loại ⇒ không thể có muối Fe3+. Sơ đồ ta có:

⇒ mCu + mFedư = m – 0,25m = 0,75m.
⇒ 0,05×64 + (m–56a)×56 = 0,25m (*)
+ Áp dụng định luật bảo toàn e cho cả quá trình ta có:
2nFepứ = nFe3+ + 2nCu + 3nNO.
⇒ nFepứ = 0,25 mol ⇒ mFepứ = 56a = 14 gam
+ Thế vào (*) ⇒ m = 43,2 gam
Đáp án D