Cho 15,8g KMn O 4 tác dụng hết với dung dịch HCl đậm đặc. Giả sử hiệu suất phản ứng là 100% thì thể tích (đktc) khí Cl 2 thu được là
A. 5,6 lít B. 0,56 lít
C. 2,8 lít D. 0,28 lít
Cho 8,7 gam MnO2 tác dụng với dung dịch axit HCl đậm đặc sinh ra V lít khí Cl2 (đktc). Hiệu suất phản ứng là 85%. V có giá trị là:
A. 2 lít
B. 2,905 lít
C. 1,904 lít
D. 1,82 lít
Cho 8,7 gam MnO2 tác dụng với dung dịch axit HCl đậm đặc sinh ra V lít khí Cl2 (đktc). Hiệu suất phản ứng là 85%. V có giá trị là :
A. 2 lít
B. 2,905 lít
C. 1,904 lít
D. 1,82 lít
Đáp án C
![]()
MnO2 + 4HCl →MnCl2 + 2H2O + Cl2
0,1 →0,1 (mol)
Do H% = 85% => ![]() = 0,085 (mol)
= 0,085 (mol)
V = 0,085.22,4 = 1,904 (lít)
Cho nhôm dư tác dụng với m gam dung dịch axit clohiđric 54.75%, sau phản ứng hoàn toàn thu đc 6.72 lít khí hiđro (đktc).
a, Viết PTHH của phản ứng.
b, Tính khối lượng nhôm đã phản ứng (giả sử hiệu suất phản ứng là 100%)?
c, Nếu hiệu suất phản ứng H = 80% tính khối lượng (m=?) dung dịch axit clohiđric 54.75% đã phản ứng.
Cho: H = 1; S = 32; O = 16; Na = 23; Cl = 35.5; Al = 27.
Mai mk thi rùi, mn giúp mk vs ạ, mk cảm ơn nhiều.
\(a) 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ b) n_{H_2} = \dfrac{6,72}{22,4} = 0,3(mol)\\ n_{Al} = \dfrac{2}{3}n_{H_2} = 0,2(mol)\\ m_{Al} = 0,2.27 = 5,4(gam)\\ c) n_{HCl\ pư} = 2n_{H_2} = 0,6(mol)\\ n_{HCl\ đã\ dùng} = \dfrac{0,6}{80\%} = 0,75(mol)\\ m_{dd\ HCl} = \dfrac{0,75.36,5}{54,75\%} = 50(gam)\)
Cho m gam hỗn hợp X gồm Al và FeO (có tỉ lệ số mol tương ứng là 3 : 2) tác dụng với dung dịch HNO 3 loãng dư thu được 4,928 lít khí NO (đktc, sản phẩm khử duy nhất) và dung dịch A. Nếu đem nung m gam hỗn hợp X đến khi phản ứng nhiệt nhôm kết thúc (giả sử hiệu suất đạt 100%) thu được hỗn hợp Y. Cho hỗn hợp Y tác dụng với dung dịch HCl dư thu được V lít khí H 2 (đktc). Giá trị của V là
A. 6,048
B. 6,272
C. 5,824
D. 6,496
Cho m gam hỗn hợp X gồm Al và FeO (có tỉ lệ số mol tương ứng là 2 : 1) tác dụng với dung dịch HNO 3 loãng dư thu được 15,68 lít khí NO (đktc, sản phẩm khử duy nhất) và dung dịch A. Nếu đem nung m gam hỗn hợp X đến khi phản ứng nhiệt nhôm kết thúc (giả sử hiệu suất đạt 100%) thu được hỗn hợp Y. Cho hỗn hợp Y tác dụng với dung dịch HCl dư thu được V lít khí H 2 (đktc). Giá trị của V là
A. 20,48
B. 20,16
C. 10,8
D. 6,496
Cho 15,8g KMnO4 tác dụng với dung dịch HCl đặc, tính thể tích khí Cl2 thu được ở đktc, biết quá trình thu khí Cl2 hao hụt 10 phần trăm
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,1--------------------------------------------------0,25 mol
n KMnO4=\(\dfrac{15,8}{158}\)=0,1 mol
Hao hụt 10%
=>VCl2=0,25.22,4.90%=5,04l
Đun nóng 22,12 gam KMnO4 thu được 21,26 gam hỗn hợp rắn. Cho hốn hợp rắn tác dụng với dung dịch HCl đặc thì lượng khí clo thoát ra là (hiệu suất phản ứng 100%)
A. 0,17 mol.
B. 0,49 mol.
C. 0,26 mol.
D. 0,29 mol.
Sau khi thực hiện phản ứng nhiệt nhôm vói Fe3O4 thu được chất rắn A và nhận thấy khối lượng nhôm giảm 0,81 gam. Cho A tác dụng với dung dịch NaOH dư thu được 0,672 lít khí (đktc), (giả sử phản ứng đều xảy ra với hiệu suất 100%). Khối lượng A là:
A. l,08g
B. l,62g
C. 2,1g
D. 3,96g
Đáp án D
8 Al + 3 Fe 3 O 4 → t o 4 Al 2 O 3 + 9 Fe
Khối lượng nhôm giảm chính là khối lượng nhôm đã tham gia phản ứng.
⇒ n Al phan ung = 0 , 81 27 = 0 , 03 ⇒ n Fe 3 O 4 = 3 8 n Al phan ung = 0 , 01125
Vì A tác dụng với dung dịch NaOH có H2 nên A có chứa Al dư và
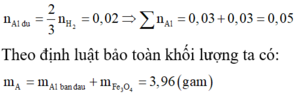
Bài 4: Cho 0,65 g kẽm tác dụng với dung dịch HCl 2M, sau phản ứng thu được khí hidro (đktc)
a. Tính thể tích khí hidro tạo thành sau phản ứng (đktc)
b. Tính khối lượng muối thu được sau phản ứng.
c. Tính thể tích dung dịch HCl 2M cần dùng.
\(a,n_{Zn}=\dfrac{0,65}{65}=0,01\left(mol\right)\)
PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,01--->0,02---->0,01---->0,01
\(V_{H_2}=0,01.22,4=0,224\left(l\right)\\ b,m_{ZnCl_2}=0,01.136=1,36\left(g\right)\\ V_{ddHCl}=\dfrac{0,02}{2}=0,01\left(l\right)\)