Phản ứng nào sau đây được dùng để điều chế clo trong phòng thí nghiệm
A. 2NaCl → 2Na + Cl 2
B. 2NaCl + 2 H 2 O → H 2 + 2NaOH + Cl 2
C. Mn O 2 + 4HCl → Mn Cl 2 + Cl 2 + H 2 O
D. F 2 + 2NaCl → 2NaF + Cl 2
Phản ứng nào sau đây được dùng để điều chế clo trong phòng thí nghiệm ?
A. 2NaCl → 2Na + Cl2
B. 2NaCl + 2H2O → H2 + 2NaOH + Cl2
C. MnO2 + 4HClđặc → t ° MnCl2 + Cl2 + 2H2O
D. F2 + 2NaCl → 2NaF + Cl2
Phản ứng nào sau đây được dùng để điều chế H2S trong phòng thí nghiệm
A. SO2 làm đỏ quỳ tím ẩm
B. FeS + dung dịch HCl loãng
C. FeS + dung dịch H2SO4 đặc, t o .
D. SO2 làm mất màu cánh hoa hồng
Phản ứng nào sau đây dùng để điều chế N2 trong phòng thí nghiệm?
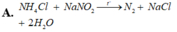
![]()
![]()
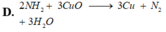
Phản ứng nào sau đây dùng để điều chế NH3 trong phòng thí nghiệm?
A. 2NH4Cl + Ca(OH)2 → t o CaCl2 + 2NH3 + 2H2O
B. N2 + 3H2 ⇄ t o , p , xt 2NH3
C. NH4HCO3 → t o NH3 + CO2 + H2O
D. Na3N + 3H2O → 3NaOH + NH3.
Phản ứng nào sau đây dùng để điều chế axit trong phòng thí nghiệm:
A. H2+ Cl2 → 2HCl.
B. NaCl(rắn)+H2SO4(đặc) → Na2SO4 +HCl↑.
C. FeS + HCl → FeCl2 + H2S↑.
D. Cl2 + H2O → HCl + HClO.
Chọn đáp án B
Trong phòng thí nghiệm ta chỉ cần lượng nhỏ nên cần phải dùng phương pháp điều chế nhanh và dễ dàng.Còn trong công nghiệp thì yêu cầu là ít tốn kém và thu được lượng lớn.
Chú ý : Theo mình nghĩ câu này cả B và C đều hợp lý.
Phản ứng nào sau đây dùng để điều chế HNO3 trong phòng thí nghiệm?
A. 4 NO 2 + O 2 + 2 H 2 O → 4 HNO 3
B. 3 NO 2 + 2 H 2 O → 2 HNO 3 + NO
C. NaNO 3 + H 2 SO 4 → t O NaHSO 4 + HNO 3
D. 2 Cu NO 3 2 + 2 H 2 O → đpdd 2 CuO + O 2 + 4 HNO 3
Đáp án C
Trong phòng thí nghiệm, HNO3 được điều chế bằng cách cho natri nitrat hoặc kali nitrat tác dụng với axit H2SO4 đặc, nóng
Lưu ý: hơi axit HNO 3 thoát ra được dẫn vào bình, được làm lạnh và ngưng tụ.
Phản ứng nào sau đây không được dùng để điều chế hiđro trong phòng thí nghiệm? A. Zn + 2HCl → ZnCl2 + H2.
B. Fe + H2SO4 → FeSO4 + H2.
C. 2Al + 3H2SO4 → Al2(SO4)3 + 3H2.
D. 2H2O 2H2 + O2.
Phản ứng tự oxi hóa, tự khử (tự oxi hóa - khử) là phản ứng có sự tăng và giảm đồng thời số oxi hóa của các nguyên tử của cùng một nguyên tố. Phản ứng nào sau đây thuộc loại trên
A. Cl 2 + 2Na → 2NaCl
B. Cl 2 + H 2 → 2HCl
C. Cl 2 + H 2 O → HCl + HClO
D. Cl 2 + 2NaBr → 2NaCl + Br 2
Trong công nghiệp HCl có thể điều chế bằng phương pháp sunfat theo phản ứng:
2NaCl (tinh thể) + H2SO4 (đặc) → t o 2HCl + Na2SO4.
Tại sao phương pháp này không được dùng để điều chế HBr và HI
A. Do tính axit của H2SO4 yếu hơn HBr và HI
B. Do NaBr và NaI đắt tiền, khó kiếm
C. Do HBr và HI sinh ra là chất độc
D. Do có phản ứng giữa HBr, HI với H2SO4 (đặc, nóng)
Do tính khử HBr, HI lớn, nó sẽ tác dụng với H2SO4 đặc nóng sinh ra Br2, I2 nên không thể điều chế HBr và HI theo phương pháp sunfat.