Để nhận biết hai bình chứa khí không màu CO2 và SO2, cách làm nào sau đây không đúng?
A. Cho mỗi khí vào nước Br2
B. Cho từ từ đến dư mỗi khí vào nước vôi trong
C. Cho mỗi khí vào dung dịch H2S
D. Cho mỗi khí vào dung dịch KMnO4
Viết phương trình phản ứng xảy ra khi cho từ từ mỗi khí CO2, SO2 đến dư vào bình nước vôi trong. Tả ngắn gọn hiện tượng quan sát được, từ đó cho biết có thể dùng nước vôi trong phân biệt 2 khí đó với nhau không
CO2+Ca(OH)2->CaCO3+H2O
SO2+Ca(OH)2->CaSO3+H2O
=> có kết tủa trắng xuất hiện
CaCO3+CO2+H2O->Ca(HCO3)2
CaSO3+SO2+H2O->Ca(HSO3)2
=>Sau đó kết tủa tan dần
PTHH:
SO2 + Cả(OH)2 -> CaSO3 + H2O
CO2 + Cả(OH)2 -> CaCO3 + H2O
Hiện tượng: SO2 và CO2 bị Cả(OH)2 hấp thụ tạo ra kết tủa trắng -> Không thể phân biệt 2 chất này bằng Cả(OH)2
Tiến hành các thí nghiệm sau:
(a) Sục khí CO2 dư vào dung dịch NaOH
(b) Cho dung dịch NaOH dư vào dung dịch Ca(HCO3)2.
(c) Cho dung dịch Ba(HCO3)2 dư vào dung dịch H2SO4.
(d) Cho Mg vào dung dịch CuSO4 dư.
(e) Cho Na đến dư vào dung dịch CH3COOH.
(f) Cho 2 ml benzen vào ống nghiệm có chứa 2 ml dung dịch nước Br2, lắc mạnh, sau đó để yên.
Viết phương trình hóa học (nếu có) và xác định các chất có trong dung dịch sau mỗi thí nghiệm. Cho rằng các phản ứng xảy ra hoàn toàn, các chất khí tan trong nước không đáng kể.
(a) CO2 + NaOH → NaHCO3
Dung dịch sau pứ chỉ có NaHCO3
(b) 2NaOH + Ca(HCO3)2 → Na2CO3 + CaCO3 + H2O
Dung dịch sau pứ: (Na2CO3; NaOH dư)
(c) Ba(HCO3)2 + H2SO4 → BaSO4 + 2CO2 + 2H2O
Dung dịch sau pứ: Ba(HCO3)2 dư
(d) Mg + CuSO4 → MgSO4 + Cu
Dung dịch sau pứ: (MgSO4; CuSO4 dư)
(e) Na + H2O → NaOH + ½ H2
NaOH + CH3COOH → CH3COONa + H2O
Dung dịch sau pứ: (NaOH dư; CH3COONa)
(f) Dung dịch sau pứ: (C6H6; Br2/H2O)
Cho các thí nghiệm sau:
(a) Sục khí CO2 đến dư vào dung dịch natri aluminat.
(b) Nhúng thanh sắt vào dung dịch H2SO4 loãng, nguội.
(c) Sục khí SO2 đến dư vào nước brom.
(d) Cho một mẩu Li vào bình kín chứa khí N2 ở nhiệt độ thường.
(e) Dẫn khí H2S đến dư qua dung dịch CuSO4.
(g) Rắc bột lưu huỳnh lên thuỷ ngân bị rơi vãi.
Số thí nghiệm có xảy ra phản ứng oxi hoá – khử là
A. 3.
B. 5.
C. 4.
D. 6.
Cho các thí nghiệm sau:
(a) Sục khí CO2 đến dư vào dung dịch natri aluminat.
(b) Nhúng thanh sắt vào dung dịch H2SO4 loãng, nguội.
(c) Sục khí SO2 đến dư vào nước brom.
(d) Cho một mẩu Li vào bình kín chứa khí N2 ở nhiệt độ thường.
(e) Dẫn khí H2S đến dư qua dung dịch CuSO4.
(g) Rắc bột lưu huỳnh lên thuỷ ngân bị rơi vãi.
Số thí nghiệm có xảy ra phản ứng oxi hoá – khử là
A. 3.
B. 5.
C. 4.
D. 6.
Giải thích:
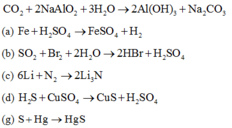
Các phản ứng oxi hóa – khử: (b), (c), (d), (g).
Đáp án C.
Cho các thí nghiệm sau:
(a) Sục khí CO2 đến dư vào dung dịch natri aluminat.
(b) Nhúng thanh sắt vào dung dịch H2SO4 loãng, nguội.
(c) Sục khí SO2 đến dư vào nước brom.
(d) Cho một mẩu Li vào bình kín chứa khí N2 ở nhiệt độ thường.
(e) Dẫn khí H2S đến dư qua dung dịch CuSO4.
(g) Rắc bột lưu huỳnh lên thuỷ ngân bị rơi vãi.
Số thí nghiệm có xảy ra phản ứng oxi hoá – khử là
A. 3
B. 5
C. 4
D. 6
Chọn đáp án C.
![]()
![]()
![]()
![]()
![]()
![]()
Các phản ứng oxi hóa – khử: (b), (c), (d), (g)
Sau khi làm thí nghiệm,có những khí thải độc hai riêng biệt sau: H2S,HCl,SO2.Có thể sục mỗi khí trên vào nước vôi trong dư để khử độc không? Hãy giải thích và viết PTHH.
1 bài hóa rất thực tế, lop7vnen hoàn toàn đủ kiến thức để làm
em khẳng định dùng nước vôi khử độc dc vì tạo ra chất mới hoặc kết tủa hoặc k độc
pt hh: H2S + Ca(OH)2 = CaS + 2H2O
2HCl + Ca(OH)2 = CaCl2 + 2H2O
SO2 + Ca(OH)2 = CaSO3 + H2O
Cho các phát biểu sau:
(1) Trong điều kiện thường, dung dịch H2S tiếp xúc với O2 trở nên vẩn đục màu vàng.
(2) Khí H2S cháy trong không khí với ngọn lửa màu vàng nhạt.
(3) Trong công nghiệp, người ta sản xuất khí H2S bằng cách cho axit HCl tác dụng với FeS.
(4) Khí sunfuro là chất khí không màu, không mùi, nặng hơn không khí.
(5) Lưu huỳnh đioxit là khí độc, tan nhiều trong nước.
(6) Dẫn khí SO2 vào dung dịch H2S có hiện tượng vẩn đục màu xanh.
(7) Dẫn khí SO2 vào dung dịch brom có hiện tượng mất màu dung dịch brom.
Số phát biểu đúng là
A. 3.
B. 7.
C. 6.
D. 4.
Đáp án A
Các trường hợp thoả mãn: 1 – 5 – 7
Cho các phát biểu sau:
(1) Trong điều kiện thường, dung dịch H2S tiếp xúc với O2 trở nên vẩn đục màu vàng.
(2) Khí H2S cháy trong không khí với ngọn lửa màu vàng nhạt.
(3) Trong công nghiệp, người ta sản xuất khí H2S bằng cách cho axit HCl tác dụng với FeS.
(4) Khí sunfuro là chất khí không màu, không mùi, nặng hơn không khí.
(5) Lưu huỳnh đioxit là khí độc, tan nhiều trong nước.
(6) Dẫn khí SO2 vào dung dịch H2S có hiện tượng vẩn đục màu xanh.
(7) Dẫn khí SO2 vào dung dịch brom có hiện tượng mất màu dung dịch brom.
Số phát biểu đúng là
A. 3.
B. 7.
C. 6.
D. 4.
Các trường hợp thoả mãn: 1 – 5 – 7
ĐÁP ÁN A
Cho các phát biểu sau:
(1) Trong điều kiện thường, dung dịch H2S tiếp xúc với O2 trở nên vẩn đục màu vàng
(2) Khí H2S cháy trong không khí với ngọn lửa màu vàng nhạt
(3) Trong công nghiệp, người ta sản xuất khí H2S bằng cách cho axit HCl tác dụng với FeS
(4) Khí sunfuro là chất khí không màu, không mùi, nặng hơn không khí
(5) Lưu huỳnh đioxit là khí độc, tan nhiều trong nước
(6) Dẫn khí SO2 vào dung dịch H2S có hiện tượng vẩn đục màu xanh
(7) Dẫn khí SO2 vào dung dịch brom có hiện tượng mất màu dung dịch brom
Số phát biểu đúng là:
A. 3.
B. 7.
C. 6.
D. 4.
(1) Trong điều kiện thường, dung dịch H2S tiếp xúc với O2 trở nên vẩn đục màu vàng
(5) Lưu huỳnh đioxit là khí độc, tan nhiều trong nước
(7) Dẫn khí SO2 vào dung dịch brom có hiện tượng mất màu dung dịch brom
ĐÁP ÁN A