Có 3 mẫu hợp kim Fe – Al, K – Na, Cu – Mg. Chỉ dùng NaOH có thể nhận biết được bao nhiêu mẫu hợp kim
A. Không nhận biết được mẫu nào
B. 1
C. 2
D. 3
Có 5 mẫu kim loại là Mg, Al, Ba, Fe, Ag. Nếu chỉ dùng thêm dung dịch H2SO4 thì có thể nhận biết được những mẫu kim loại nào ?
A. Mg, Ba, Ag.
B. Mg, Ba, Al.
C. Mg, Ba, Al, Fe.
D. Cả 5 mẫu kim loại.
Đáp án D.
- Cho dd H2SO4 loãng lần vào các mẫu thử:
+ Mẫu có khí thoát ra có có kết tủa trắng là Ba
Ba + H2SO4 → BaSO4↓ + H2↑
+ Mẫu có khí thoát ra và dung dịch muối thu được có màu trắng xanh là Fe
Fe + H2SO4 → FeSO4 + H2↑
+ Mẫu không tan là Ag
+ 2 mẫu còn lại cùng có khí không màu thoát ra là Al và Mg
Mg + H2SO4 → MgSO4 + H2↑
2Al + 3H2SO4 → Al2(SO4)3 + 3H2↑
- Lấy một lượng dư kim loại Ba (đã nhận biết được ở trên) nhỏ vài giọt dd H2SO4 loãng đến sẽ xảy ra phản ứng
Ba + H2SO4 → BaSO4↓ + H2↑
Ba + 2H2O → Ba(OH)2 + H2↑
Lọc bỏ kết tủa BaSO4↓ ta thu được dd Ba(OH)2
- Cho Ba(OH)2 lần lượt vào 2 mẫu thử chưa nhận biết được là Mg và Al
+ Kim loại nào thấy khí thoát ra là Al
2Al + 2H2O + Ba(OH)2 → Ba(AlO2)2 + 2H2↑
+ Kim loại nào không có hiện tượng gì là Mg
⇒ Vậy sẽ nhận ra được cả 5 kim loại
Có 3 mẫu hợp kim Fe – Al, K – Na, Cu – Mg. Có thể dùng dung dịch nào dưới đây có thể phân biệt 3 mẫu hợp kim trên ?
A. HCl
B. NaOH
C. H 2 S O 4 loãng
D. M g C l 2
Có 3 mẫu hợp kim Fe – Al, K – Na, Cu – Mg. Có thể dùng dung dịch nào dưới đây để phân biệt 3 mẫu hợp kim trên
A. HCl
B. NaOH
C. H2SO4 loãng
D. MgCl2
Có 4 mẫu bột kim loại là Na, Al , Ca, Fe. Chỉ dùng nước làm thuốc thử, thì số kim loại có thể phân biệt được là bao nhiêu?
A. 1
B. 2
C. 3
D. 4
Đáp án D.
Trích mẫu thử rồi đổ nước vào từng mẫu thử
Kim loại nào phản ứng mạnh với nước, tạo dung dịch trong suốt là Na
Kim loại nào phản ứng mạnh với nước, tạo dung dịch trắng đục là Ca vì Ca(OH)2 ít tan, kết tủa trắng
Cho dd NaOH đến dư vào 2 mẫu thử còn lại, mẫu thử nào tác dụng tạo kết tủa rồi kết tủa tan, có giải phóng khí là Al.
Chất còn lại không phản ứng là Fe
PTHH:
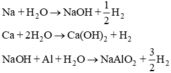
Có 4 mẫu bột kim loại là Na, Al , Ca, Fe. Chỉ dùng nước làm thuốc thử, thì số kim loại có thể phân biệt được là bao nhiêu?
A. 1. B. 2.
C. 3. D. 4.
| Na | Al | Ca | Fe | |||
| H2O | dd trong suốt Có khí H2 bay ra | Không hiện tượng | dd vẩn đục Ca(OH)2 ít tan Có khí H2 bay ra | Không hiện tượng | |||
| dd NaOH (Sản phẩm kim loại Na+ H2O) | \\\\ | Kim loại tan và có khí thoát ra | \\\\ | Không hiện tượng |
PTHH: 2Na + 2H2O→ 2NaOH + H2↑
Ca + H2O → Ca(OH)2 + H2
Al + NaOH + H2O → NaAlO2 + 3/2H2↑
Chú ý:\\\\: đã nhận biết
Chọn D
có 5 mẫu kim loại Ba,Mg,Fe,Al,Ag nếu chỉ dùng dd H2SO4 loãng có thể nhận biết được những kim loại nào.Viết PTHH minh họa.
- Trích mẫu thử, đánh STT
- Hòa tan các kim loại vào nước nếu thấy:
+ Kim loại không tan: Ag
+ Kim loại tan, tạo dd không màu đồng thời có khí không màu, không mùi thoát
ra: Mg, Al, Fe
`Mg + H_2SO_4 -> MgSO_4 + H_2`
`2Al + 3H_2SO_4 -> Al_2(SO_4)_3 + 3H_2`
`Fe + H_2SO_4 -> FeSO_4 + H_2`
+ Kim loại tan, có khí không màu, không mùi bay lên đồng thời xuất hiện kết tủa màu trắng: Ba
\(Ba+H_2SO_4\rightarrow BaSO_4\downarrow+H_2\)
- Cho Ba tiếp vào dd H2SO4 loãng cho tới khi dư, lọc bỏ phần kết tủa thu được dd Ba(OH)2
- Cho dd Ba(OH)2 vào dd thu được của các kim loại còn lại, nếu thấy:
+ Có kết tủa trắng xuất hiện: dd MgSO4 -> kim loại ban đầu là Mg
\(MgSO_4+Ba\left(OH\right)_2\rightarrow BaSO_4\downarrow+Mg\left(OH\right)_2\downarrow\)
+ Có kết tủa trắng xuất hiện, sau đó tan ra một phần: dd Al2(SO4)3 -> kim loại ban đầu là Al
\(Al_2\left(SO_4\right)_3+3Ba\left(OH\right)_2\rightarrow2Al\left(OH\right)_3\downarrow+3BaSO_4\downarrow\\ Ba\left(OH\right)_2+2Al\left(OH\right)_3\rightarrow Ba\left(AlO_2\right)_2+4H_2O\)
+ Có kết tủa trắng xuất hiện, sau đó một phần hóa nâu đỏ ngoài không khí: dd FeSO4 -> kim loại ban đầu là Fe
\(FeSO_4+Ba\left(OH\right)_2\rightarrow Fe\left(OH\right)_2\downarrow+BaSO_4\downarrow\\ 4Fe\left(OH\right)_2+O_2+2H_2O\rightarrow4Fe\left(OH\right)_3\downarrow\)
- Dán nhãn
Nhận biết được Ba vì có kết tủa, khí thoát ra:
Ba + H2SO4 -> BaSO4 + H2
Nhận biết được Ag vì không có hiện tượng.
Các kim loại còn lại chưa nhận biết được vì đều tan tạo dung dịch trong suốt không màu
Cho các hỗn hợp kim loại sau: (1) Mg – Fe, (2) Mg – K, (3) Mg – Ag, (4) Ca – Be. Chỉ
dùng H2O có thể nhận biết được bao nhiêu hỗn hợp kim loại trên ?.
A. 1
B. 2
C. 3
D. 4
Có 4 mẫu kim loại là Na, Ca, Al, Fe. Chỉ dùng thêm nước làm thuốc thử có thể nhận biết được tối đa:
A. 1 chất
B. 2 chất
C. 3 chất
D. 4 chất
A/ Chỉ dùng một thuốc thử hãy phân biệt các dung dịch sau:
NaOH, CuSO4, Fe(NO3)3, Fe(NO3)2, NH4Cl, AlCl3
B/ Có 5 mẫu kim loại :Ba, Mg, Fe, Ag, Al chỉ dùng dung dịch H2SO4 loãng (không được dùng chất khác ). Hãy nhận biết ra 5 kim loại trên.
giúp mình với!!!!!!!
a. Cho dung dịch NaOH lần lượt vào các mẫu thử :
- Kết tủa xanh lam : CuSO4
- Kết tủa nâu đỏ : Fe(NO3)3
- Kết tủa trắng xanh , hóa nâu đỏ trong không khí : Fe(NO3)2
- Sủi bọt khí mùi khai : NH4Cl
- Kết tủa keo trắng , tan dần trong NaOH dư : AlCl3
- Không HT : NaOH
\(2NaOH+CuSO_4\rightarrow Na_2SO_4+Cu\left(OH\right)_2\)
\(3NaOH+Fe\left(NO_3\right)_3\rightarrow3NaNO_3+Fe\left(OH\right)_3\)
\(2NaOH+Fe\left(NO_3\right)_2\rightarrow2NaNO_3+Fe\left(OH\right)_2\)
\(NaOH+NH_4Cl\rightarrow NaCl+NH_3+H_2O\)
\(3NaOH+AlCl_3\rightarrow3NaCl+Al\left(OH\right)_3\)
\(NaOH+Al\left(OH\right)_3\rightarrow NaAlO_2+2H_2O\)
a, - Trích từng dung dịch làm mẫu thử và đánh số thứ tự .
- Chọn thuốc thử là dung dịch NaOH dư .
- Nhỏ vào từng mẫu thử .
+, Mẫu thử không hiện tượng là NaOH
+, Mẫu thử tạo kết tủa xanh lơ là CuSO4
PTHH : CuSO4 + 2NaOH -> Cu(OH)2 + Na2SO4
+, Mẫu thử tạo kết tủa nâu đỏ là Fe(NO3)3
PTHH : Fe(NO3)3 + 3NaOH -> 3NaNO3 + Fe(OH)3
+, Mẫu thử tạo kết tủa trắng xanh rồi hóa nâu đỏ trong không khí là Fe(NO3)2
Fe(NO3)2 + 2NaOH -> Fe(OH)2 + 2NaNO3
2Fe(OH)2 + O2 + H2O -> 2Fe(OH)3
+, Mẫu thử tạo khí mùi khai là NH4Cl
PTHH : NH4Cl + NaOH -> NaCl + NH3 + H2O
+, Mẫu thử tạo kết tủa keo rồi tan là AlCl3
3NaOH + AlCl3 -> Al(OH)3 + 3NaCl
Al(OH)3 + NaOH -> NaAlO2 + H2O
b.
Cho dung dịch H2SO4 loãng lần lượt vào từng chất :
- Tan , sủi bọt , tạo kết tủa trắng : Ba
- Tan , sủi bọt : Mg , Fe , Al
- Không tan : Ag
Cho Ba phản ứng đến dư với dung dịch H2SO4 => Lọc kết tủa , thu được dung dịch Ba(OH)2
Cho dung dịch Ba(OH)2 vào các dung dịch còn lại :
- Kết tủa trắng : chất ban đầu là : Mg
- Kết tủa trắng xanh , hóa nâu đỏ trong không khí : Fe
- Kết tủa keo trắng , tan dần : Al
PTHH em tự viết nhé !