Cho từ từ dung dịch HCl 1M vào dung dịch chứa x mol NaOH và y mol NaAlO2. Số mol Al(OH)3 (n mol) tạo thành phụ thuộc vào thể tích dung dịch HCl (V ml) được biểu diễn bằng đồ thị bên. Tỷ số của x/y có giá trị là
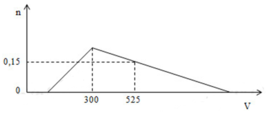
A. 1/3
B. 1/4
C. 2/3
D. 2/5
Cho từ từ dung dịch HCl 1M vào dung dịch chứa x mol NaOH và y mol NaAlO2. Số mol Al(OH)3 (n mol) tạo thành phụ thuộc vào thể tích dung dịch HCl (V ml) được biểu diễn bằng đồ thị bên. Tỷ số của x/y có giá trị là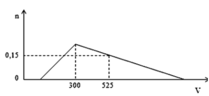
A. 1/3
B. 1/4
C. 2/3
D. 2/5
Đáp án A
+ Tại V = 300 ml:
nHCl = nNaOH + nNaAlO2 => 0,3 = x + y (1)
+ Tại V = 525 ml:
nHCl = nNaOH + nNaAlO2 + 3(nNaAlO2 – n↓) => 0,525 = x + y + 3(y-0,15) (2)
Giải hệ (1) và (2) => x = 0,075; y = 0,225
=> x:y = 0,075:0,225 = 1/3
Cho từ từ dung dịch HCl 1M vào dung dịch chứa x mol NaOH và y mol NaAlO2. Số mol Al(OH)3 (n mol) tạo thành phụ thuộc vào thể tích dung dịch HCl (V ml) được biểu diễn bằng đồ thị bên. Tỷ số của x/y có giá trị là
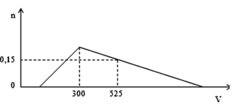
A. 1/3
B. 1/4
C. 2/3
D. 2/5
+ Tại V = 300 ml:
nHCl = nNaOH + nNaAlO2 => 0,3 = x + y (1)
+ Tại V = 525 ml:
nHCl = nNaOH + nNaAlO2 + 3(nNaAlO2 – n↓) => 0,525 = x + y + 3(y-0,15) (2)
Giải hệ (1) và (2) => x = 0,075; y = 0,225
=> x:y = 0,075:0,225 = 1/3
Đáp án A
Cho từ từ dung dịch HCl 1M vào dung dịch chứa x mol NaOH và y mol NaAlO2. Số mol Al(OH)3 (n mol) tạo thành phụ thuộc vào thể tích dung dịch HCl (V ml) được biểu diễn bằng đồ thị bên.
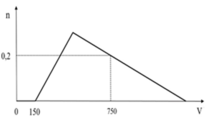
Giá trị của x và y lần lượt là
A. 0,30 và 0,30.
B. 0,30 và 0,35.
C. 0,15 và 0,35.
D. 0,15 và 0,30.
Giải thích:
H+ + OH- → H2O
0,15 ← 0,15
H+ + AlO2 -+ H2O → Al(OH)3↓
y← y → y
3H+ + Al(OH)3↓ → Al3+ + 3H2O
3(y – 0,2) ← (y – 0,2)
Bảo toàn H+ => ∑ nH+ = 0,15 + y + 3(y – 0,2) = 0,75
=> y = 0,3 mol
nNaOH = nH+ = 0,15 (mol)
Vậy x = 0,15 mol ; y = 0,3 mol
Đáp án D
Cho từ từ dung dịch HCl 1M vào dung dịch chứa x mol NaOH và y mol NaAlO2. Số mol Al(OH)3 (n mol) tạo thành phụ thuộc vào thể tích dung dịch HCl (V ml) được biểu diễn bằng đồ thị bên
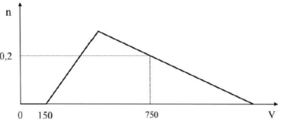
Giá trị của x và y lần lượt là
A. 0,30 và 0,30
B. 0,30 và 0,35.
C. 0,15 và 0,35
D. 0,15 và 0,30.
Đáp án D
Các phản ứng trong quá trình xảy ra như sau:
• HCl + NaOH → NaCl + H2O 1 || • HCl + NaAlO2 + H2O → NaCl + Al(OH)3↓ 2
• 3HCl + Al(OH)3 → AlCl3 + 3H2O 3. (xảy ra lần lượt như đồ thị biểu diễn).
Tại điểm V = 150 mL ⇔
n
H
C
l
= 0,15 mol là kết thúc phản ứng 1 ⇒ x =
n
N
a
O
H
= 0,15 mol.
Tại điểm V = 750 mL ⇔
n
H
C
l
= 0,75 mol;
n
A
l
(
O
H
)
3
↓ = 0,2 mol là thời điểm
phản ứng 2 đã kết thúc, đang diễn ra phản ứng 3 (hòa tan một phần tủa).
Tại điểm sản phẩm gồm (x + y) mol NaCl + 0,2 mol Al(OH)3 + (y – 0,2) mol AlCl3.
⇒ Bảo toàn nguyên tố Cl có: (x + y) + 3 × (y – 0,2) = 0,75 mol ⇒ y = 0,3 mol.
Cho từ từ dung dịch HCl 1M vào dung dịch chứa x mol NaOH và y mol NaAlO2. Số mol Al(OH)3 (n mol) tạo thành phụ thuộc vào thể tích dung dịch HCl (V ml) được biểu diễn bằng đồ thị bên.
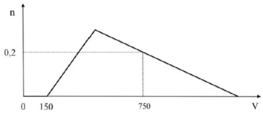
Giá trị của x và y lần lượt là
A. 0,30 và 0,30
B. 0,30 và 0,35
C. 0,15 và 0,35
D. 0,15 và 0,30.
Cho từ từ dung dịch HCl 1M vào dung dịch chứa X mol NaOH và y mol NaAlO2. Số mol Al(OH)3 (n mol) tạo thành phụ thuộc vào thể tích dung dịch HCl (V ml) được biểu diễn bằng đồ thị dưới đây
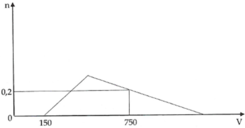
Giá trị của x và y lần lượt là
A. 0,30 và 0,30
B. 0,30 và 0,35
C. 0,15 và 0,35
D. 0,15 và 0,30
Cho từ từ dung dịch HCl 1M vào dung dịch chứa x mol NaOH và y mol NaAlO2. Số mol Al(OH)3 ( n mol) tạo thành phụ thuộc vào thể tích dung dịch HCl (V ml) được biểu diễn bằng đồ thị dưới đây:
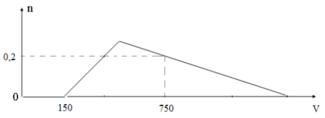
Giá trị của x và y lần lượt là:
A. 0,15 và 0,30
B. 0,30 và 0,35.
C. 0,15 và 0,35
D. 0,30 và 0,30
Chọn A
Vì: Tại V = 150ml thì bắt đầu xuất hiện kết tủa => Đây là giá trị H+ dùng để trung hòa hết NaOH
=> nNaOH = nHCl = 0,15 (mol)
Tại V= 750 ml ta thấy đồ thị lên cao rồ lại xuống => tạo kết tủa đạt cực đại sau đó bị hòa tan 1 phần
AlO2- + H+ + H2O → Al(OH)3
Al(OH)3 + H+ → Al3+ + 2H2O
Áp dụng công thức nhanh ta có:
nH+ = 4nAlO2- - 3nAl(OH)3 + nOH-
=> 0,75 = 4y – 3.0,2 + 0,15
=> y = 0,3
Vậy x = 0,15 và y = 0,3
Cho từ từ dung dịch HCl 1M vào dung dịch chứa x mol NaOH và y mol NaAlO2. Số mol Al(OH)3 ( n mol) tạo thành phụ thuộc vào thể tích dung dịch HCl (V ml) được biểu diễn bằng đồ thị dưới đây
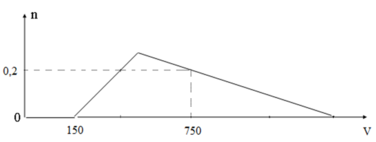
Giá trị của x và y lần lượt là
A. 0,15 và 0,30.
B. 0,30 và 0,35.
C. 0,15 và 0,35.
D. 0,30 và 0,30.
Giải thích:
Tại V = 150ml thì bắt đầu xuất hiện kết tủa => Đây là giá trị H+ dùng để trung hòa hết NaOH
=> nNaOH = nHCl = 0,15 (mol)
Tại V= 750 ml ta thấy đồ thị lên cao rồ lại xuống => tạo kết tủa đạt cực đại sau đó bị hòa tan 1 phần
AlO2- + H+ + H2O → Al(OH)3
Al(OH)3 + H+ → Al3+ + 2H2O
Áp dụng công thức nhanh ta có:
nH+ = 4nAlO2- - 3nAl(OH)3 + nOH-
=> 0,75 = 4y – 3.0,2 + 0,15
=> y = 0,3
Vậy x = 0,15 và y = 0,3
Đáp án A
Cho từ từ dung dịch HCl 1M vào dung dịch A chứa NaOH và NaAlO2. Số mol Al(OH)3 (x mol) tạo thành phụ thuộc vào thể tích dung dịch HC1 (V ml) được biểu diễn bằng đồ thị dưới đây
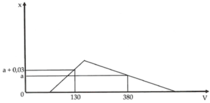
Tổng số mol các chất tan trong A là
A. 0,085
B. 0,075
C. 0,17
D. 0,15