Nguyên tử M có tổng số electron ở phân lớp p là 7 và số nơtron nhiều hơn số proton là 1 hạt. Số khối của nguyên tử M là
A. 25
B. 22
C. 27
D. 28
Cho hợp chất X có công thức phân tử là MxRy trong đó M chiếm 52,94% về khối lượng. Biết x + y = 5. Trong nguyên tử M số nơtron nhiều hơn số proton là 1. Trong nguyên tử R có số nơtron bằng số proton. Tổng số hạt proton; electron và nơtron trong X là 152. Tổng số hạt proton có trong X là:
A. 46.
B. 50
C. 52
D. 60
M chiếm 52,94% về khối lượng:
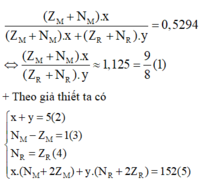
Quan sát – phân tích: Để tìm câu trả lời cho bài toán ta chỉ cần xác định được 4 ẩn x;y; Z M ; Z R
Vì vậy ta sẽ tìm cách khử các ẩn không cần thiết bằng cách thế phương trình (3) và (4) lầ lượt vào phương trình (1) và (5):
Thế (3) và (4) vào phương trình (1) ta được:
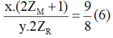
Thế (3) và (4) vào phương trình (5) ta được:
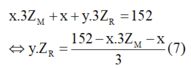
Quan sát – phân tích: Ba phương trình (2); (6); (7) với 4 ẩn ta nghĩ ngay đến biện luận để tìm nghiệm.
Thế (7) vào (6) ta được
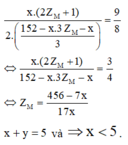
Mặt khác x nguyên
x nhận các giá trị 1, 2, 3, 4
Ta có bảng sau:
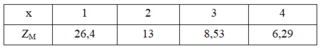
=> Cặp nghiệm thỏa mãn: x = 2 và Z M = 13 ⇒ M là Al
Thay x và ZM vào (7) và (2) ta tìm được y =3 và Z R = 8 ⇒ R là Oxi
Do đó hợp chất X là Al2O3 tổng số proton trong X là 13.2 + 8.3 = 50
Đáp án B.
Trong phân tử M2X, tổng số hạt proton, nơtron và electron là 140 hạt, số hạt mang điện nhiều hơn số hạt không mang điện là 44 hạt. Số khối của nguyên tử M lớn hơn số khối của nguyên tử X là 23. Số hạt mang điện tích âm trong một nguyên tử M nhiều hơn số hạt mang điện tích âm trong một nguyên tử X là 11 hạt. Xác định số hiệu nguyên tử của M và X ?
Đáp án:
K2O Giải chi tiết: Đặt số proton và notron của M lần lượt là p và n số proton và notron của X lần lượt là p' và n' Ta có hệ phương trình: ⎧⎪ ⎪ ⎪ ⎪⎨⎪ ⎪ ⎪ ⎪⎩2.(2p+n)+(2p′+n′)=140(1)(2.2p+2p′)−(2n+n′)=44(2)(p+n)−(p′+n′)=23(3)(2p+n)−(2p+n′)=34(4)Tu(1)va(2)⇒{2.(2p+p′)+(2n+n′)=1402.(2p+p′)−(2n+n′)=44⇒{2p+p′=46(5)2n+n′=48(6)Tu(3)va(4)⇒{(p−p′)+(n−n′)=232(p−p′)+(n−n′)=34⇒{p−p′=11(7)n−n′=12(8)Giai(5)va(7)⇒{p=19p′=8Giai(6)va(8)⇒{n=20n′=8{2.(2p+n)+(2p′+n′)=140(1)(2.2p+2p′)−(2n+n′)=44(2)(p+n)−(p′+n′)=23(3)(2p+n)−(2p+n′)=34(4)Tu(1)va(2)⇒{2.(2p+p′)+(2n+n′)=1402.(2p+p′)−(2n+n′)=44⇒{2p+p′=46(5)2n+n′=48(6)Tu(3)va(4)⇒{(p−p′)+(n−n′)=232(p−p′)+(n−n′)=34⇒{p−p′=11(7)n−n′=12(8)Giai(5)va(7)⇒{p=19p′=8Giai(6)va(8)⇒{n=20n′=8 Số khối của M là: A = p + n = 19 + 20 = 39 => M là Kali (kí hiệu: K) Số khối của X là: A' = p'+ n' = 8 + 8 = 16 => X là Oxi (kí hiệu: O) => CT hợp chất: K2O
Em tham khảo link này https://hoc24.vn/cau-hoi/cho-hop-chat-mx2-trong-phan-tu-nay-tong-so-hat-co-ban-la-140-va-so-hat-mang-dien-nhieu-hon-so-hat-ko-mang-dien-la-44-hatso-khoi-cua-x-lon-hon-so-kho.158928398419
Tổng số proton, nơtron, electron trong phân tử XY2 là 96. Số khối của nguyên tử Y bằng 0,6 lần số proton của nguyên tử X. Số khối của nguyên tử X nhiều hơn số hạt mang điện của Y là 28. Y là
A. Cl (Z=17)
B. C (Z=6)
C. S (Z=16)
D. F (Z=9)
Đáp án B
Theo giả thiết ta có: 2 ( Z X + 2 Z Y ) + N X + 2 N Y = 96 ( 1 ) Z Y + N Y = 0 , 6 Z X ( 2 ) Z X + N X - 2 Z Y = 28 ( 3 )
Thế (3) và (2) vào (1) ta có:
2 ( Z X + 2 Z Y ) + 28 - Z X + 2 Z Y + 2 ( 0 , 6 Z X - Z Y ) = 96 ⇔ 2 , 2 Z X + 4 Z Y = 68 ⇔ 11 Z X + 20 Z Y = 340 ⇔ Z Y = 340 - 11 Z X 20
Z Y là một số nguyên dương nên ta suy ra 340 - 11 Z X 20 phải là 1 số nguyên dương mà 340 chia hết cho 20 nên để 340 - 11 Z X 20 là một số nguyên dương thì Z X : 20 11 Z X < 340 ⇒ Z X = 20 ⇒ Z Y = 6 ⇒ Y
Tổng số proton, nơtron, electron trong phân tử XY2 là 96. Số khối của nguyên tử Y bằng 0,6 lần số proton của nguyên tử X. Số khối của nguyên tử X nhiều hơn số hạt mang điện của Y là 28. Y là
A. Cl (Z=17)
B. C (Z=6)
C. S (Z=16)
D. F (Z=9)
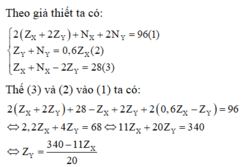
Z Y là một số nguyên dương nên ta suy ra 340 - 11 Z X 20 phải là 1 số nguyên dương mà 340 chia hết cho 20 nên để 340 - 11 Z X 20 là một số nguyên dương thì
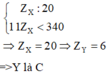
Đáp án B
Một nguyên tử của nguyên tố X có tổng số hạt proton, nơtron, electron là 52 và có số khối là 35. Số electron ở lớp vỏ nguyên tử nguyên tố X là
A. 18. B. 23. C. 15. D. 17.
Câu 7: 7.1: Hai nguyên tử A và B có tổng số hạt proton, nơtron, electron là 78, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 26. Số hạt mang điện của nguyên tử A nhiều hơn số hạt mang điện của nguyên tử B là 28. Hãy xác định hai nguyên tố A và B. Cho biết số hiệu nguyên tử của một số nguyên tố như sau: ZN = 7; ZNa = 11; ZCa = 20; ZFe = 26; ZCu = 29; ZC = 6; ZS = 16.
Câu 9: 9.1: Hòa tan hoàn toàn 10,2 gam một oxit kim loại hóa trị (III) cần 331,8 gam dung dịch H2SO4 vừa đủ. Dung dịch muối sau phản ứng có nồng độ 10%. Xác định công thức của oxit kim loại.
Nguyên tử X có tổng số hạt proton, nơtron, electron là 34. Biết số nơtron nhiều hơn số proton là 1. Số khối của nguyên tử X là
A. 11.
B. 23.
C. 35.
D. 46.
Chọn B
Gọi số hạt proton, nơtron, electron trong X lần lượt là p, n và e.
Theo bài ra ta có hệ phương trình :
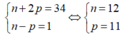
Vậy số khối của nguyên tử X là 11 + 12 = 23.
5. Nguyên tử Cacbon có 6e và số n nhiều hơn số p là 1 hạt 6. Nguyên tử Đồng có số khối là 65, số p ít hơn số n là 7 hạt 7. Nguyên tử Nhôm có 13 electron và số nơtron nhiều hơn proton 1 hạt 8. Nguyên tử Lưu huỳnh có số khối là 32, số proton bằng số11. Nguyên tử Hiđro có 1p và không có nơtron 12. Nguyên tử Natri có 1le và 12n
Nguyên tử (A) có tổng số proton, nơtron, electron là 94 trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22. Xác định số hạt electron, proton, notron và xác định tên nguyên tố và kí hiệu nguyên tử của A?
ta có
P+E+N=94 =>2P+N=94
P+E-N=22 => 2P-N=22
=> P=E=29,N = 36
=> A là kim loại đồng (Cu)