Dung dịch X gồm 0,3 mol K+; 0,6 mol Mg2+; 0,3 mol Na+; 0,6 mol Cl- và a mol Y2-. Cô cạn dung dịch X, thu được m gam muối khan. Ion Y2- và giá trị của m là
A. SO42- và 169,5.
B. CO32- và 126,3.
C. SO42- và 111,9.
D. CO32- và 90,3.
Dung dịch X gồm 0,3 mol K+; 0,6 mol Mg2+; 0,3 mol Na+; 0,6 mol Cl- và a mol Y2-. Cô cạn dung dịch X, thu được m gam muối khan. Ion Y2- và giá trị của m là
A. SO42- và 169,5
B. CO32- và 126,3.
C. SO42- và 111,9.
D. CO32- và 90,3.
Chọn C
Loại B, C vì CO32- tạo kết tủa với Mg2+. Như vậy Y2- là SO42-.
Bảo toàn điện tích ⇒ 0,3 + 0,6.2 + 0,3 = 0,6 + 2a ⇒ a = 0,6
⇒ m = 0,3.39 + 0,6.24 + 0,3.23 + 0,6.35,5 + 0,6.96 = 111,9
Dung dịch X gồm 0,3 mol K+; 0,6 mol Mg2+; 0,3 mol Na+; 0,6 mol Cl- và a mol Y2-. Cô cạn dung dịch X, thu được m gam muối khan. Ion Y2- và giá trị của m là
A. SO42- và 169,5.
B. CO32- và 126,3.
C. SO42- và 111,9.
D. CO32- và 90,3.
Đáp án : C
Y không thể là CO32- vì sẽ kết tủa Mg2+ => Y2- là SO42-
Bảo toàn điện tích : nK + 2nMg + nNa = nCl + 2nSO4
=> nSO4 = 0,6 mol
=> m = 111,9g
Dung dịch X gồm 0,15 mol K + ; 0,3 mol Mg 2 + ; 0,25 mol Na + ; a mol Cl - và b mol SO 4 2 - . Cô cạn dung dịch X thu được 61,8 gam muối khan. Giá trị của b là
A. 0,4
B. 0,3
C. 0,2
D. 0,5
Một dung dịch hỗn hợp X gồm Na+ (0,3 mol), K+(0,1 mol) và OH-. Cho 100ml dung dịch H2SO4 2M vào dung dịch X. Tính khối lượng muối thu được.
Muối thu đk:: Na+ :0,3mol , K+ :0,1mol , SO42- :0,2 mol → m=30g
Dung dịch X gồm fe2+0,1mol; h+0,2 mol và so4 2- .Dung dịch Y gồm na+0,3 mol ; ba2+ 0,1 mol và oh- .Trộn X với Y thì thu đc khối lượng kết tủa bn
Bảo toàn điện tích cho dung dịch X
2nSO4(2-) = 0,1.2+0,2=0,4(mol)
=> nSO4(2-) = 0,2(mol)
Bảo toàn điện tích cho dung dịch Y
nOH- = nNa+ + 2nBa2+ = 0,3 +2.0,1=0,5(mol)
OH- + H+ -> H2O
0,2......0,2 (mol)
Ba2+ + SO4 2- -> BaSO4
0,1.........0,1 .........0,1 (mol)
Fe2+ + 2OH- -> Fe(OH)2
0,1.........0,2 .......0,1 (mol)
mkết tủa = 0,1.233 + 0,1.90=32,3(g)
BTĐT X : 2.0,1+ 0,2=2.nSO4 2-
=> nSO4 2-=0.2
BTĐT Y : 0,3 + 0,1.2=nOH-
=>nOH-=0,5
H+ + OH- ---> H2O
0,2-----0,2
Ba2+ SO4 2- ----> BaSO4
0,1--------------------0,1
Fe2+ + 2OH------> Fe(0h)2
0,1-------------------0,1
mkết tủa = 0,1.233+ 0,1.90=32,3
Ba2+ + SO42- --> BaSO4
0.1______________0.1
H+ + OH- --> H2O
0.2___0.2
Fe2+ + 2OH- --> Fe(OH)2
0.1_____________0.1
mKt = mBaSO4 + mFe(OH)2 = 0.1*233 + 0.1*90=32.3 g
Dung dịch X chứa 0,2 mol K+; 0,3 mol Ba2+; 0,2 mol C l - ; x mol H C O 3 - . Giá trị của x là
A. 0,6
B. 0,4
C. 0,3
D. 0,2
Chọn đáp án A.
Bảo toàn điện tích có:
x = 0 , 2 + 2 . 0 , 3 - 0 , 2 = 0 , 6 m o l
Dung dịch X chứa 0,2 mol K+; 0,3 mol Ba2+; 0,2 mol C l - ; x mol H C O 3 - . Giá trị của x là
A. 0,6
B. 0,4
C. 0,3
D. 0,2
Chọn đáp án A.
Bảo toàn điện tích có x = 0,2 + 2.0,3 - 0,2 = 0,6 mol
Cho 0,3 mol hỗn hợp X gồm axit glutamic và lysin vào 400 ml dung dịch HCl 1M thu được dung dịch X. Biết Y phản ứng vừa đủ với 800ml dung dịch NaOH 1M. Số mol lysin trong hỗn hợp X là
A. 0,15
B. 0,25.
C. 0,1.
D. 0,2.
Hòa tan hoàn toàn hỗn hợp X gồm Al; K và BaO vào nước dư, thu được dung dịch Y và 0,27 mol khí H2. Cho từ từ đến hết dung dịch chứa 0,06 mol H2SO4 và 0,3 mol HCl vào Y, thu được 20,22 gam hỗn hợp kết tủa và dung dịch Z chỉ chứa 22,35 gam hỗn hợp các muối clorua và muối sunfat trung hòa. Phần trăm khối lượng của Al có trong X là?
A. 8,33%
B. 9,38%
C. 12,56%
D. 19,44%
Định hướng tư duy giải
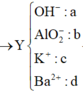

=> 0,3.35,5 + 96(0,06 – d) + 39c + 9(0,42 – 2d – c) = 22,35