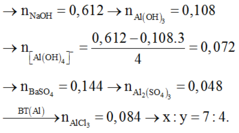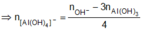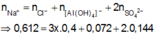Cho 400 ml dung dịch E gồm AlCl3 xM và Al2(SO4)3 yM tác dụng với 612 ml dung dịch NaOH 1M, sau các phản ứng xảy ra hoàn toàn kết thúc thí nghiệm ta thu được 8,424 gam kết tủa. Mặt khác, khi cho 400 ml E tác dụng với dung dịch BaCl2 dư thì ta thu được 33,552 gam kết tủa. Tỉ lệ x:y là
A. 4:3
B. 3:4
C. 7:4
D.3:2