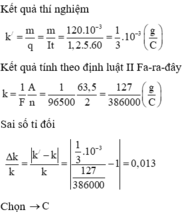Xác định điện tích nguyên tố e bằng cách dựa vào định luật II Fa-ra-đây về điện phân. Cho biết số Fa-ra-đây F = 96500 C/mol.

Những câu hỏi liên quan
Xác định độ lớn điện tích nguyên tố e bằng cách dựa vào định luật II Fa−ra− đây về điện phân. Biết số Fa−ra−đây F − 96500 C/mol, số Avo−ga−dro
N
A
6
,
023
.
10
23
. A.
1
,
606
.
10
-
19
C. B.
1
,
601
....
Đọc tiếp
Xác định độ lớn điện tích nguyên tố e bằng cách dựa vào định luật II Fa−ra− đây về điện phân. Biết số Fa−ra−đây F − 96500 C/mol, số Avo−ga−dro N A = 6 , 023 . 10 23 .
A. 1 , 606 . 10 - 19 C.
B. 1 , 601 . 10 - 19 C.
C. 1 , 605 . 10 - 19 C.
D. 1 , 602 . 10 - 19 C
đáp án D
m = 1 F A n q ,
xét nguyên tố hóa trị n = 1 thì m = 1 F A q .
+ Khi có 1 mol chất (số hạt là NA) giải phóng ra ở điện cực tức m = A thì q = F = 96500C → Độ lớn điện tích của một hạt ion hóa trị 1 (bằng độ lớn điện tích nguyên tố):
q 0 = 96500 6 , 023 . 10 23 = 1 , 602 . 10 - 19 C
Đúng 0
Bình luận (0)
Xác định độ lớn điện tích nguyên tố e bằng cách dựa vào định luật II Fa-ra-đây về điện phân. Biết số Fa-ra-đây F 96500 C/mol, số Avo-ga-dro
N
A
6
,
023
.
10
23
. A.
1
,
606
.
10
-
19
C
B.
1...
Đọc tiếp
Xác định độ lớn điện tích nguyên tố e bằng cách dựa vào định luật II Fa-ra-đây về điện phân. Biết số Fa-ra-đây F = 96500 C/mol, số Avo-ga-dro N A = 6 , 023 . 10 23 .
A. 1 , 606 . 10 - 19 C
B. 1 , 601 . 10 - 19 C
C. 1 , 605 . 10 - 19 C
D. 1 , 602 . 10 - 19 C
Xác định độ lớn điện tích nguyên tố e bằng cách dựa vào định luật II Fa–ra–đây về điện phân. Biết số Fa–ra–đây F 96500 C/mol, số Avo–ga–dro NA 6,023.
10
23
. A. 1,606.
10
-
19
C. B. 1,601.
10
-
19
C. C. 1,605....
Đọc tiếp
Xác định độ lớn điện tích nguyên tố e bằng cách dựa vào định luật II Fa–ra–đây về điện phân. Biết số Fa–ra–đây F = 96500 C/mol, số Avo–ga–dro NA = 6,023. 10 23 .
A. 1,606. 10 - 19 C.
B. 1,601. 10 - 19 C.
C. 1,605. 10 - 19 C.
D. 1,602. 10 - 19 C.
Đáp án D
Theo định luật II Fa-ra-đây về điện phân thì :
![]()
Muốn có một đượng lượng gam A/n của một chất giải phóng ra ở mồi điện cực của bình điện phân thì cần phải có điện lượng q = F culong chuyển qua bình điện phân . Điện lượng này đúng bằng tổng điện tích của các ion trong một đương lượng gam A/n của chất đó chuyển qua bình điện phân
Vì số nguyên tử có trong mỗi khối lượng mol nguyên tử A của một nguyên tố đúng bằng số Avô-ga-đrô
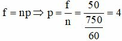
1 mol hóa trị n = 1 sẽ có điện tích qo tính bằng :

![]()
Đúng 0
Bình luận (0)
Để xác đương lượng điện hóa của đồng, một học sinh đã cho dòng điện có cường độ 1,2 A chạy qua bình điện phân chứa dung dịch đồng sunphat
C
u
S
O
4
trong khoảng thời gian 5,0 phút và thu được 120 mg đồng bám vào catôt. Xác định sai số tỉ đối của kết quả thí nghiệm do học sinh thực hiện với kết quả tính toán theo định luật II Fa-ra -đây về điện phân khi lấy hằng số...
Đọc tiếp
Để xác đương lượng điện hóa của đồng, một học sinh đã cho dòng điện có cường độ 1,2 A chạy qua bình điện phân chứa dung dịch đồng sunphat C u S O 4 trong khoảng thời gian 5,0 phút và thu được 120 mg đồng bám vào catôt. Xác định sai số tỉ đối của kết quả thí nghiệm do học sinh thực hiện với kết quả tính toán theo định luật II Fa-ra -đây về điện phân khi lấy hằng số Fa-ra -đây là F = 96500 (C/mol) khối lượng mol nguyên tử của đồng A = 63,5 g/mol và hóa trị n = 2
A. 2%
B. 2,3%
C. 1,3%
D. 1,2%
Để xác đương lượng điện hóa của đồng (Cu), một học sinh đã cho dòng điện có cường độ 1,2 A chạy qua bình điện phân chứa dung dịch đồng sunphat (
C
u
S
O
4
) trong khoảng thời gian 5,0 phút và thu được 120 mg đồng bám vào catôt. Xác định sai số tỉ đối của kết quả thí nghiệm do học sinh thực hiện với kết quả tính toán theo định luật II Fa – ra – đây về điện phân khi lấy số Fa – ra – đay F 96500 (C/mol), khối lượng mol nguyên tử củ...
Đọc tiếp
Để xác đương lượng điện hóa của đồng (Cu), một học sinh đã cho dòng điện có cường độ 1,2 A chạy qua bình điện phân chứa dung dịch đồng sunphat ( C u S O 4 ) trong khoảng thời gian 5,0 phút và thu được 120 mg đồng bám vào catôt. Xác định sai số tỉ đối của kết quả thí nghiệm do học sinh thực hiện với kết quả tính toán theo định luật II Fa – ra – đây về điện phân khi lấy số Fa – ra – đay F = 96500 (C/mol), khối lượng mol nguyên tử của đồng A = 63,5 g/mol và hóa trị n = 2
A. 2,2%
B. 2,3%
C. 1,3%
D. 1,2%
đáp án C
+ Kết quả thí nghiệm:
k / = m q = m I t = 120 . 10 - 3 1 , 2 . 5 . 60 = 1 3 . 10 - 3 g C
+ Kết quả tính theo định luật II Fa – ra – đây:
k = 1 F A n = 1 96500 63 , 5 2 = 127 386000 g C
+ Sai số tỉ đối:
Δ k k = k / - k k = 1 3 . 10 - 3 127 386000 - 1 = 0 , 013
Đúng 0
Bình luận (0)
Để xác đương lượng điện hóa của đồng (Cu), một học sinh đã cho dòng điện có cường độ 1,2 A chạy qua bình điện phân chứa dung dịch đồng sunphat (CuSO4) trong khoảng thời gian 5,0 phút và thu được 120 mg đồng bám vào catôt. Xác định sai số tỉ đối của kết quả thí nghiệm do học sinh thực hiện với kết quả tính toán theo định luật II Fa–ra–đây về điện phân khi lấy số Fa–ra–day F 96500 (C/mol), khối lượng mol nguyên tử của đồng A 63,5 g/mol và hóa trị n 2 A. 2,2% B. 2,3% C. 1,3% D. 1,2%
Đọc tiếp
Để xác đương lượng điện hóa của đồng (Cu), một học sinh đã cho dòng điện có cường độ 1,2 A chạy qua bình điện phân chứa dung dịch đồng sunphat (CuSO4) trong khoảng thời gian 5,0 phút và thu được 120 mg đồng bám vào catôt. Xác định sai số tỉ đối của kết quả thí nghiệm do học sinh thực hiện với kết quả tính toán theo định luật II Fa–ra–đây về điện phân khi lấy số Fa–ra–day F = 96500 (C/mol), khối lượng mol nguyên tử của đồng A = 63,5 g/mol và hóa trị n = 2
A. 2,2%
B. 2,3%
C. 1,3%
D. 1,2%
Đáp án C
Kết quả của học sinh tính
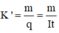
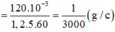
Kết quả của định luật II Fa-ra-đây:
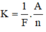

Sai số tỉ đối :
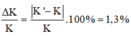
Đúng 0
Bình luận (0)
Cách tính số nguyên tử (n) trong một mol kim loại nào sau đây là đúng? (biết số Fa−ra−day là F và điện
tích nguyên tố là e).
A. n = F.e
B. n = F + e
C. n = F e
D. n = e F
Một bình điện phân chứa dung dịch AgN
O
3
với anôt bằng bạc. Khối lượng bạc bám vào catôt của bình điện phân sau 16 phút 5 giây là 6,48 g. Biết bạc có khối lượng mol là A 108 g/mol và hóa trị n 1. Lấy số Fa – ra – đây F 96500 C/mol. Cường độ dòng điện chạy qua bình điện phân là A. 5 A. B. 6 A. C. 0,5 A. D. 4 A.
Đọc tiếp
Một bình điện phân chứa dung dịch AgN O 3 với anôt bằng bạc. Khối lượng bạc bám vào catôt của bình điện phân sau 16 phút 5 giây là 6,48 g. Biết bạc có khối lượng mol là A = 108 g/mol và hóa trị n = 1. Lấy số Fa – ra – đây F = 96500 C/mol. Cường độ dòng điện chạy qua bình điện phân là
A. 5 A.
B. 6 A.
C. 0,5 A.
D. 4 A.
Đáp án B
+ Khối lượng Ag bám ở catot m = A I t F n → I = m F n A t = 6 , 48 . 96500 . 1 108 . 965 = 6 A .
Đúng 0
Bình luận (0)
Một bình điện phân chứa dung dịch AgN
O
3
với anôt bằng bạc. Khối lượng bạc bám vào catôt của bình điện phân sau 16 phút 5 giây là 6,48 g. Biết bạc có khối lượng mol là A 108 g/mol và hóa trị n 1. Lấy số Fa – ra – đây F 96500 C/mol. Cường độ dòng điện chạy qua bình điện phân là A. 5 A. B. 6 A. C. 0,5 A. D. 4 A.
Đọc tiếp
Một bình điện phân chứa dung dịch AgN O 3 với anôt bằng bạc. Khối lượng bạc bám vào catôt của bình điện phân sau 16 phút 5 giây là 6,48 g. Biết bạc có khối lượng mol là A = 108 g/mol và hóa trị n = 1. Lấy số Fa – ra – đây F = 96500 C/mol. Cường độ dòng điện chạy qua bình điện phân là
A. 5 A.
B. 6 A.
C. 0,5 A.
D. 4 A.
Đáp án B
+ Khối lượng Ag bám ở catot m = A I t F n → I = m F n A t = 6 , 48 . 96500 . 1 108 . 965 = 6 A .
Đúng 0
Bình luận (0)