Hòa tan 10 gam hỗn hợp gồm Fe và FexOy bằng HCl thu được 1,12 lít H2 (đktc). Cũng lượng hỗn hợp này nếu hòa tan hết bằng dung dịch HNO3 đặc nóng thu được 5,6 lít NO2 (đktc). Công thức FexOy là
A. FeO
B. Fe3O4
C. Fe2O3
D. Fe3O4 hay FeO
Hỗn hợp X gồm Fe, FeO, Fe2O3 và Fe3O4. Hòa tan X trong 400 ml dung dịch HCl 2M, thấy thoát ra 2,24 lít H2 (đktc) và còn lại 2,8 gam sắt chưa tan. Nếu cho toàn bộ hỗn hợp X vào dung dịch HNO3 đặc nóng (dư) thì thu được bao nhiêu lít khí NO2 (đktc)?
A. 4,48 lít.
B. 10,08 lít.
C. 16,8 lít.
D. 20,16 lít.
Hòa tan hết m gam hỗn hợp gồm a mol FeO , a mol Fe2O3 và b mol Fe3O4 bằng dung dịch HNO3 đặc nóng thu được 6,72 lít NO2 ( đktc ). Giá trị của m gam là
A. 46,4
B. 48,0
C. 35,7
D. 69,6
Hòa tan hết m gam hỗn hợp gồm x mol FeO, x mol Fe2O3 và y mol Fe3O4 bằng dung dịch HNO3 đặc nóng, thu được 6,72 lít NO2 (đktc). Giá trị của m là
A. 46,4.
B. 48,0.
C. 35,7.
D. 69,6.
Tiến hành phản ứng nhiệt nhôm hỗn hợp A gồm Al và Fe x O y (trong điều kiện không có không khí) được hỗn hợp B. Nghiền nhỏ, trộn đều hỗn hợp B rồi chia thành hai phần.
Phần 1 : có khối lượng 10,2 gam được hòa tan hết trong dung dịch HNO 3 dư, đun nóng thu được dung dịch C và 2,912 lít NO (sản phẩm khử duy nhất).
Phần 2 : tác dụng với dung dịch NaOH dư đun nóng thu được 0,672 lít H 2 đktc và còn lại 2,52 gam chất rắn.
Biết các phản ứng xảy ra hoàn toàn, thể tích các khí đo ở đktc. Công thức Fe x O y là
A. Fe 3 O 4
B. FeO
C. Fe 2 O 3
D. FeO hoặc F Fe 3 O 4
Hòa tan hoàn toàn hỗn hợp gồm Fe, FeO, Fe2O3 và Fe3O4 bằng lượng vừa đủ 300ml dung dịch HNO3 5M thu được V lít hỗn hợp khí NO2 và NO (đktc) và 96,8 gam Fe(NO3) . Giá trị của V là
A. 4,48 lít
B. 2,24 lít
C. 8,96 lít
D. 6,72 lít
Đáp án D
n Fe ( NO 3 ) 3 = 0 , 4 ; n HNO 3 = 1 , 5
Áp dụng định luật bảo toàn nguyên tố cho N, ta có:
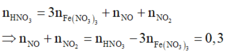
Vậy V = 0,3.22,4 = 6,72 (lít)
Hòa tan hoàn toàn 2,44 gam hỗn hợp bột X gồm FexOy và Cu bằng dung dịch HNO3 đặc nóng (dư). Sau phản ứng thu được 0,336 lít khí NO (sản phẩm khử duy nhất ở đktc) và dung dịch chứa 7,93 gam hỗn hợp muối nitrat. Phần trăm khối lượng của Cu trong X là:
A. 39,34%
B. 65,57%
C. 26,23%
D. 13,11%
Quy hỗn hợp X gồm có a mol Fe, b mol Cu và c mol O
Ta có 56a + 64b + 16c= 2,44
Bảo toàn nguyên tố Fe và Cu có nFe(NO3)3= nFe= a mol;nCu(NO3)2= nCu= b mol
Khối lượng muối nitrat là
mmuối= mFe(NO3)3+ mCu(NO3)2=242a + 188b= 7,93 gam
QT cho e:
Fe→ Fe3++ 3e
a 3amol
Cu → Cu2++ 2e
b 2b
QT nhận e :
O+ 2e→ O-2
c 2c
N+5+ 3e → NO
0,045← 0,015
Theo ĐL BT electron thì : ne cho= ne nhận nên 3a+ 2b= 2c+ 0,045 (3)
Giải hệ gồm (1), (2) và (3) có a= 0,025; b= 0,01 và c= 0,025
→%mCu= 0,01.64.100%/2,44=26,23%
Đáp án C
Tiến hành phản ứng nhiệt nhôm hỗn hợp A gồm Al và Fe x O y (trong điều kiện không có không khí) được hỗn hợp B. Nghiền nhỏ, trộn đều hỗn hợp B rồi chia thành hai phần.
- Phần 1 : có khối lượng 4,83 gam được hòa tan hết trong dung dịch HNO 3 dư, đun nóng thu được dung dịch C và 1,232 lít NO (sản phẩm khử duy nhất).
- Phần 2 : tác dụng với dung dịch NaOH dư đun nóng thu được 1,008 lít H 2 và còn lại 7,56 gam chất rắn.
Biết các phản ứng xảy ra hoàn toàn, thể tích các khí đo ở đktc. Công thức Fe x O y là
A. Fe 3 O 4
B. FeO
C. Fe 2 O 3
D. FeO hoặc Fe 3 O 4
Hòa tan hết m gam hỗn hợp X gốm Mg, F e C l 3 vào nước chỉ thu được dung dịch Y gồm 3 muối và không còn chất rắn. Nếu hòa tan m gam X bằng dung dịch HCl dư thì thu được 2,688 lít H 2 (đktc). Dung dịch Y có thể hòa tan vừa hết 1,12 gam bột Fe. Giá trị của m là:
A. 46,82 gam
B. 56,42 gam
C. 48,38 gam
D. 52,22 gam
M g + 2 F e C l 3 → M g C l 2 + 2 F e C l 2 (1)
M g + 2 H C l → M g C l 2 + H 2 (2)
Từ phản ứng (2) ta có:
n M g = n H 2 = 2,688/22,4 = 0,12 mol
Dung dịch Y gồm 3 muối ⇒ M g C l 2 , F e C l 2 , F e C l 3 ⇒ F e C l 3 sau phản ứng (1) còn dư.
⇒ n F e C l 3 (1) = 2.nMg = 2.0,12 = 0,24g
F e + 2 F e C l 3 → 3 F e C l 2 (3)
⇒ n F e C l 3 (3) = 2 n F e = 0,04 mol
⇒ n F e C l 3 b d = n F e C l 3 ( 3 ) + n F e C l 3 ( 1 )
= 0,04+0,24 = 0,28g
⇒ m X = 0,12.24 + 0,28.(56+35,5.3) = 48,3g
⇒ Chọn C.
Hòa tan hoàn toàn m gam hỗn hợp A gồm Fe và kim loại M ( hóa trị không đổi) trong dung dịch HCl dư, thu được 1,008 lít khí (đktc) và dung dịch chứa 4,575 gam muối.
1. Tính khối lượng m.
2. Hòa tan hết m gam hỗn hợp A trong dung dịch chứa đồng thời hai axit: HNO3 ( đặc) và H2SO4 ( khi đun nóng) thu được 1,8816 lít hỗn hợp B gồm 2 khí (đktc). Tỉ khối của hỗn hợp B so với H2 bằng 25,25. Xác định kim loại M biết rằng trong dung dịch tạo thành không chứa muối amoni.
Câu 1

Áp dụng định luật bảo toàn nguyên
tố H ta có:
nHCl = 2nH2 = 2.0,045 = 0,09 mol
Áp dụng định luật bảo toàn khối lượng
ta có: mA + mHCl = m muối + mH2
=> m = m muối + mH2 – mA = 4,575 + 0,045.2 – 0,09.36,5 = 1,38 (gam)
Câu 2

Do cho kim loại phản ứng với H2SO4 đặc và HNO3 đặc nên khí sinh ra là SO2 và NO2.
Áp dụng phương pháp đường chéo ta có:
SO2: 64 4,5
50,5
NO2: 46 13,5
→nSO2=nNO2=4,513,5=13

Đặt số mol của Fe và M lần lượt là x và y (mol)
- Khi cho hỗn hợp tác dụng với HCl:
Fe + 2HCl → FeCl2 + H2
x x (mol)
M + nHCl → MCln + 0,5nH2
y 0,5ny (mol)
nH2 = 0,045 => x + 0,5ny = 0,045 (1)
- Khi cho hỗn hợp tác dụng với HNO3 đặc và H2SO4 đặc:
Ta có các bán phản ứng oxi hóa – khử:
Fe → Fe3+ + 3e
x 3x
M → Mn+ + ne
y ny
S+6 + 2e → S+4 (SO2)
0,021 0,042
N+5 + 1e → N+4 (NO2)
0,063 0,063
Áp dụng định luật bảo toàn electron ta có: 3x + ny = 0,042 + 0,063 hay 3x + ny = 0,105 (2)
Từ (1) và (2) ta có hệ phương trình sau:

Mặt khác: mA = mFe + mM => 1,38 = 0,015.56 + My => My = 0,54(4)
Từ (3) và (4) suy ra M = 9n
Ta có bảng sau:
| n |
1 |
2 |
3 |
| M |
9 (loại) |
18 (loại) |
27 (nhận) |
Vậy kim loại M là nhôm, kí hiệu là Al.