Cho 4,05 gam Al tác dụng với dung dịch H2SO4 loãng dư thu được V lít khí H2 ở đktc. Giá trị của V là
A. 2,24
B. 3,36
C. 4,05
D. 5,04
Câu 33. Cho a gam nhôm tác dụng với 300 gam dung dịch H2SO4 loãng 3M , D = 1,2 g/ml thu được V lít khí hiđro (đktc). Giá trị của a, V lần lượt là
A. 13,5; 8,96 B. 8,1 ; 16,8 C. 4,05; 13,44 D. 13,5 ; 16,8
Hòa tan hoàn toàn 4,05 gam Al trong dung dịch HCl dư, thu được V lít khí H2 (đktc). Giá trị của V là
A. 3,36
B. 5,04
C. 6,72
D. 5,6
Đáp án B
Phương pháp: Bảo toàn e
Hướng dẫn giải: Bảo toàn e ta có: 3nAl = 2nH2 => nH2 = 1,5nAl = 1,5.(4,05/27) = 0,225 mol
=> V = 0,225.22.4 = 5,04 lít
`n_(H_2)=V/(22,4)=(3,36)/(22,4)=0,15(mol)`
\(PTHH:2Al+3H_2SO_4->Al_2\left(SO_4\right)_3+3H_2\)
tỉ lệ 2 ; 3 ; 1 ; 3
n(mol) 0,1<-------------------------------------0,15
`m_(Al)=n*M=0,1*27=2,7(g)`
`=>B`
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,1<-----------------------------------0,15
\(m_{Al}=0,1.27=2,7\left(g\right)\)
Vậy chọn B.
Hòa tan hoàn toàn 4,05 gam Al bằng dung dịch NaOH dư thu được V lít H 2 ( đo ở đktc). Giá trị của V là:
A. 5,60
B. 2,24
C. 4,48
D. 5,04
Cho m gam hỗn hợp 2 kim loại Al và Cu chia làm 2 phần bằng nhau :
- Phần 1 : Cho tác dụng với dung dịch H 2 SO 4 loãng, dư thu được 1,344 lít khí H 2 (đktc).
- Phần 2 : Cho tác dụng với dung dịch H 2 SO 4 đặc nóng, dư, thu được 2,24 lít khí SO 2 (đktc) .Xác định giá trị của m.
Các PTHH :
2Al + 3 H 2 SO 4 → Al 2 SO 4 3 + 3 H 2 (1)
2Al + 6 H 2 SO 4 → Al 2 SO 4 3 + 3 SO 2 + 6 H 2 O (2)
Cu + 2 H 2 SO 4 → Cu SO 4 + 2 H 2 O + SO 2 (3)
Theo PTHH (1) số mol Al tham gia phản ứng bằng 2/3 số mol H 2 => Khối lượng AI trong hỗn hợp : 2×2/3×0,06×27 = 2,16(g)
Số mol SO 2 được giải phóng bởi Al: 2,16/27 x 3/2 = 0,12 mol
Theo PTHH (2) và (3) số mol SO 2 giải phóng bởi Cu : 2.0,1 - 0,12 = 0,08 (mol)
Theo PTHH (3) khối lượng Cu trong hỗn hợp : 0,08. 64 = 5,12 (g)
Vậy m = 2,16 + 5,12 = 7,28 (g).
Cho 16,8 gam sắt tác dụng với dung dịch H2SO4 loãng dư thu được V lít khí H2 đktc. Giá trị của V là
A. 13,44
B. 10,08
C. 4,48
D. 6,72
Chọn đáp án D
Ta có: ne=0,3
=>nH2=0,3
=>V=6,72(l)
Hòa tan m gam Fe trong dung dịch H2SO4 loãng thì sinh ra 3,36 lít khí (đktc). Nếu cho m gam Fe tác dụng với H2SO4 đặc, nóng, dư thì thu được V lít khí SO2 (đktc). Giá trị của V là
A. 10,08.
B. 5,04.
C. 3,36.
C. 3,36.
Đáp án B
Xét giai đoạn m gam Fe tác dụng với dung dịch H2SO4 loãng:
Sơ đồ phản ứng :
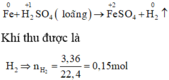
Các quá trình nhường, nhận electron :
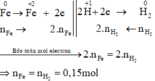
Xét giai đoạn m gam Fe tác dụng với H2SO4 đặc, nóng , dư:
Sơ đồ phản ứng:
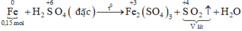
Các quá trình nhường, nhận electron:
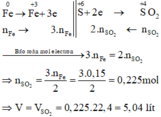
Nung nóng m gam hỗn hợp Al và Fe 2 O 3 (trong môi trường không có không khí) đến khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp rắn Y. Chia Y thành hai phần bằng nhau:
- Phần 1 tác dụng với dung dịch H 2 SO 4 loãng (dư), sinh ra 5,04 lít khí H 2 (ở đktc);
- Phần 2 tác dụng với dung dịch NaOH (dư), sinh ra 1,68 lít khí H 2 (ở đktc).
Giá trị của m là
A. 22,7
B. 21,4
C. 17,4
D. 34,8
Cho 1,3 gam Zn và 1,6 gam Cu tác dụng với dung dịch H 2 S O 4 loãng, dư. Sau phản ứng thu được V lít khí H 2 (đktc). Giá trị của V là
A. 1,008 lít.
B. 0,336 lít.
C. 0,448 lít.
D. 0,672 lít.