Cho 14 gam hỗn hợp Mg, Fe, Zn vào dung dịch H2SO4 loãng dư tạo ra 6,72 lít H2 (đktc). Khối lượng muối sunfat thu được trong dung dịch là:
A. 53,1 gam
B. 42,8 gam
C. 32,4 gam.
D. 38,4 gam
Cho 13,6 gam hỗn hợp kim loại Fe, Mg vào dung dịch H2SO4 loãng, dư thu được 6,72 lít H2 (đktc) và dung dịch A. Cho NaOH dư vào dung dịch A thu được kết tủa B. Lọc và nung B trong không khí đến khối lượng không đổi thu được m gam chất rắn. Giá trị của m là:
- Đặt nFe=a (mol); nMg=b (mol)
- nH2=0,3 (mol)
pư: Mg+2HCl --> MgCl2 +H2
Fe+2HCl --> FeCl2 +H2
=> hệ: 56a+24b=13,6
a+b=0,3
=> a=0,2 (mol) ; b=0,1 (mol)
- Bảo toàn Fe => nFe2O3=0,1 (mol)
- Bảo toàn Mg => nMgO=0,1 (mol)
=> mrắn=20 (g)
Hỗn hợp X gồm Al, Zn và Fe. Cho m gam hỗn hợp X tác dụng với H2SO4 loãng dư, thu được 5,6 lít H2 (đktc). Mặt khác, khi hòa tan hoàn toàn X trong dung dịch H2SO4 đặc nóng (dư), thu được 6,72 lít SO2 (đktc). Khối lượng Fe có trong m gam hỗn hợp X là
A. 5,6 gam.
B. 8,4 gam.
C. 6,72 gam.
D. 2,8 gam.
Hỗn hợp X gồm Al, Zn và Fe. Cho m gam hỗn hợp X tác dụng với H2SO4 loãng, dư thu được 5,6 lít H2 (đktc). Mặt khác, khi hòa tan hoàn toàn X trong dung dịch H2SO4 đặc, nóng dư thu được 6,72 lít SO2 (đktc). Tính khối lượng Fe có trong m gam hỗn hợp X
A. 5,6 gam
B. 8,4 gam
C. 6,72 gam
D. 2,8 gam
Đáp án : A
nH2 = 0,25 mol; nSO2 = 0,3 mol
2H+ + 2e → H2 S+6 + 2e → S+4
0,5 <-- 0,25 0,6 <-- 0,3
nFe = 0,6 – 0,5 = 0,1 mol
=> mFe = 5,6g
Lấy 10,3g gam hỗn hợp gồm Al và Mg trong dung dịch H2SO4 loãng dư thu được 11,2 lít khí H2 (đktc) tính khối lượng muối sunfat tạo thành 9 (áp dụng định luật bảo toàn khối lượng)
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
$Mg + H_2SO_4 \to MgSO_4 + H_2$
Theo PTHH :
$n_{H_2SO_4\ pư} = n_{H_2} = \dfrac{11,2}{22,4} = 0,5(mol)$
Bảo toàn khối lượng :
$m_{muối} = 10,3 + 0,5.98 - 0,5.2 = 58,3(gam)$
Cho 30,8 gam hỗn hợp X gồm Fe, FeO, FeCO3, Mg, MgO và MgCO3 tác dụng vừa đủ với dung dịch H2SO4 loãng, thu được 7,84 lít (đktc) hỗn hợp khí Y gồm CO2, H2 và dung dịch Z chỉ chứa 60,4 gam hỗn hợp muối sunfat trung hòa. Tỉ khối của Y so với He là 6,5. Khối lượng của FeSO4 trong dung dịch Z là
A. 22,4 gam.
B. 30,4 gam.
C. 26,8 gam.
D. 30,0 gam.
Đáp án B
Dùng phương pháp đường chéo tính được mol CO2 là 0,2 mol và H2 là 0,15 mol.
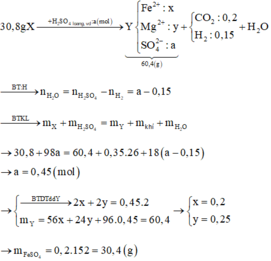
Cho 14,5g hỗn hợp Mg, Fe, Zn tác dụng hết với dung dịch H2SO4 loãng thấy thoát ra 6,72 lít H2 (đktc). Cô cạn dung dịch sau phản ứng được khối lượng muối khan tạo ra là:
A. 34,3 g
B. 43,3 g
C. 33,4 g
D. 33,8 g
Cho 20,2 gam hỗn hợp X gồm Zn và Mg vào dung dịch H 2 SO 4 loãng dư thu được 11,2 lít khí (đktc). Cô cạn dung dịch sau phản ứng, khối lượng muối khan thu được là
A. 68,2 gam.
B. 70,25 gam.
C. 60,0 gam.
D. 80,5 gam.
Đáp án A
Gọi M là kim loại chung cho Zn và Mg với hóa trị n
Sơ đồ phản ứng: M + H 2 SO 4 ( loãng , dư ) → M 2 ( SO 4 ) n ⏟ muối + H 2 ↑
Khí thu được là
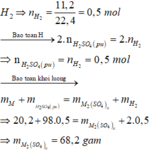
Hòa tan hoàn toàn 2,43 gam hỗn hợp gồm Mg và Zn vào một lượng vừa đủ dung dịch H2SO4 loãng, sau phản ứng thu được 1,12 lít H2 (đktc) và dung dịch X. Khối lượng muối trong dung dịch X là
A. 7,23.
B. 5,83
C. 7,33
D. 4,83
Hòa tan hoàn toàn 2,43 gam hỗn hợp gồm Mg và Zn vào một lượng vừa đủ dung dịch H2SO4 loãng, sau phản ứng thu được 1,12 lít H2 (đktc) và dung dịch X. Khối lượng muối trong dung dịch X là
A. 5,83 gam
B. 4,83 gam
C. 7,33 gam
D. 7,23 gam
Đáp án D
Ta có mMuối = mKim loại + mSO42–.
Mà nSO42– = nH2 = 0,05 mol.
⇒ mMuối = 2,43 + 0,05×96 = 7,23 gam