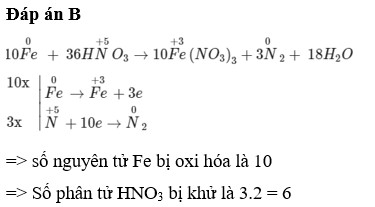Do liên kết H-O trong phân tử HNO3 phân cực , nên HNO3 phân li hoàn toàn và tạo ra ion …... khi hòa tan
vào H2O, theo thuyết ……………… HNO3 thể hiện tính ……..…… Dung dịch HNO3 làm ………… chuyển đỏ, tác
dụng ………., ………., …………

Những câu hỏi liên quan
Hoà tan hoàn toàn 10,2 gam Al2O3 trong dung dịch HNO3 15% a) Tính khối lượng dung dịch HNO3 phản ứng b) Tính số phân tử nước tạo thành mn giúp mình với
\(n_{Al_2O_3}=\dfrac{10.2}{102}=0.1\left(mol\right)\)
\(Al_2O_3+6HNO_3\rightarrow2Al\left(NO_3\right)_3+3H_2O\)
\(0.1...........0.6..................................0.3\)
\(m_{dd_{HNO_3}}=\dfrac{0.6\cdot63\cdot100}{15}=252\left(g\right)\)
Số phân tử nước :
\(0.3\cdot6\cdot10^{23}=1.8\cdot10^{23}\left(pt\right)\)
Đúng 2
Bình luận (0)
a)
n Al2O3 = 10,2/102 = 0,1(mol)
$Al_2O_3 + 6HNO_3 \to 2Al(NO_3)_3 + 3H_2O$
n HNO3 = 6n HNO3 = 0,6(mol)
=> m dd HNO3 = 0,6.63/15% = 252(gam)
b)
n H2O = 3n Al2O3 = 0,3(mol)
Số nguyên tử H2O : N = 0,3.6.1023 = 1,8.1023 phân tử
Đúng 2
Bình luận (0)
a) Số mol của Al203 là
nAl2O3 = \(\dfrac{10,2}{102}=0,1\) ( mol )
Theo PTHH :
Al203 + 6HNO3 → 2Al(NO3)3 + 3H20
0,1 0,6 0,3
Khối lượng HNO3 là :
mHNO3 = 0,6 . 63 = 37,8 g
Khối lượng dung dịch HNO3 phản ứng là :
mddHNO3 = \(\dfrac{37,8}{15}.100=252\) g
b) Theo PTHH : nH20 = 0,3 mol
Số phân tử nước tạo thành là :
0,3 . 6,022.1023 = 1,8066.1023 ( phân tử )
Đúng 0
Bình luận (0)
Có các nhận xét sau về N và hợp chất của nó:1) N2 tương đối trơ về hoạt động hóa học ở điều kiện thường vì trong phân tử có một liên kết ba bền.2) Khí NH3 tan tốt trong H2O tạo được dung dịch có môi trường bazơ.3) HNO3 được tạo ra khi cho hỗn hợp khí (NO2 và O2) sục vào H2O.4) Khi phản ứng với Fe2O3 thì HNO3 đóng vai trò là chất oxi hóa.5) Khi sục khí NH3 đến dư vào dung dịch CuSO4 thì sau phản ứng hoàn toàn thu được kết tủa màu xanh.6) Trong công nghiệp NH3 được tạo ra khi cho N2 phản ứng với H...
Đọc tiếp
Có các nhận xét sau về N và hợp chất của nó:
1) N2 tương đối trơ về hoạt động hóa học ở điều kiện thường vì trong phân tử có một liên kết ba bền.
2) Khí NH3 tan tốt trong H2O tạo được dung dịch có môi trường bazơ.
3) HNO3 được tạo ra khi cho hỗn hợp khí (NO2 và O2) sục vào H2O.
4) Khi phản ứng với Fe2O3 thì HNO3 đóng vai trò là chất oxi hóa.
5) Khi sục khí NH3 đến dư vào dung dịch CuSO4 thì sau phản ứng hoàn toàn thu được kết tủa màu xanh.
6) Trong công nghiệp NH3 được tạo ra khi cho N2 phản ứng với H2.
Trong các nhận xét trên số nhận xét đúng là:
A. 2
B. 3
C. 4
D. 5
Có các nhận xét sau về N và hợp chất của nó: 1) N2 tương đói trơ về hoạt dộng hóa học ở điều kiện thường vì trong phân tử có một liên kết ba bền. 2)Khí NH3 tan tốt trong H2O tạo được dung dịch có môi trường bazơ. 3)HNO3 được tạo ra khi cho hỗn hợp khí (NO2 và O2) sục vào H2O. 4)Khi phản ứng với Fe2O3 thì HNO3 đóng vai trò là chất oxi hóa. 5)Khi sục khí NH3 đến dư vào dung dịch CuSO4 thì sau phản ứng hoàn toàn thu dược kết tủa màu xanh. ...
Đọc tiếp
Có các nhận xét sau về N và hợp chất của nó:
1) N2 tương đói trơ về hoạt dộng hóa học ở điều kiện thường vì trong phân tử có một liên kết ba bền.
2)Khí NH3 tan tốt trong H2O tạo được dung dịch có môi trường bazơ.
3)HNO3 được tạo ra khi cho hỗn hợp khí (NO2 và O2) sục vào H2O.
4)Khi phản ứng với Fe2O3 thì HNO3 đóng vai trò là chất oxi hóa.
5)Khi sục khí NH3 đến dư vào dung dịch CuSO4 thì sau phản ứng hoàn toàn thu dược kết tủa màu xanh.
6) Trong công nghiệp NH3 được tạo ra khi cho N2 phản ứng với H2.
Trong các nhận xét trên số nhận xét đúng là:
A.2
B.3
C.4
D.5
Chọn đáp án C
1) N2 tương đói trơ về hoạt dộng hóa học ở điều kiện thường vì trong phân tử có một liên kết ba bền.(Đúng)
2)Khí NH3 tan tốt trong H2O tạo được dung dịch có môi trường bazơ.(Đúng)
3)HNO3 được tạo ra khi cho hỗn hợp khí (NO2 và O2) sục vào H2O.(Đúng)
4)Khi phản ứng với Fe2O3 thì HNO3 đóng vai trò là chất oxi hóa.
5)Khi sục khí NH3 đến dư vào dung dịch CuSO4 thì sau phản ứng hoàn toàn thu dược kết tủa màu xanh.(Sai tạo phức)
6) Trong công nghiệp NH3 được tạo ra khi cho N2 phản ứng với H2.(Đúng)
Đúng 0
Bình luận (0)
Cho sắt tan hoàn toàn trong dung dịch
H
N
O
3
loãng, nóng thu được khí
N
2
. Sau khi đã cân bằng số phân tử
H
N
O
3
bị khử và số nguyên tử Fe bị oxi hóa là A. 10 và 6 B. 6 và 10 C. 10 và 3 D. 3 và 10
Đọc tiếp
Cho sắt tan hoàn toàn trong dung dịch H N O 3 loãng, nóng thu được khí N 2 . Sau khi đã cân bằng số phân tử H N O 3 bị khử và số nguyên tử Fe bị oxi hóa là
A. 10 và 6
B. 6 và 10
C. 10 và 3
D. 3 và 10
Phân tử HNO3 có cấu tạo như sau: Các loại liên kết có trong phân tử HNO3 là A. cộng hoá trị và ion B. ion và phối trí C. phối trí (cho - nhận) và cộng hoá trị D. cộng hoá trị và hiđro
Đọc tiếp
Phân tử HNO3 có cấu tạo như sau:
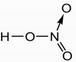
Các loại liên kết có trong phân tử HNO3 là
A. cộng hoá trị và ion
B. ion và phối trí
C. phối trí (cho - nhận) và cộng hoá trị
D. cộng hoá trị và hiđro
Chọn C
phối trí (cho - nhận) và cộng hoá trị
Đúng 0
Bình luận (0)
Trong phản ứng: Al + HNO3
→
Al(NO3)3 + NO + H2O, số phân tử HNO3 bị Al khử và số phân tử HNO3 tạo muối nitrat là: A. 1 và 3. B. 3 và 2. C. 4 và 3. D. 3 và 4.
Đọc tiếp
Trong phản ứng: Al + HNO3 → Al(NO3)3 + NO + H2O, số phân tử HNO3 bị Al khử và số phân tử HNO3 tạo muối nitrat là:
A. 1 và 3.
B. 3 và 2.
C. 4 và 3.
D. 3 và 4.
Al + 4HNO3 → Al(NO3)3 + NO + 2H2O
Số phân tử HNO3 bị khử thành NO là 1; số phân tử HNO3 tạo muối Al(NO3)3 là 3 ⇒ Chọn A.
Đúng 0
Bình luận (0)
Trong phản ứng: Al + HNO3
→
Al(NO3)3 + NO + H2O, số phân tử HNO3 bị Al khử và số phân tử HNO3 tạo muối nitrat là: A. 1 và 3 B. 3 và 2 C. 4 và 3 D. 3 và 4
Đọc tiếp
Trong phản ứng: Al + HNO3 → Al(NO3)3 + NO + H2O, số phân tử HNO3 bị Al khử và số phân tử HNO3 tạo muối nitrat là:
A. 1 và 3
B. 3 và 2
C. 4 và 3
D. 3 và 4
Đáp án A
Al + 4HNO3 → Al(NO3)3 + NO + 2H2O
Số phân tử HNO3 bị khử thành NO là 1; số phân tử HNO3 tạo muối Al(NO3)3 là 3
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 10,8g một oxit sắt trong dung dịch HNO3 dư thoát ra 1,12l khí NO ở đktc. Tìm công thức phân tử của oxit sắt
nNO=0,05 mol
Gọi CT oxit sắt là Fe2On
Fe+n => Fe+3 +(3-n)e
0,15/(3-n)mol<= 0,15mol
N+5 +3e =>N+2
0,15 mol<=0,05 mol
=>n oxit sắt=0,075/(3-n) mol
=>m oxit=0,075(56.2+16n)=10,8(3-n)
=> n=2
=>CT oxit là FeO
Đúng 0
Bình luận (2)
Hòa tan hoàn toàn 10,8g một oxit sắt trong dung dịch HNO3 dư thoát ra 1,12l khí NO ở đktc. Tìm công thức phân tử của oxit sắt
nNO=0,05 mol
Gọi CT oxit sắt là Fe2On
0,15/(3-n)mol<= 0,15mol
N+5 +3e =>N+2
0,15 mol<=0,05 mol
=>n oxit sắt=0,075/(3-n) mol
=>m oxit=0,075(56.2+16n)=10,8(3-n)
=> n=2
=>CT oxit là FeO
Đúng 0
Bình luận (0)
nNO=0,05 mol
Gọi CT oxit sắt là Fe2On
Fe+n => Fe+3 +(3-n)e
0,15/(3-n)mol<= 0,15mol
N+5 +3e =>N+2
0,15 mol<=0,05 mol
=>n oxit sắt=0,075/(3-n) mol
=>m oxit=0,075(56.2+16n)=10,8(3-n)
=> n=2
=>CT oxit là FeO
Đúng 0
Bình luận (0)
oxit sắt gồm Fe và O
coi nFe=a mol; nO=b mol
có 56a+16b=10,8
Fe0->Fe3++3e Oo+2e->O2-
a 3a b 2b
N5++3e->N3+
0,15 0,05
suy ra 3a=2b+0,15
ta tính a=0,15,b=0,15
a:b=1:1--->CT FeO
Đúng 0
Bình luận (0)