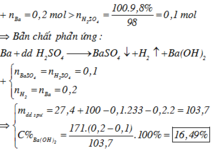cho m(gam) dung dịch bari clorua tác dung với 100g dung dịch axit sunfuric tạo thành 4,66 g kết tủa trắng.Tính m và nồng độ phần trăm dung dịch sau phản ứng
Lưu ý : mdd = mbd +mct - mkết tủa/m khí

Những câu hỏi liên quan
Cho 8 gam sắt 3 oxit tác dụng vừa đủ với 100 gam dung dịch axit sunfuric a% Tính a Tính nồng độ phần trăm dung dịch muối sau phản ứng Cho dung dịch muối sau phản ứng tác dụng với dung dịch natri hiđroxit dư tính khối lượng kết tủa thu được
\(n_{Fe_2O_3}=\dfrac{8}{160}=0,05\left(mol\right)\)
PTHH: Fe2O3 + 3H2SO4 --> Fe2(SO4)3 + 3H2O
______0,05------>0,15--------->0,05
=> mH2SO4 = 0,15.98 = 14,7(g)
=> \(C\%\left(H_2SO_4\right)=\dfrac{14,7}{100}.100\%=14,7\%\)
\(C\%\left(Fe_2\left(SO_4\right)_3\right)=\dfrac{0,05.400}{8+100}.100\%=18,52\%\)
PTHH: Fe2(SO4)3 + 6NaOH --> 2Fe(OH)3\(\downarrow\) + 3Na2SO4
________0,05----------------------->0,1
=> mFe(OH)3 = 0,1.107=10,7(g)
Đúng 0
Bình luận (0)
Dung dịch A chứa CuSO4 8% và (NH4) 2SO4 6,6% . Cho 15,07g Bari vào 100g dung dịch A, sau phản ứng thứ được dung dịch B, khí C và kết tủa D. Tính nồng độ phần trăm chất tan trong dung dịch B
Xem chi tiết
Cho 4,11 gam kim loại bari tác dụng với 19,6 gam dung dịch axit sunfuric 10%, người ta thu được dung dịch A, kết tủa m gam B và V lít khí D (đktc). Tính nồng độ phần trăm của chất tan trong dung dịch A.
Cho 16 gam đồng (II) oxit CuO phản ứng vửa đủ với 400 gam dung dịch axit sunfuric H2SO4 thu được dung dịch A
a)Viết pthh xảy ra
b)Tính nồng độ phần trăm của dung dịch axit clohidric
c)Tính nồng độ phần trăm muối reong dung dịch sau phản ứng
d)Cho dd A tác dụng hoàn toàn với BaCl2 thu được m kết tủa B .Tính m
a) PTHH: CuO + H2SO4 → CuSO4 + H2O (1)
b) \(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
Theo PT1: \(n_{H_2SO_4}=n_{CuO}=0,2\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=0,2\times98=19,6\left(g\right)\)
\(\Rightarrow C\%_{ddH_2SO_4}=\dfrac{19,6}{400}\times100\%=4,9\%\)
c) Theo PT1: \(n_{CuSO_4}=n_{CuO}=0,2\left(mol\right)\)
\(\Rightarrow m_{CuSO_4}=0,2\times160=32\left(g\right)\)
\(\Sigma m_{dd}=16+400=416\left(g\right)\)
\(\Rightarrow C\%_{ddCuSO_4}=\dfrac{32}{416}\times100\%=7,69\%\)
d) CuSO4 + BaCl2 → BaSO4↓ + CuCl2 (2)
Theo PT2: \(n_{BaSO_4}=n_{CuSO_4}=0,2\left(mol\right)\)
\(\Rightarrow m_{BaSO_4}=0,2\times233=46,6\left(g\right)\)
Vậy m=46,6
Đúng 0
Bình luận (0)
Cho 100 ml dung dịch H2SO4 2M ( D = 1,2 g/m) tác dụng với 100 ml dung dịch BaCl2 1m ( D = 1,32 g/ml )
a) Tính khối lượng chất kết tủa tạo thành
b) Tính nồng độ phần trăm và nồng độ mol của dung dịch tạo thành
\(n_{H_2SO_4}=0.1\cdot2=0.2\left(mol\right)\)
\(m_{dd_{H_2SO_4}}=100\cdot1.2=120\left(g\right)\)
\(n_{BaCl_2}=0.1\cdot1=0.1\left(mol\right)\)
\(m_{dd_{BaCl_2}}=100\cdot1.32=132\left(g\right)\)
\(BaCl_2+H_2SO_4\rightarrow BaSO_4+2HCl\)
\(0.1................0.1.........0.1...............0.2\)
\(\Rightarrow H_2SO_4dư\)
\(m_{BaSO_4}=0.1\cdot233=23.3\left(g\right)\)
\(V_{dd}=0.1+0.1=0.2\left(l\right)\)
\(C_{M_{H_2SO_4\left(dư\right)}}=\dfrac{0.2-0.1}{0.2}=0.5\left(M\right)\)
\(C_{M_{HCl}}=\dfrac{0.2}{0.2}=1\left(M\right)\)
\(m_{\text{dung dịch sau phản ứng}}=120+132-23.3=228.7\left(g\right)\)
\(C\%_{H_2SO_4\left(dư\right)}=\dfrac{0.1\cdot98}{228.7}\cdot100\%=4.28\%\)
\(C\%_{HCl}=\dfrac{0.2\cdot36.5}{228.7}\cdot100\%=3.2\%\)
Đúng 3
Bình luận (1)
Hòa tan 9,3 gam Na2O vào 90,7 gam H2O tạo thành dung dịch A Cho dung dịch A tác dụng với 200 gam dung dịch FeSO4 16% ta thu được kết tủa B và dung dịch C nung kết tủa B đến khối lượng không đổi ta thu được chất rắn D
a) tính nồng độ phần trăm của dung dịch A
b) tính khối lượng chất B và nồng độ phần trăm dung dịch C sau khi bỏ kết tủa B
a/
\(n_{Na_2O}=\dfrac{9,3}{62}=0,15\left(mol\right)\)
\(Na_2O+H_2O\rightarrow2NaOH\)
0,15 0,3 (mol)
\(m_{NaOH}=0,3.40=12\left(g\right)\)
\(m_A=90,7+9,3=100\left(g\right)\)
\(C\%_{NaOH}=\dfrac{12}{100}.100\%=12\%\)
b/
m\(_{FeSO_4}=\dfrac{16.200}{100}=32\left(g\right)\)
\(\rightarrow m_{FeSO_4}=\dfrac{32}{152}=\dfrac{4}{19}\left(mol\right)\)
\(2NaOH+FeSO_4\rightarrow Na_2SO_4+Fe\left(OH\right)_2\downarrow\)
bđ: 0,3 \(\dfrac{4}{19}\) 0 0 (mol)
pư: 0,3 0,15 0,15 0,15 (mol)
dư: 0 \(\dfrac{23}{380}\) (mol)
\(m_{Fe\left(OH\right)_2}=0,15.90=13,5\left(g\right)\)
\(m_C=100+200-13,5=286,5\left(g\right)\)
\(m_{Na_2SO_4}=0,15.142=21,3\left(g\right)\)
\(\rightarrow C\%_{Na_2SO_4}=\dfrac{21,3}{286,5}.100\%\approx7,4\%\)
\(m_{FeSO_4\left(dư\right)}=\dfrac{23}{380}.152=9,2\left(g\right)\)
\(\rightarrow C\%_{FeSO_4\left(dư\right)}=\dfrac{9,2}{286,5}.100\%\approx3,2\%\)
Đúng 2
Bình luận (0)
Cho 160 gam dung dịch CuSO4 nồng độ 10%phản ứng với 150 gam dung dịch NaOH 8%, thu được m gam kết tủa Cu(OH)2và dung dịch X. Tính m và nồng độ phần trăm mỗi chất tan trong dung dịch X
\(n_{CuSO_4}=\dfrac{160.10\%}{160}=0,1\left(mol\right)\)
\(n_{NaOH}=\dfrac{150.8\%}{40}=0,3\left(mol\right)\)
PTHH: CuSO4 + 2NaOH --> Cu(OH)2 + Na2SO4
Xét tỉ lệ: \(\dfrac{0,1}{1}< \dfrac{0,3}{2}\) => CuSO4 hết, NaOH dư
PTHH: CuSO4 + 2NaOH --> Cu(OH)2 + Na2SO4
0,1------>0,2------->0,1------->0,1
=> m = 0,1.98 = 9,8 (g)
\(\left\{{}\begin{matrix}m_{NaOH_{dư}}=\left(0,3-0,2\right).40=4\left(g\right)\\m_{Na_2SO_4}=0,1.142=14,2\left(g\right)\end{matrix}\right.\)
mdd sau pư = 160 + 150 - 9,8 = 300,2 (g)
\(\left\{{}\begin{matrix}C\%_{NaOH_{dư}}=\dfrac{4}{300,2}.100\%=1,33\%\\C\%_{Na_2SO_4}=\dfrac{14,2}{300,2}.100\%=4,73\%\end{matrix}\right.\)
Đúng 5
Bình luận (0)
\(m_{CuSO_4}=\dfrac{160.10}{100}=16\left(g\right)\\ n_{NaOH}=\dfrac{8.150}{100}=12\left(g\right)\\ \rightarrow\left\{{}\begin{matrix}n_{CuSO_4}=\dfrac{16}{160}=0,1\left(mol\right)\\n_{NaOH}=\dfrac{12}{40}=0,3\left(mol\right)\end{matrix}\right.\)
PTHH: 2NaOH + CuSO4 ---> Cu(OH)2 + Na2SO4
LTL: \(0,1< \dfrac{0,3}{2}\rightarrow\) NaOH dư
Theo pt: \(\left\{{}\begin{matrix}n_{NaOH\left(pư\right)}=\dfrac{1}{2}n_{CuSO_4}=2.0,1=0,2\left(mol\right)\\n_{Na_2SO_4}=n_{Cu\left(OH\right)_2}=n_{CuSO_4}=0,1\left(mol\right)\end{matrix}\right.\)
\(\rightarrow m=0,1.98=9,8\left(g\right)\\ m_{dd}=160+150-9,8=300,2\left(g\right)\\ \rightarrow\left\{{}\begin{matrix}C\%_{NaOH\left(dư\right)}=\dfrac{\left(0,3-0,2\right).40}{300,2}=1,33\%\\C\%_{Na_2SO_4}=\dfrac{0,1.142}{300,2}=4,73\%\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Cho 200ml dung dịch axit sunfuric nồng độ 1M và 200ml vào dung dịch Bari clorua nồng độ 0,75M.
a, Viết PTHH ? Chất nào dư sau Phản ứng ? Dư bao nhiêu ?
b, Tính khối lượng kết tủa tạo thành và nồng độ Mol vào dung dịch thu được sau phản ứng (Coi Thể Tích Chất Kết Tủa Không Đáng Kể).
Giúp mình với, mình cần gấp....
Đọc tiếp
Cho 200ml dung dịch axit sunfuric nồng độ 1M và 200ml vào dung dịch Bari clorua nồng độ 0,75M.
a, Viết PTHH ? Chất nào dư sau Phản ứng ? Dư bao nhiêu ?
b, Tính khối lượng kết tủa tạo thành và nồng độ Mol vào dung dịch thu được sau phản ứng (Coi Thể Tích Chất Kết Tủa Không Đáng Kể).
Giúp mình với, mình cần gấp.... ![]()
Ta có: \(\left\{{}\begin{matrix}n_{H_2SO_4}=0,2.1=0,2\left(mol\right)\\n_{BaCl_2}=0,2.0,75=0,15\left(mol\right)\end{matrix}\right.\)
PT: H2SO4 + BaCl2 -> 2HCl + BaSO4
cứ:1..................1...............2.............1 (mol)
vậy:0,15<-----0,15--------->0,3------>0,15(mol)
Chất dư là H2SO4
Số mol H2SO4 dư bằng: 0,2-0,15=0,05(mol)
=> mH2SO4(dư=0,05.98=4,9(g)
b) Chất kết tủa là BaSO4
=> mBaSO4=n.M=0,15.233=34,95(g)
Dung dịch thu được sau phản ứng gồm: HCl(0,3mol) và H2SO4dư(0,05mol)
Vd d sau phản ứng=Vd d H2SO4 + Vd d BaCl2=200+200=400ml=0,4(lít)
=> CM HCl=n/V=0,3/0,4=0,75(M)
CM H2SO4=n/V=0,05/0,4=0,125(M)
Đúng 0
Bình luận (1)
Cho từ từ 27,40 gam Ba vào 100 gam dung dịch H2SO4 9,80%, sau khi phản ứng kết thúc thu được m gam kết tủa, dung dịch X và khí Y. Nồng độ phần trăm của chất tan có trong dung dịch Y là A. 16,49%. B. 13,42%. C. 16,52%. D. 16,44%.
Đọc tiếp
Cho từ từ 27,40 gam Ba vào 100 gam dung dịch H2SO4 9,80%, sau khi phản ứng kết thúc thu được m gam kết tủa, dung dịch X và khí Y. Nồng độ phần trăm của chất tan có trong dung dịch Y là
A. 16,49%.
B. 13,42%.
C. 16,52%.
D. 16,44%.