Xác định khối lượng axit sunfuric có thể thu được từ 16 tấn quặng có chứa 60% FeS2. Biết hiệu suất mỗi phản ứng là 95%.
A. 6,772 tấn
B. 7,448 tấn
C. 13,444 tấn
D. 14,896 tấn
Xác định khối lượng axit sunfuric có thể thu được từ 16 tấn quặng có chứa 60% FeS2. Biết hiệu suất mỗi phản ứng là 95%.
A. 6,772 tấn
B. 7,448 tấn
C. 13,444 tấn
D. 14,896 tấn
Giả sử hiệu suất của phản ứng đều là 100% thì khối lượng H 2 SO 4 sản xuất được từ 1,6 tấn quặng chứa 60% FeS 2 là
A. 1,568 tấn B. 1,725 tấn
C. 1,200 tấn D. 6,320 tấn
Từ 1,6 tấn quặng có chứa 60% FeS2, người ta có thể sán xuất được khối lượng axit sunfuric là bao nhiêu?
A. 1558kg
B. 1578kg
C. 1548kg
D. 1568kg
Từ 3 tấn quặng pirit sắt (chứa 58% \(FeS_2\) về khối lượng), phần còn lại là các tạp chất trơ) điều chế được a tấn axit sunfuric 98%, hiệu suất phản ứng chung của quá trình là 70%
a) Phương trình
b) Tính a
a) 4 FeS2 + 11 O2 -to-> 2 Fe2O3 + 8 SO2
SO2+ 1/2 O2 -to,xt-> SO3
SO3+ H2O -> H2SO4
mFeS2= 0,58. 3=1,74(tấn)
m(H2SO4, lí thuyết)=(98.1,74)/480=0,35525(tấn)
Vì: H=70% -> mH2SO4(TT)=0,35525.70%=0,248675(tấn)
=> mddH2SO4= (0,248675.100)/98=0,25375(tấn)=253,75(kg)
Cho 10 tấn quặng hemantit chứa 60 % Fe2O3.Khối lượng Fe có thể điều chế được là :
(Biết : Fe=56, O=16)
A. 60 tấn
B. 42 tấn
C. 6 tấn
D. 4,2 tấn
\(m_{Fe}=70\%.60\%.10=4,2\left(tấn\right)\)
Trong công nghiệp, axit sunfuric được điều chế từ quặng pirit sắt. Khối lượng dung dịch H 2 S O 4 98% điều chế được từ 1,5 tấn quặng pirit sắt có chứa 80% F e S 2 (hiệu suất toàn quá trình là 80%) là
A. 0,80 tấn
B. 1,60 tấn
C. 1,25 tấn
D. 2,00 tấn
Trong công nghiệp, axit sunfuric được điều chế từ quang pirit sắt. Khối lượng H2SO4 điều chế được từ 1,5 tấn quặng pirit sắt có chứa 80% FeS2 ( hiệu suất toàn quá trình là 80%) là:
A. 1,568 tấn
B. 1,96 tấn
C. 1,25 tấn
D. 2,00 tấn
Đáp án A.
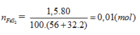
FeS2 → 2H2SO4 (Bảo toàn S)
0,01 → 0,02 (mol)
Do hiệu suất là 80%
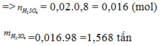
Có một loại quặng pirit chứa 96% FeS2. Nếu mỗi ngày nhà máy sản xuất 100 tấn axit sunfuric 98% thì cần m tấn quặng pirit trên và biết hiệu suất của cả quá trình sản xuất H2SO4 là 90%. Gía trị của m là:
A. 69,44 tấn
B. 68,44tấn
C. 67,44 tấn
D. 70,44tấn
từ 1,6 tấn quặng pirit sắt có chứa 60% FeS2 có thể sản xuất được bao nhiêu tấn axit H2SO4 ? Biết hiệu suất của quá trình phản ứng là 80% .
mFeS2=1,6.10^6.60%=960000g
=>nFeS2=960000/120=8000 mol
Sơ đồ cả quá trình tạo H2SO4
FeS2 =>2SO2 =>2SO3 =>2H2SO4
8000 mol =>16000 mol
Theo sơ đồ bảo toàn ngtố S ta có nH2SO4=8000.2.80%=12800 mol
=>mH2SO4=12800.98=1254400g=1,2544 tấn