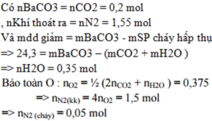Đốt cháy 6,4g C và 6,72 lít O2(dktc) sản phẩm là CO2 tìm khối lượng của chất còn lại dư và thể tích khí CO2 thu được.

Những câu hỏi liên quan
đốt cháy 4,8 g cacbon bằng 6,72 lít khí oxi thu được sản phẩm sau phản ứng là CO2 . Tìm khối lượng chất còn dư và thể tích khí CO2 thu được.
nC=4,8/12=0,4(mol)
nO2=6,72/22,4=0,3(mol)
PTHH: C+ O2 -to-> CO2
Ta có: 0,4/1 > 0,3/1
=> C dư, O2 hết, tính theo nO2
=> nCO2=nC(p.ứ)=nO2=0,3(mol)
=>nC(dư)=0,4-0,3=0,1(mol)
=>mC(dư)=0,1.12=1,2(g)
V(CO2,đktc)=V(O2,đktc)=6,72(l) (Số mol tỉ lệ thuận thể tích)
Đúng 5
Bình luận (0)
Đốt cháy hoàn toàn một hợp chất hữu cơ X (C, H, N) bằng lượng không khí vừa đủ (gồm 1/5 thể tích O2, còn lại là N2) được khí CO2 , H2O và N2. Cho toàn bộ sản phẩm cháy qua bình đựng dung dịch Ba(OH)2 dư thấy có 39,4 gam kết tủa, khối lượng dung dịch giảm đi 24,3 gam. Khí thoát ra khỏi bình có thể tích 34,72 lít (đktc). Biết dX/O2 2. CTPT của X là A. C2H4N2 B. C2H8N C. C2H7N2 D. C2H7N
Đọc tiếp
Đốt cháy hoàn toàn một hợp chất hữu cơ X (C, H, N) bằng lượng không khí vừa đủ (gồm 1/5 thể tích O2, còn lại là N2) được khí CO2 , H2O và N2. Cho toàn bộ sản phẩm cháy qua bình đựng dung dịch Ba(OH)2 dư thấy có 39,4 gam kết tủa, khối lượng dung dịch giảm đi 24,3 gam. Khí thoát ra khỏi bình có thể tích 34,72 lít (đktc). Biết dX/O2< 2. CTPT của X là
A. C2H4N2
B. C2H8N
C. C2H7N2
D. C2H7N
Đốt cháy hoàn toàn một hợp chất hữu cơ X (C, H, N) bằng lượng không khí vừa đủ (gồm 1/5 thể tích O2, còn lại là N2) được khí CO2 , H2O và N2. Cho toàn bộ sản phẩm cháy qua bình đựng dung dịch Ba(OH)2 dư thấy có 39,4 gam kết tủa, khối lượng dung dịch giảm đi 24,3 gam. Khí thoát ra khỏi bình có thể tích 34,72 lít (đktc). Biết dX/O2 2. CTPT của X là A. C2H7N B. C3H9N C. C3H6N2 D. C2H4N2
Đọc tiếp
Đốt cháy hoàn toàn một hợp chất hữu cơ X (C, H, N) bằng lượng không khí vừa đủ (gồm 1/5 thể tích O2, còn lại là N2) được khí CO2 , H2O và N2. Cho toàn bộ sản phẩm cháy qua bình đựng dung dịch Ba(OH)2 dư thấy có 39,4 gam kết tủa, khối lượng dung dịch giảm đi 24,3 gam. Khí thoát ra khỏi bình có thể tích 34,72 lít (đktc). Biết dX/O2 < 2. CTPT của X là
A. C2H7N
B. C3H9N
C. C3H6N2
D. C2H4N2
bài 1: đốt cháy 3,92 (lít) ch4 (đktc) trong bình chứa 3,84 (gam) oxi. sản phẩm tạo thành là co2 và h2o. a) viết pthh xảy ra b) sau phản ứng, chất nào còn dư ? khối lượng dư là bao nhiêu gam ? c) cho thể tích khí co2 thu được ở trên vào dd naoh thì thu được h2o và chất tan na2co3. tính khối lượng na2co3?
$a) CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O$
b) $n_{CH_4} = \dfrac{3,92}{22,4} = 0,175(mol)$
$n_{O_2} = \dfrac{3,84}{32} = 0,12(mol)$
Ta thấy : $n_{CH_4} : 1 > n_{O_2} : 2$ nên $CH_4$ dư
$n_{CH_4\ pư} = \dfrac{1}{2}n_{O_2} = 0,06(mol)$
$\Rightarrow m_{CH_4\ dư} = (0,175 - 0,06).16 = 1,84(gam)$
c) $2NaOH + CO_2 \to Na_2CO_3 + H_2O$
Theo PTHH :
$n_{Na_2CO_3} = n_{CO_2} = \dfrac{1}{2}n_{CH_4} = 0,06(mol)$
$m_{Na_2CO_3} = 0,06.106 = 6,36(gam)$
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 48 gam Cacbon (C) trong 44,8 lít oxi (O2) ở đktc thu được sản phẩm là khí cacbonđioxit ( CO2) a. Xác định chất dư, chất hết trong phản ứng trên.b. Tính khối lượng của sản phẩm thu được sau phản ứng. (Cho C 12, H 1, O 16) giúp tui vs ạ
Đọc tiếp
Đốt cháy hoàn toàn 48 gam Cacbon (C) trong 44,8 lít oxi (O2) ở đktc thu được sản phẩm là khí cacbonđioxit ( CO2)
a. Xác định chất dư, chất hết trong phản ứng trên.
b. Tính khối lượng của sản phẩm thu được sau phản ứng.
(Cho C = 12, H = 1, O = 16)
giúp tui vs ạ
\(a,m_C=48\left(g\right)\rightarrow n_C=\dfrac{m_C}{M_C}=\dfrac{48}{12}=4\left(mol\right)\)
\(V_{O_2}=44,8\left(l\right)\rightarrow n_{O_2}=\dfrac{V_{O_2}}{22,4}=\dfrac{44,8}{22,4}=2\left(mol\right)\)
\(PTHH:C+O_2\underrightarrow{t^o}CO_2\)
\(pt:\) \(1mol\) \(1mol\)
\(đb:\) \(4mol\) \(2mol\)
Xét tỉ lệ:
\(\dfrac{n_{C\left(đb\right)}}{n_{C\left(pt\right)}}=\dfrac{4}{1}=4>\dfrac{n_{O_2\left(đb\right)}}{n_{O_2\left(pt\right)}}=\dfrac{2}{1}=2\)
\(\Rightarrow\) \(O_2\) hết, \(C\) dư.
\(b,PTHH:C+O_2\underrightarrow{t^o}CO_2\)
\(pt:\) \(1mol\) \(1mol\)
\(đb:\) \(2mol\) \(2mol\)
\(\Rightarrow m_{CO_2}=n_{CO_2}.M_{CO_2}=2.\left(1.C+2.O\right)=2.\left(1.12+2.16\right)=88\left(g\right)\)
Đúng 3
Bình luận (0)
\(a.n_C=\dfrac{48}{12}=4\left(mol\right);n_{O_2}=\dfrac{44,8}{22,4}=2\left(mol\right)\\ C+O_2\xrightarrow[t^0]{}CO_2\)
Theo pt:\(\dfrac{4}{1}>\dfrac{2}{1}\Rightarrow C\) dư, O2 pư hết
\(b.C+O_2\xrightarrow[t^0]{}CO_2\\ \Rightarrow n_{CO_2}=n_{O_2}=2mol\\ m_{CO_2}=2.44=88\left(g\right)\)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn a gam một amin (no, đơn chức, mạch hở) cần dùng 8,4 lít khí O2 (ở đktc) thu được khí CO2 và 6,3 gam hơi nước và khí N2. Sục sản phẩm cháy vào bình X đựng dung dịch nước vôi trong (dư), chỉ còn lại duy nhất một chất khí thoát ra. Khối lượng bình X tăng m gam. Giá trị m là A. 8,8. B. 18,3. C. 15,1. D. 20,0.
Đọc tiếp
Đốt cháy hoàn toàn a gam một amin (no, đơn chức, mạch hở) cần dùng 8,4 lít khí O2 (ở đktc) thu được khí CO2 và 6,3 gam hơi nước và khí N2. Sục sản phẩm cháy vào bình X đựng dung dịch nước vôi trong (dư), chỉ còn lại duy nhất một chất khí thoát ra. Khối lượng bình X tăng m gam. Giá trị m là
A. 8,8.
B. 18,3.
C. 15,1.
D. 20,0.
Chọn đáp án C
Vì amin no đơn chức mạch hở ⇒ CTTQ là CnH2n+3N
Ta có: CnH2n+3N + 6 n + 3 4 O2 → (n + 1,5) H2O + nCO2 + 1 2 N2
⇒ nO2 × (n + 1,5) = nH2O × (6n + 3) ÷ 4
⇔ 0,375 × (n + 1,5) = 0,35 × (1,5n + 0,75)
⇔ n = 2 ⇒ Amin có ctpt là C2H7N
⇒ nCO2 = 0,2 ⇒ mCO2 = 8,8 gam.
+ Mà mBình ↑ = mCO2 + mH2O = 8,8 + 6,3 = 15,1 gam
⇒ Chọn C
Đúng 0
Bình luận (0)
Câu 1: Đốt cháy 4,8 g cacbon bằng 7,437 lít khí oxi (đkc) thu được sản phẩm sau phản ứng là CO2. Cho biết chất nào còn dư sau phản ứng và dư bao nhiêu gam. Tính thể tích khí CO2 thu được (đkc)Câu 2: Cho 2,4 g Mg tác dụng với 9,916 lít Cl2 thu được MgCl2. Cho biết chất nào còn dư sau phản ứng và dư bao nhiêu gam. Tính Khối lượng MgCl2 thu được.
Đọc tiếp
Câu 1: Đốt cháy 4,8 g cacbon bằng 7,437 lít khí oxi (đkc) thu được sản phẩm sau phản ứng là CO2. Cho biết chất nào còn dư sau phản ứng và dư bao nhiêu gam. Tính thể tích khí CO2 thu được (đkc)
Câu 2: Cho 2,4 g Mg tác dụng với 9,916 lít Cl2 thu được MgCl2. Cho biết chất nào còn dư sau phản ứng và dư bao nhiêu gam. Tính Khối lượng MgCl2 thu được.
Câu 1 :
$n_C = \dfrac{4,8}{12} = 0,4(mol) ; n_{O_2} = \dfrac{7,437}{24,79} = 0,3(mol)$$
$C + O_2 \xrightarrow{t^o} CO_2$
Ta thấy :
$n_C : 1 > n_{O_2} : 1$ nên C dư
$n_{C\ pư} = n_{O_2} = 0,3(mol) \Rightarrow m_{C\ dư} = (0,4 - 0,3).12 = 1,2(gam)$
$\Rightarorw V_{CO_2} = V_{O_2} = 7,437(lít)$
Câu 2 :
$n_{Mg} = \dfrac{2,4}{24} = 0,1(mol)$
$n_{Cl_2} = \dfrac{9,916}{24,79} = 0,4(mol)$
$Mg + Cl_2 \xrightarrow{t^o} MgCl_2$
Ta thấy :
$n_{Mg} : 1 < n_{Cl_2} : 1$ nên $Cl_2$ dư
$n_{Cl_2\ pư} = n_{Mg} = 0,1(mol) \Rightarrow m_{Cl_2\ dư} = (0,4 - 0,1).71 = 21,3(gam)$
$n_{MgCl_2}= n_{Mg} = 0,1(mol) \Rightarrow m_{MgCl_2} = 0,1.95 = 9,5(gam)$
Đúng 2
Bình luận (0)
Đốt chát 6,2 g photpho trong bình chưa 6,72 lít khí O2 (đktc)
a) Chất nào còn dư, và dư bao nhiêu?
b) Tính khối lượng sản phẩm thu được?
a)
\(n_P = \dfrac{6,2}{31} = 0,2(mol) ; n_{O_2} = \dfrac{6,72}{22,4} = 0,3(mol)\\ 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\)
Ta thấy :
\(\dfrac{n_P}{4} = 0,05 < \dfrac{n_{O_2}}{5} = 0,06\) nên O2 dư.
\(n_{O_2\ pư} = \dfrac{5}{4}n_P = 0,25(mol)\\ \Rightarrow m_{O_2\ dư} = (0,3 - 0,25).32 = 1,6(gam)\)
b)
\(n_{P_2O_5} = \dfrac{n_P}{2} = 0,1(mol)$\\ m_{P_2O_5} = 0,1.142 = 14,2(gam)\)
Đúng 4
Bình luận (0)
Đốt cháy hoàn toàn a gam cacbohirat X cần 6,72 lít
O
2
(đktc) thu được
C
O
2
và
H
2
O
. Hấp thụ hết sản phẩm cháy bằng dung dịch nước vôi trong dư, thấy khối lượng dung dịch vôi trong giảm 11,4 gam. X thuộc loại : A. Polisaccarit. B. Monosaccarit. C. Trisaccarit. D. Đissaccarit.
Đọc tiếp
Đốt cháy hoàn toàn a gam cacbohirat X cần 6,72 lít O 2 (đktc) thu được C O 2 và H 2 O . Hấp thụ hết sản phẩm cháy bằng dung dịch nước vôi trong dư, thấy khối lượng dung dịch vôi trong giảm 11,4 gam. X thuộc loại :
A. Polisaccarit.
B. Monosaccarit.
C. Trisaccarit.
D. Đissaccarit.