Những chất nào trong số các chất sau được dùng để điều chế oxi trong phòng thí nghiệm?
a) Fe3O4.
b) KClO3.
c) KMnO4.
d) CaCO3.
e) Không khí.
g) H2O.
Câu 2 (0,5đ): Hóa chất nào được dùng để điều chế khí O2 trong phòng thí nghiệm.
A. Nước, không khí. B. CaCO3, H2O.
C. KMnO4, KClO3 D. Sự quang hợp của cây xanh.
Câu 18: Những chất được dùng để điều chế oxi trong phòng thí nghiệm là: |
A. KClO3 và CaCO3
B. KMnO4 và H2O |
C. KMnO4 và không khí
D. KClO3 và KMnO4
Câu 19: Điều khẳng định nào sau đây là đúng ? Không khí là :
A. Một hỗn hợp.
B. Một hợp chất.
C.Một đơn chất.
D. Một chất tinh khiết.
Câu 20: Chỉ ra tên gọi đúng của hợp chất Al2O3
A. Sắt oxit.
B. Sắt (III) oxit.
C. Nhôm oxit.
D. Nhôm (III) oxit.
Câu 21: Chỉ ra công thức của oxit viết sai
A. Mg0.
B. P205.
C. FeO2.
D. ZnO.
Câu 22: Phản ứng hóa học không xảy ra sự oxi hóa là: A. 4NH3 + 502 → 4NO + 6H2O
B. O2 + 2H2 → 2H2O C. Ca + O2 + CaO
D. NaOH + HCl → NaCl + H2O
Câu 23: Khi nhiệt phân 49 g kali clorat (KClO3). Thể tích khí oxi sinh ra (ở đktc) là :
A. 3,361.
B. 6,721.
C. 13,441.
D. 22,41.
Câu 24: Khí Oxi hóa lỏng ở nhiệt độ nào sau đây:
A. Ở -183 °C
B. Ở -196 °C
C. Ở 183 °C
D. Ở 196°C II.
TỰ LUẬN:
Câu 1:Hoàn thành các PTHH của các phản ứng sau và chỉ ra phản ứng nào là phản ứng hóa hợp? phản ứng nào là phản ứng phân hủy?
a. KNO3 , KNO2 + O2
b. Cu + Cl210, CuCl2
c. Na2CO3 + CO2 + H2O → NaHCO
d. CaCO3 _ > CaO + CO2
Câu 2: (3 đ) a. Tính thể tích khí oxi thu được (ở đktc) khi nhiệt phân hoàn toàn 47,4 gam KMnO4 .
b. Nếu dùng 6,75 gam nhôm cho tác dụng với lượng oxi thu được ở phản ứng trên thì khi phản | ứng kết thúc chất nào còn dư? Khối lượng dư là bao nhiêu gam?
Câu 3:(2,0 điểm) Có 3 bình không nhãn chứa các khí sau: O, N, CO2. Bằng phương pháp hóa học em hãy nhận biết các khí trên?
Câu 4: (3,0 điểm)
Đốt cháy hoàn toàn 126 g sắt trong bình chứa khí O2. a. Tính thể tích khí O2 (ở đktc) đã tham gia phản ứng trên. b. Tính khối lượng KClOg cần dùng để khi phân huỷ thì thu được một thể tích khí O2 (ởđktc) bằng với thể tích khí 0 đã sử dụng ở phản ứng trên.
Câu 18: Những chất được dùng để điều chế oxi trong phòng thí nghiệm là: |
A. KClO3 và CaCO3
B. KMnO4 và H2O |
C. KMnO4 và không khí
D. KClO3 và KMnO4
Câu 19: Điều khẳng định nào sau đây là đúng ? Không khí là :
A. Một hỗn hợp.
B. Một hợp chất.
C.Một đơn chất.
D. Một chất tinh khiết.
Câu 20: Chỉ ra tên gọi đúng của hợp chất Al2O3
A. Sắt oxit.
B. Sắt (III) oxit.
C. Nhôm oxit.
D. Nhôm (III) oxit.
Câu 21: Chỉ ra công thức của oxit viết sai
A. Mg0.
B. P205.
C. FeO2.
D. ZnO.
Câu 22: Phản ứng hóa học không xảy ra sự oxi hóa là: A. 4NH3 + 502 → 4NO + 6H2O
B. O2 + 2H2 → 2H2O C. Ca + O2 + CaO
D. NaOH + HCl → NaCl + H2O
Câu 23: Khi nhiệt phân 49 g kali clorat (KClO3). Thể tích khí oxi sinh ra (ở đktc) là :
A. 3,361.
B. 6,721.
C. 13,441.
D. 22,41.
Câu 24: Khí Oxi hóa lỏng ở nhiệt độ nào sau đây:
A. Ở -183 °C
B. Ở -196 °C
C. Ở 183 °C
D. Ở 196°C II.
5: Phản ứng nào dưới đây là phản ứng hóa hợp?
A. CuO + H2_10> Cu +H2O
B. CO2 + Ca(OH)21° > CaCO3 + H2O
C. 2KMnO4 10 KMnO4 + MnO2 + O2
D. CaO + H200 Ca(OH)2
Câu 6. Những chất được dùng để điều chế oxi trong phòng thí nghiệm là
A. KClO3 và KMnO4 .
B. KMnO4 và H2O.
C. KClO3 và CaCO3 .
D. KMnO4 và không khí.
Câu 7: Nhóm công thức nào sau đây biểu diễn toàn oxit?
A. CuO, CaCO3, SO3
B. N2O5 ; Al2O3 ; SiO2
C. FeO; KC1, P2O5
D. CO2 ; H2SO4; MgO
Câu 8: Phản ứng hoá học có xảy ra sự oxi hoá là
A. 4NH3 + 502 + 4NO + 6H2O
B. Na2O + H2O → 2NaOH
C. CaCO3 +CaO + CO2
D. Na2SO4 + BaCl2 → BaSO4 + 2NaCl
Câu 9: Đốt cháy hoàn toàn 2,4 gam Mg trong khí oxi dư thu được khối lượng MgO làm
A. 4 gam.
B. 4,3 gam.
C. 4,6 gam.
D. 4.9 gam.
Câu 10: Khối lượng KMnO4 cần dùng để điều chế 1,12 lít khí oxi là
A. 7,9 gam.
B. 15,8 gam.
C. 3,95 gam.
D. 14,2 gam.
Câu 11: Người ta không nên dùng nước để dập tắt đám cháy bằng xăng dầu vì
A. xăng dầu không tan trong nước, nhẹ hơn nước.
B. xăng dầu cháy mạnh trong nước.
C. xăng dầu nặng hơn nước.
D. xăng dầu cháy mạnh hơn khi có nước.
Câu 12: Đốt cháy hoàn toàn 3,1 gam P trong bình chứa 5,6 lít khí oxi thu được khối lượng P2O5 là
A.9,1 gam. B. 8,1 gam. C. 7,1 gam. D. 6,1 gam.
5: Phản ứng nào dưới đây là phản ứng hóa hợp?
A. CuO + H2_10> Cu +H2O
B. CO2 + Ca(OH)21° > CaCO3 + H2O
C. 2KMnO4 10 KMnO4 + MnO2 + O2
D. CaO + H200 Ca(OH)2
Câu 6. Những chất được dùng để điều chế oxi trong phòng thí nghiệm là
A. KClO3 và KMnO4 .
B. KMnO4 và H2O.
C. KClO3 và CaCO3 .
D. KMnO4 và không khí.
Câu 7: Nhóm công thức nào sau đây biểu diễn toàn oxit?
A. CuO, CaCO3, SO3
B. N2O5 ; Al2O3 ; SiO2
C. FeO; KC1, P2O5
D. CO2 ; H2SO4; MgO
Câu 8: Phản ứng hoá học có xảy ra sự oxi hoá là
A. 4NH3 + 502 + 4NO + 6H2O
B. Na2O + H2O → 2NaOH
C. CaCO3 +CaO + CO2
D. Na2SO4 + BaCl2 → BaSO4 + 2NaCl
Câu 9: Đốt cháy hoàn toàn 2,4 gam Mg trong khí oxi dư thu được khối lượng MgO làm
A. 4 gam.
B. 4,3 gam.
C. 4,6 gam.
D. 4.9 gam.
Câu 10: Khối lượng KMnO4 cần dùng để điều chế 1,12 lít khí oxi là
A. 7,9 gam.
B. 15,8 gam.
C. 3,95 gam.
D. 14,2 gam.
Câu 11: Người ta không nên dùng nước để dập tắt đám cháy bằng xăng dầu vì
A. xăng dầu không tan trong nước, nhẹ hơn nước.
B. xăng dầu cháy mạnh trong nước.
C. xăng dầu nặng hơn nước.
D. xăng dầu cháy mạnh hơn khi có nước.
Câu 12: Đốt cháy hoàn toàn 3,1 gam P trong bình chứa 5,6 lít khí oxi thu được khối lượng P2O5 là
A.9,1 gam. B. 8,1 gam. C. 7,1 gam. D. 6,1 gam.
Câu 21: Các chất dùng để điều chế Oxi trong phòng thí nghiệm là
A. KClO3 B. KMnO4 C. CaCO3 D. KClO3 và KMnO4
Câu 22: Tổng hệ số của chất tham gia và sản phẩm là
2KClO3 toà 2KCl + 3O2
A. 2&5 B. 5&2 C. 2&2 D. 2&3
Câu 23: Có những cách nào điều chế oxi trong công nghiệp
A. Dùng nguyên liệu là không khí B. Dùng nước làm nguyên liệu
C. Dùng kim loại và axit D. Dùng nước và không khí.
Câu 24: Số sản phẩm tạo thành của phản ứng phân hủy là
2 B. 3 C. 2 hay nhiều sản phẩm D. 1
Câu 25: Nhiệt phân 12,25 g KClO3 thấy có khí bay lên. Tính thể tích của khí ở đktc
A. 4,8 l B. 3,36 l C. 2,24 l D. 3,2 l
21.
$2KClO_3\xrightarrow{t^o,MnO_2}2KCl+3O_2$
$2KMnO_4\xrightarrow{t^o}K_2MnO_4+MnO_2+O_2$
$\to D$
22.
$2KClO_3\xrightarrow{t^o}2KCl+3O_2$
$\to A$
23. $D$
24. $C$
25.
$n_{KClO_3}=\frac{12,25}{122,5}=0,1(mol)$
$2KClO_3\xrightarrow{t^o,MnO_2}2KCl+3O_2$
Theo PT: $n_{O_2}=\frac{3}{2}n_{KClO_3}=0,15(mol)$
$\to V_{O_2}=0,15.22,4=3,36(l)$
$\to B$
Câu 1: Nhóm công thức nào sau đây biểu diễn toàn Oxit
A. CuO, CaCO3, SO3 B. FeO, KCl, P2O5 C. N2O5 , Al2O3 , SiO2 , HNO3 D. CO2, SO2,
MgO
Câu 2: Những chất được dùng để điều chế oxi trong phòng thí nghiệm là
A. KClO3 và KMnO4 . B. KMnO4 và H2O. C. KClO3 và CaCO3 D. KMnO4 và không khí.
Câu 3: Chất khí nào nhẹ nhất trong các chất khí sau:
A. CO2 B. SO2 C. O2 D. H2S
Câu 4: Nguyên liệu dùng để điều chế khí hiđro trong phòng thí nghiệm là:
A. Zn và H2O B. Fe và KCl C. O2 và H2 D. Al và HCl
Câu 5: Khí Hidro được bơm vào khinh khí cầu, bóng thám không vì Hidro là khí
A. không màu. B. khí nhẹ nhất trong các loại khí.
C. có tác dụng với Oxi trong không khí. D. ít tan trong nước.
Câu 6: Cho a gam sắt tác dụng hết với dung dịch H2SO4 thu được FeSO4 và 4,48 lít khí H2
ở (đktc). Giá trị của a là A. 11,2 g B. 5,6g C. 22,4g D. 1,12g
Câu 7: Chất nào sau đây có thể tác dụng với oxi để tạo thành oxit bazơ?
A. P B. S C. Fe D. Si
Câu 8: Dãy chất nào sau đây toàn là bazơ
A. HBr, Mg(OH)2, KOH, HCl B. Ca(OH)2, Cu(OH)2 , Fe(OH)3, KOH C. Fe(OH)3 , CaCO3, HCl, ZnS D. Fe(OH)2, KCl, NaOH, HBr
Câu 9: Tất cả các kim loại trong dãy nào sau đây tác dụng được với H2O ở nhiệt độ thường?
A. Fe, Zn, Li, Sn B. Cu, Pb, Rb, Ag.
C. K, Na, Ca, Ba. D. Al, Hg, Cs, Sr Câu 10: Nhóm các chất nào sau đây đều là axit?
A. HCl, HNO3, KOH, KCl. B. HNO3, CO2, H2SO4, NaOH.
C. HCl, HNO3, H2SO4. D. HCl, HNO3, H2SO4, NaCl.
Câu 11: Trong các chất sau: Na, P2O5, CaO, Na2O. Nước tác dụng được với chất nào tạo ra axit?
A. Na B. P2O5 C. CaO D. Na2O
Câu 12: Dãy chất nào sau đây toàn là muối
A. NaHCO3, MgCO3 ,BaCO3 B. NaCl, HNO3 , BaSO4 C. NaOH, ZnCl2 , FeCl2 D. NaHCO3, MgCl2 , CuO Câu 13: Phát biểu nào sau đây về oxi là không đúng?
A. Oxi là phi kim hoạt động rất mạnh, nhất là ở nhiệt độ cao.
B. Oxi tạo oxit axit với hầu hết các kim loại.
C. Oxi không có màu và không có mùi.
D. Oxi cần thiết cho sự sống.
Câu 14: Phản ứng nào sau đây là phản ứng thế ?
A. 4P + 5O2 2P2O5 B. 2Al + 6HCl 2AlCl3 + 3H2 C. CaCO3 to CaO + CO2 D. C + O2 to CO2
Câu 15: . Hỗn hợp khí hidro và khí oxi là hỗn hợp nổ. Hỗn hợp này nổ mạnh nhất ở tỉ lệ về thể tích là bao nhiêu:

1d
2a
3c
4d
5b
6a
7c
8b
9c
10c
11b
12a
13b
14b
15 2:1
t đoán z nha![]()
Trong những chất sau, những chất nào được dùng để điều chế khí oxi? Viết phương trình phản ứng và nêu điều kiện phản ứng: C u S O 4 ; K C l O 3 ; C a C O 3 ; K M n O 4 ; H 2 O ; K 2 S O 4 ; HgO
Các chất được dùng để điều chế oxi: K C l O 3 ; K M n O 4 ; H 2 O ; HgO.
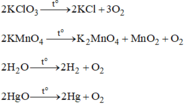
Bài 1: Những chất nào trong số những chất sau được dùng để điều chế khí oxi trong phòng thí nghiệm
a) \(Fe_3O_4\) b) \(KCLO_3\) c)\(KMnO_4\) d) \(CaCO_3\) e) Không khí g) \(H_2O\)
Bài 2: Sự khác nhau giữa phản ứng phân hủy và phản ứng hóa hợp ? Dẫn ra hai thí dụ để minh họa .
Bài 3: Nung đá vôi ( thành phần chính là \(CaCO_3\) ) được vôi sống CaO và khí cacbonic \(CO_2\)
a, Viết phương trình hóa học của phản ứng.
b, Phản ứng nung vôi thuộc loại pahrn ứng hóa học nào ? Vì sao?
BÀI 4: TRong phòng thí nghiệm , người ta điều chế oxit sắt từ \(Fe_3O_4\) baengf cách dùng oxi oxi hóa sắt ở nhiệt độ cao .
a, Tính số gam sắt và số gam khí oxi cần dùng để điều chế được 2,32g oxit sắt từ.
b, Tính số gam kali pemanganat \(KMnO_4\) cần dùng để có được lượng oxi dùng cho phản ứng trên.
Mn giúp với mai phải nộp rồi!
Bài 1. b) và c)
Bài 2. # Sự khác nhau:
- Chất tham gia:
+ Phản ứng phân hủy: một chất
+ Phản ứng hóa hợp: hai hay nhiều chất
- Chất tạo thành:
+ Phản ứng phân hủy: hai hay nhiều chất
+ Phản ứng hóa hợp: một chất
# Thí dụ minh họa:
- Phản ứng phân hủy:
2\(KMnO_4\) ---> \(K_2MnO_4\) + \(MnO_2\) + \(O_2\)
2\(KClO_3\) ---> 2KCl + 3\(O_2\)
- Phản ứng hóa hợp:
2Mg + \(O_2\) ---> 2MgO
2Fe + 3\(Cl_2\) --->\(2FeCl_3\)
Bài 3. a. \(CaCO_3\) ---> CaO + \(CO_2\) (Lập và cân bằng phương trình)
b. Phản ứng nung vôi thuộc loại phản ứng phân hủy. Vì có một chất tham gia và hai chất tạo thành
Bài 4. 3Fe + 2\(O_2\) ---> \(Fe_3O_4\) (Lập và cân bằng phương trình)
0,03 mol 0,02 mol 0,01 mol
a. + Số mol của \(Fe_3O_4\)
\(n_{Fe_3O_4}\) = \(\dfrac{m}{M}\) = \(\dfrac{2,32}{232}\) = 0,01 (mol)
+ Số g của Fe:
\(m_{Fe}\) = n . M = 0,03 . 56 = 1,68 (g)
+ Số g của \(O_2\)
\(m_{O_2}\) = n . M = 0,02 . 32 = 0,64 (g)
b. 2\(KMnO_4\) ---> \(K_2MnO_4\) + \(MnO_2\) + \(O_2\) (Lập và cân bằng phương trình)
0,04 mol 0,02 mol 0,02 mol 0,02 mol
Số g của \(KMnO_4\)
\(m_{KMnO_4}\) = n . M = 0,04 . 158 = 6,32 (g)
________________________________________
Có gì không đúng nhắn mình nhé :))
Cho các chất có CTHH: KMnO4, CaO, Na, Fe, KClO3, Fe2O3, SO3, CO, K2O, Zn, Ba, P2O5, K, Na2O, CuO. Hãy cho biết:
a) Những chất nào tác dụng được với nước ở nhiệt độ thường?
b) Chất nào dùng để điều chế khí oxi trong phòng thí nghiệm?
c) Những chất nào tác dụng được với HCl hoặc H2SO4 (1) để điều chế H2 trong PTN? Viết PTHH, ghi rõ điều kiện phản ứng (nếu có) và cho biết chúng thuộc loại phản ứng nào?
Trong phòng thí nghiệm, khí clo thường được điều chế bằng cách oxi hóa hợp chất nào sau đây:
A. NaCl.
B. HCl.
C. KClO3.
D. KMnO4.
Đáp án B. HCl đúng.
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O