Biết rằng canxi oxit (vôi sống) CaO hóa hợp với nước tạo ra canxi hidroxit ( vôi tôi) C a O H 2 , chất này tan được trong nước, cứ 56g CaO hóa hợp vừa đủ với 18g H 2 O . Bỏ 2,8g CaO vào trong một cốc lớn chứa 400ml nước tạo ra dung dịch C a O H 2 , còn gọi là nước vôi trong. Tính khối lượng của dung dịch C a O H 2 , giả sử nước trong cốc là nước tinh khiết

Những câu hỏi liên quan
Biết rằng canxi oxit (vôi sống) CaO hóa hợp với nước tạo ra canxi hidroxit ( vôi tôi)
C
a
O
H
2
, chất này tan được trong nước, cứ 56g CaO hóa hợp vừa đủ với 18g
H
2
O
. Bỏ 2,8g CaO vào trong một cốc lớn chứa 400ml nước tạo ra dung dịch
C
a
O
H...
Đọc tiếp
Biết rằng canxi oxit (vôi sống) CaO hóa hợp với nước tạo ra canxi hidroxit ( vôi tôi) C a O H 2 , chất này tan được trong nước, cứ 56g CaO hóa hợp vừa đủ với 18g H 2 O . Bỏ 2,8g CaO vào trong một cốc lớn chứa 400ml nước tạo ra dung dịch C a O H 2 , còn gọi là nước vôi trong. Tính khối lượng của canxi hidroxit.
Ta có:
Cứ 56g CaO hóa hợp vừa đủ với 18g H 2 O .
Vậy 2,8g CaO hóa hợp vừa đủ với x(g) H 2 O .
→ x = (2,8 x 18)/56 = 0,9(g)
Công thức khối lượng của phản ứng:
m C a O + m H 2 O = m C a O H 2
2,8 + 0,9 = 3,7 (g)
Vậy khối lượng của C a O H 2 là 3,7g.
Đúng 0
Bình luận (0)
Biết rằng canxi oxit (vôi sống) CaO hóa hợp với nước tạo ra canxi hidroxit (vôi tôi) Ca(OH)2, chất này tan được trong nước, cứ 56 gam CaO hóa hợp vừa đủ với 18 gam H2O. Bỏ 2,8 gam CaO vào trong một cốc lớn chứa 400 ml nước tạo ra dung dịch Ca(OH) 2, còn gọi là nước vôi trong.a/ Tính khối lượng của canxi hiđroxit thu được.b/ Tính khối lượng của dung dịch Ca(OH)2, giả sử nước trong cốc là nước tinh khiết
Đọc tiếp
Biết rằng canxi oxit (vôi sống) CaO hóa hợp với nước tạo ra canxi hidroxit (vôi tôi) Ca(OH)2, chất này tan được trong nước, cứ 56 gam CaO hóa hợp vừa đủ với 18 gam H2O. Bỏ 2,8 gam CaO vào trong một cốc lớn chứa 400 ml nước tạo ra dung dịch Ca(OH) 2, còn gọi là nước vôi trong.
a/ Tính khối lượng của canxi hiđroxit thu được.
b/ Tính khối lượng của dung dịch Ca(OH)2, giả sử nước trong cốc là nước tinh khiết
a)
\(n_{CaO}=\dfrac{2,8}{56}=0,05\left(mol\right)\)
PTHH: CaO + H2O --> Ca(OH)2
0,05------------>0,05
=> mCa(OH)2 = 0,05.74 = 3,7 (g)
b) dH2O = 1 g/ml
=> mH2O = 400.1 = 400 (g)
mdd = 2,8 + 400 = 402,8 (g)
Đúng 2
Bình luận (0)
Biết rằng canxi oxit (CaO – vôi sống) hóa hợp với nước tạo ra canxi hiđroxit (Ca(OH)2 – vôi tôi), chất này tan được trong nước, cứ 112 gam CaO hóa hợp vừa đủ với 36 gam H2O. Bỏ 5,6 gam CaO vào trong một cốc lớn chứa 400 ml nước tạo ra dung dịch Ca(OH)2, còn gọi là nước vôi trong.(a) Tính khối lượng của canxi hiđroxit.(b) Tính khối lượng của dung dịch Ca(OH)2, giả sử nước trong cốc là nước tinh khiết (D 1g/ml).
Đọc tiếp
Biết rằng canxi oxit (CaO – vôi sống) hóa hợp với nước tạo ra canxi hiđroxit (Ca(OH)2 – vôi tôi), chất này tan được trong nước, cứ 112 gam CaO hóa hợp vừa đủ với 36 gam H2O. Bỏ 5,6 gam CaO vào trong một cốc lớn chứa 400 ml nước tạo ra dung dịch Ca(OH)2, còn gọi là nước vôi trong.
(a) Tính khối lượng của canxi hiđroxit.
(b) Tính khối lượng của dung dịch Ca(OH)2, giả sử nước trong cốc là nước tinh khiết (D = 1g/ml).
biết rằng cani oxit( vôi sống) CaO hóa hợp với nước tạo ra canxi hiđroxit(vôi tôi) Ca(OH)2 , chất này tan được trong nước cứ 56g CaO hóa hợp vừa đủ với 18g H2O
Canxi cacbonat là thành phần chính của đá vôi. Khi nung đá vôi xảy ra phản ứng hóa học sau: Canxi cacbonat → Canxi oxit + cacbon đioxit. Biết rằng khi nung 280kg đá vôi tạo ra 140kg canxi oxit CaO (vôi sống) và 110kg khí cacbon đioxit CO2. a) Viết công thức về khối lượng của các chất trong phản ứng. b) Tính tỉ lệ phần trăm về khối lượng canxi cacbonat chứa trong đá vôi.
Đọc tiếp
Canxi cacbonat là thành phần chính của đá vôi. Khi nung đá vôi xảy ra phản ứng hóa học sau:
Canxi cacbonat → Canxi oxit + cacbon đioxit.
Biết rằng khi nung 280kg đá vôi tạo ra 140kg canxi oxit CaO (vôi sống) và 110kg khí cacbon đioxit CO2.
a) Viết công thức về khối lượng của các chất trong phản ứng.
b) Tính tỉ lệ phần trăm về khối lượng canxi cacbonat chứa trong đá vôi.
a) mCaCO3 = mCaO + mCO2
b) Khối lượng của CaCO3 đã phản ứng:
140 + 110 = 250 kg
Tỉ lệ phần trăm khối lượng CaCO3 chứa trong đá vôi:
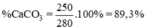
Đúng 3
Bình luận (1)
Hãy phân tích cho biết trường hợp nào xảy ra hiện tượng hóa học, trường hợp nào xảy ra hiện tượng vật lí. Hòa vôi sống vào nước được vôi tôi (vôi tôi là chất canxi hidro oxit, nước vôi trong là dung dịch chất này).
Hiện tượng hóa học vì vôi sống vào nước và trở thành vôi tôi là chất khác.
Đúng 0
Bình luận (0)
Canxi cacbonat (CaCO3) là thành phần chính của đá vôi. Khi nung đá vôi xẩy ra phản ứng hóa học sau:Canxi cacbonat à Canxi oxit + Canbon đioxitBiết rằng khi nung 280kg đá vôi tạo ra 140kg canxi CaO (vôi sống) và 110kg khí cacbon đioxit CO2.a) Viết công thức về khối lượng phản ứng.b) Tính tỉ lệ phần trăm về khối lượng canxi cacbonat chứa trong đá vôi.
Đọc tiếp
Canxi cacbonat (CaCO3) là thành phần chính của đá vôi. Khi nung đá vôi xẩy ra phản ứng hóa học sau:
Canxi cacbonat à Canxi oxit + Canbon đioxit
Biết rằng khi nung 280kg đá vôi tạo ra 140kg canxi CaO (vôi sống) và 110kg khí cacbon đioxit CO2.
a) Viết công thức về khối lượng phản ứng.
b) Tính tỉ lệ phần trăm về khối lượng canxi cacbonat chứa trong đá vôi.
a) Công thức về khối lượng phản ứng:
mCaCO3 = mCaO + mCO2
b) Áp dụng định luật bảo toàn khối lượng ta có :
mCaCO3 = 140 + 110 = 250 kg
Tỉ lệ phần trăm của Canxi cacbonat có trong đá vôi là :
%mCaCO3 = \(\frac{250.100\text{%}}{280}\) = 89,28%.
Đúng 1
Bình luận (0)
câu này làm sao vậy mn : Canxi cacbonat là thành phần chính của đá vôi. Khi nung đá vôi xảy ra phản ứng hoá học sau: Canxi cacbonat → Canxi oxit + Cacbon đioxit Biết rằng khi nung 280 kg đá vôi (CaCO3) tạo ra 140 kg vôi sống (CaO) và 110 kg khí cacbon đioxit. Tính tỉ lệ phần trăm về khối lượng canxi cacbonat chứa trong đá vôiA. 89,3% B. 88,3% C. 98,3%
Đọc tiếp
câu này làm sao vậy mn
: Canxi cacbonat là thành phần chính của đá vôi. Khi nung đá vôi xảy ra phản ứng hoá học sau:
Canxi cacbonat → Canxi oxit + Cacbon đioxit
Biết rằng khi nung 280 kg đá vôi (CaCO3) tạo ra 140 kg vôi sống (CaO) và 110 kg khí cacbon đioxit. Tính tỉ lệ phần trăm về khối lượng canxi cacbonat chứa trong đá vôi
A. 89,3% B. 88,3% C. 98,3%
\(m_{CaCO_3}=m_{CaO}+m_{CO_2}=250\left(kg\right)\\ \%m_{\dfrac{CaCO_3}{\text{đ}\text{á}.v\text{ô}i}}=\dfrac{250}{280}.100\approx89,3\%\)
Đúng 1
Bình luận (0)
Canxicacbonat(CaCo3) là thành phần chính của đá vôi. Khi nung đá vôi (Canxi cacbonat) bị phân hủy theo phản ứng hóa học sau:Canxi cacbonat - Canxi oxit + Cacbon dioxit Biết khi nung 560kg đá vôi tạo ra 280kg Canxi oxit Cao(Vôi sống) và 110kg khí Cacbon dioxit Co2a. Viết công thức về khối lượng của các chất trong phản ứng.b. Tính tỉ lệ phần trăm khối lượng canxi cacbonat chứa trong đá vôi.
Đọc tiếp
Canxicacbonat(CaCo3) là thành phần chính của đá vôi. Khi nung đá vôi (Canxi cacbonat) bị phân hủy theo phản ứng hóa học sau:
Canxi cacbonat -> Canxi oxit + Cacbon dioxit
Biết khi nung 560kg đá vôi tạo ra 280kg Canxi oxit Cao(Vôi sống) và 110kg khí Cacbon dioxit Co2
a. Viết công thức về khối lượng của các chất trong phản ứng.
b. Tính tỉ lệ phần trăm khối lượng canxi cacbonat chứa trong đá vôi.
a) Công thức về khối lượng phản ứng:
mCaCO3 = mCaO + mCO2
b) mCaCO3 = 280 + 110 = 390 kg
=> %CaCO3
= \(\frac{390}{560}\) = 69,7%
Đúng 0
Bình luận (0)














