Canxi oxit tác dụng được với: nước (1), dung dịch axit HCl (2), khí C O 2 (3), khí CO (4). Các tính chất đúng là thêm:
A. (1), (4)
B. (1), (2), (4)
C. (2), (3), (4)
D. (1), (2), (3)
Trong các thí nghiệm sau:
(1) Cho SiO2 tác dụng với axit HF.
(2) Cho khí SO2 tác dụng với khí H2S.
(3) Cho khí NH3 tác dụng với CuO đun nóng.
(4) Cho CaOCl2 tác dụng với dung dịch HCl đặc.
(5) Cho Si đơn chất tác dụng với dung dịch NaOH.
(6) Cho khí O3 tác dụng với Ag.
(7) Cho dung dịch NH4Cl tác dụng với dung dịch NaNO2 đun nóng.
(8) Cho khí F2 vào nước nóng.
(9) Nhiệt phân Cu(NO3)2.
(10) Sục khí Clo vào dung dịch NaOH.
Số thí nghiệm tạo ra đơn chất là
A. 7.
B. 6.
C. 9.
D. 8.
Đáp án D

Kiến thức cần nhớ
Silic (Si)
* Silic có 2 dạng thù hình là silic vô định hình và silic tinh thể.
Silic vô định hình: là chất bột màu nâu, không tan trong nước nhưng tan trong kim loại nóng chảy.
Silic tinh thể: có màu xám, có ánh kim, có cấu trúc giống kim cương nên có tính bán dẫn.
* Các mức oxi hóa có thể có của Si: -4; 0; +2; +4 (số oxi hóa +2 ít đặc trưng) nên Si có cả tính khử và tính oxi hóa.
Si + 2Fe2 → SiF4
Si + 2NaOH + H2O → Na2SiO3 + 2H2
SILIC ĐIOXIT (SiO2)
* Là chất ở dạng tinh thể nguyên tử, không tan trong nước. Trong tự nhiên chủ yếu tồn tại ở dạng khoáng vật thạch anh.
* SiO2 có tính chất của oxi axit, tan chậm trong dung dịch kiềm và tan dễ trong kiềm nóng chảy hoặc cacbonat kim loại kiềm nóng chảy → silicat.
SiO2 + 2NaOH → Na2SiO3 + H2O
SiO2 + Na2CO3 → Na2SiO3 + CO2
* SiO2 tan trong HF; phản ứng này dùng để khắc chữ lên bề mặt thủy tinh
Axit H2SiO3
* Dạng keo, không tan trong nước, khi đun nóng dễ bị mất nước
* Khi sấy khô H2SiO3 mất một phần nước tạo thành vật liệu xốp là silicagen được dùng làm chất hút ẩm và hấp phụ nhiều chất.
* Là axit yếu, yếu hơn axit cacbonic nên điều chế bằng cách dùng axit mạnh đẩy ra khỏi muối hoặc thủy phân một số hợp chất của Si. Na2SiO3 + CO2 + H2O → H2SiO3 + Na2CO3
Muối silicat
* Là muối của axit silicic thường không màu, khó tan (trừ muối kim loại kiềm tan được).
* Dung dịch đậm đặc của Na2SiO3 được gọi là thủy tinh lỏng được dùng để chế tạo keo dán thủy tinh và sứ, bảo quản vải và gỗ khỏi bị cháy. Trong dung dịch, silicat của kim loại kiềm bị thủy phân mạnh tạo môi trường bazơ.
Trong các thí nghiệm sau:
(1) Cho SiO2 tác dụng với axit HF.
(2) Cho khí SO2 tác dụng với khí H2S.
(3) Cho khí NH3 tác dụng với CuO đun nóng.
(4) Cho CaOCl2 tác dụng với dung dịch HCl đặc.
(5) Cho Si đơn chất tác dụng với dung dịch NaOH.
(6) Cho khí O3 tác dụng với Ag.
(7) Cho dung dịch NH4Cl tác dụng với dung dịch NaNO2 đun nóng.
(8) Cho khí F2 vào nước trong.
(9) Nhiệt phân Cu(NO3)2.
(10) Sục khí Clo vào dung dịch NaOH.
Số thí nghiệm tạo ra đơn chất là:
A.7.
B.6.
C.9.
D.8.
Chọn D
(1) Không, SiO 2 + 4 HF → SiF 4 ↑ + 2 H 2 O
(2)Có, SO 2 + H 2 S → 3 S ↓ + 2 H 2 O
(3)Có, 2 NH 3 + 3 CuO → t ° 3 Cu + N 2 + 3 H 2 O
(4)Có, CaOCl 2 + 2 HCl → CaCl 2 + Cl 2 + H 2 O
(5)Có, Si + 2 NaOH + H 2 O → Na 2 SiO 3 + H 2 ↑
(6)Có, 2 Ag + O 3 → Ag 2 O + O 2
(7)Có, NH 4 Cl + NaNO 2 → t ° N 2 + H 2 O + NaCl
(8)Có, 2 F 2 + 2 H 2 O → t ° 4 HF + O 2
(9)Có, Cu ( NO 3 ) 2 → t ° thường CuO + 2 NO + 1 2 O 2
(10)Không, Cl 2 + NaOH → NaCl + NaClO + H 2 O
Trong các thí nghiệm sau:
(1) Cho SiO2 tác dụng với axit HF.
(2) Cho khí SO2 tác dụng với khí H2S.
(3) Cho khí NH3 tác dụng với CuO đun nóng.
(4) Cho CaOCl2 tác dụng với dung dịch HCl đặc.
(5) Cho Si đơn chất tác dụng với dung dịch NaOH.
(6) Cho khí O3 tác dụng với Ag.
(7) Cho dung dịch NH4Cl tác dụng với dung dịch NaNO2 đun nóng.
(8) Cho khí F2 vào nước nóng.
(9) Nhiệt phân Cu(NO3)2.
(10) Sục khí Clo vào dung dịch NaOH.
Số thí nghiệm tạo ra đơn chất là
A. 7.
B. 6.
C. 9.
D. 8.
Chọn đáp án D
Phản ứng tạo đơn chất là: 2, 3, 4, 5, 6, 7, 8, 9
Trong các thí nghiệm sau:
(1) Cho SiO2 tác dụng với axit HF.
(2) Cho khí SO2 tác dụng với khí H2S.
(3) Cho khí NH3 tác dụng với CuO đun nóng.
(4) Cho CaOCl2 tác dụng với dung dịch HCl đặc.
(5) Cho Si đơn chất tác dụng với dung dịch NaOH.
(6) Cho khí O3 tác dụng với Ag.
(7) Cho dung dịch NH4Cl tác dụng với dung dịch NaNO2 đun nóng.
(8) Cho khí F2 vào nước trong.
(9) Nhiệt phân Cu(NO3)2.
(10) Sục khí Clo vào dung dịch NaOH.
Số thí nghiệm tạo ra đơn chất là:
A.7.
B.6
C.9.
D.8.
Trong các thí nghiệm sau:
(1) Cho SiO2 tác dụng với axit HF.
(2) Cho khí SO2 tác dụng với khí H2S.
(3) Cho khí NH3 tác dụng với CuO đun nóng.
(4) Cho CaOCl2 tác dụng với dung dịch HCl đặc.
(5) Cho Si đơn chất tác dụng với dung dịch NaOH.
(6) Cho khí O3 tác dụng với Ag.
(7) Cho dung dịch NH4Cl tác dụng với dung dịch NaNO2 đun nóng.
(8) Cho khí F2 vào nước nóng.
(9) Nhiệt phân Cu(NO3)2.
(10) Sục khí Clo vào dung dịch NaOH.
Số thí nghiệm tạo ra đơn chất là
A. 7.
B. 6.
C. 9.
D. 8
Chọn đáp án D
(1) Cho SiO2 tác dụng với axit HF
SiO2 + 4HF → SiF4 + 2H2O
(2) Cho khí SO2 tác dụng với khí H2S
SO2 + 2H2S → 3S + 2H2O
(3) Cho khí NH3 tác dụng với CuO đun nóng
2NH3 + 3CuO → 3Cu + N2 + 3H2O
(4) Cho CaOCl2 tác dụng với dung dịch HCl đặc
CaOCl2 + 2HCl → CaCl2 + Cl2 + H2O
(5) Cho Si đơn chất tác dụng với dung dịch NaOH
Si + 2NaOH + H2O → Na2SiO3 + 2H2
(6) Cho khí O3 tác dụng với Ag
2Ag + O3 → Ag2O + O2
(7) Cho dung dịch NH4Cl tác dụng với dung dịch NaNO2 đun nóng
NH4Cl + NaNO2 → NaCl + N2 + 2 H2O
(8) Cho khí F2 vào nước nóng
2F2 + 2H2O → 4HF + O2
(9) Nhiệt phân Cu(NO3)2
2Cu(NO3)2 → 2CuO + 4NO2 + O2
(10) Sục khí Clo vào dung dịch NaOH
Cl2 + 2NaOH → NaCl + NaClO + H2O
Vậy có 8 phản ứng tạo sản phẩm đơn chất
Trong các thí nghiệm sau:
(1)Cho SiO2 tác dụng với axit HF.
(2) Cho khí SO2 tác dụng với khí H2S.
(3) Cho tinh thể KMnO4 vào dung dịch HCl đặc.
(4) Cho CaOCl2 tác dụng với dung dịch HCl đặc.
(5) Cho Si đơn chất tác dụng với dung dịch NaOH.
(6) Cho khí O3 tác dụng với dụng với Ag.
(7) Cho dung dịch NH4Cl tác dụng với dung dịch NaNO2 đun nóng.
(8) Cho khí F2 vào nước nóng.
(9) Nhiệt phân Cu(NO3)2.
(10) Sục khí clo vào dung dịch NaOH.
Số thí nghiệm tạo ra đơn chất là:
A.7
B.6
C.9
D.8
Đáp án D
( 1 ) SiO 2 + 4 HF → SiF 4 + 2 H 2 O ( 2 ) SO 2 + 2 H 2 S → 3 S + 2 H 2 O ( 3 ) 2 KMnO 4 + 16 HCl → 5 Cl 2 + 2 MnCl 2 + 2 KCl + 8 H 2 O ( 4 ) CaOCl 2 + 2 HCl ( đặc ) → CaCl 2 + Cl 2 + H 2 O ( 5 ) Si + 2 NaOH + H 2 O → Na 2 SiO 3 + 2 H 2 ( 6 ) O 3 + 2 Ag → Ag 2 O + O 2 ( 7 ) NH 4 Cl + NaNO 2 → t ° NaCl + N 2 + 2 H 2 O ( 8 ) 2 F 2 + 2 H 2 O → t ° 4 HF + O 2 ( 9 ) 2 Cu ( NO 3 ) 2 → t ° 2 CuO + 4 NO 2 + O 2 ( 10 ) Cl 2 + 2 NaOH → NaCl + NaClO + H 2 O
Các thí nghiệm thu được đơn chất gồm (2), (3), (4), (5), (6), (7) , (8), (9).
Trong các thí nghiệm sau:
(1)Cho SiO2 tác dụng với axit HF.
(2) Cho khí SO2 tác dụng với khí H2S.
(3) Cho tinh thể KMnO4 vào dung dịch HCl đặc.
(4) Cho CaOCl2 tác dụng với dung dịch HCl đặc.
(5) Cho Si đơn chất tác dụng với dung dịch NaOH.
(6) Cho khí O3 tác dụng với dụng với Ag.
(7) Cho dung dịch NH4Cl tác dụng với dung dịch NaNO2 đun nóng.
(8) Cho khí F2 vào nước nóng.
(9) Nhiệt phân Cu(NO3)2.
(10) Sục khí clo vào dung dịch NaOH.
Số thí nghiệm tạo ra đơn chất là:
A. 7.
B. 6.
C. 9.
D. 8.
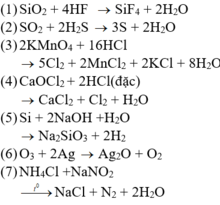
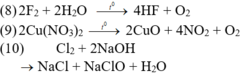
Các thí nghiệm thu được đơn chất gồm (2), (3), (4), (5), (6), (7) , (8), (9).
Đáp án D.
Bài 1: Cho 40g hỗn hợp natri và canxi oxit tác dụng với nước dư thu được dung dịch A và 6,72l khí B (đktc)
a) Tính khối lượng của các chất có trong hỗn hợp
b) Tính khối lượng của các chất tan có trong dung dịch A
Bài 2: hòa tan hết 52,2(g) sắt từ oxit bằng dung dịch axit clohiđic dư. Tính khối lượng của các muối thu được sau phản ứng
Bài 3: Đốt cháy hết 16,8(g) sắt trong không khí oxi dư thu được m(g) sắt oxit vào dung dịch axt sunfic. Tính khối lượng muối thu được sau phản ứng
Bài 2 :
\(n_{Fe_3O_4} = \dfrac{52,2}{232} = 0,225(mol)\\ Fe_3O_4 + 8HCl \to 2FeCl_3 + FeCl_2 + 4H_2O\\ n_{FeCl_2} = n_{Fe_3O_4} = 0,225(mol) \Rightarrow m_{FeCl_2} = 0,225.127 = 28,575(gam)\\ n_{FeCl_3} = 2n_{Fe_3O_4} = 0,45(mol) \Rightarrow m_{FeCl_3} = 0,45.162,5 = 73,125(gam)\)
Bài 3 :
\(n_{Fe} = \dfrac{16,8}{56} = 0,3(mol)\\ 3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4\\ n_{Fe_3O_4} = \dfrac{1}{3}n_{Fe} = 0,1(mol)\\ Fe_3O_4 + 4H_2SO_4 \to Fe_2(SO_4)_3 + FeSO_4 + 4H_2O\\ n_{FeSO_4} = n_{Fe_2(SO_4)_3} = n_{Fe_3O_4} = 0,1(mol)\\ \Rightarrow m_{FeSO_4} = 0,1.152 = 15,2(gam)\\ m_{Fe_2(SO_4)_3} = 0,1.400 = 40(gam)\)
Cho các trường hợp sau:
(1) O3 tác dụng với dung dịch KI.
(2) Axit HF tác dụng với SiO2.
(3) MnO2 tác dụng với dung dịch HCl đặc, đun nóng.
(4) Khí SO2 tác dụng với nước Cl2.
(5) KClO3 tác dụng với dung dịch HCl đặc, đun nóng.
(6) Đun nóng dung dịch bão hòa gồm NH4Cl và NaNO2.
(7) Cho khí NH3 qua CuO nung nóng.
Số trường hợp tạo ra đơn chất là
A. 6.
B. 5.
C. 4.
D. 3.