Hỗn hợp khí A chứa eilen và H2. Tỉ khối của A đối với hiđro là 7,5. Dẫn A đi qua chất xuc tác Ni nung nóng thu được hh khí B có tỉ khối đối với hiđro là 9,0. Hiệu suất phản ứng cộng hiđro của etilen là:
A. 33,3%
B. 66,7%
C. 25%
D. 50%
Hỗn hợp khí A chứa eten và hiđro. Tỉ khối của A đối với hiđro là 7,5. Dẫn A đi qua chất xúc tác Ni nung nóng thì A biến thành hỗn hợp khí B có tỉ khối đối với hiđro là 9,0.
Tính hiệu suất phản ứng cộng hiđro của eten.
Giả sử trong 1 mol hỗn hợp A có x mol C 2 H 4 và (1-x) mol H 2 .
M A = 28x + 2(1 - x) = 7,5.2 = 15 (g/mol) ;
⇒ x = 0,5.
Giả sử khi dẫn 1 mol A qua chất xúc tác Ni, có n mol C 2 H 4 tham gia phản ứng :
C 2 H 4 + H 2 → C 2 H 6
n mol n mol n mol
Số mol khí còn lại trong hỗn hợp B là (1-n) mol. Theo định luật bảo toàn khối lượng :
m B = m A = 15 g.
Khối lượng của 1 mol B:
![]()
Hiệu suất phản ứng:
![]()
Có: \(\overline{M}_A=2.7,5=15\), sử dụng sơ đồ đường chéo
=> n(C2H4) : n(H2) = 1:1
Giả sử trong có 1 mol hỗn hợp A
=> m(A)=15g
BTKL: m(B)=m(A)= 15g
=>\(n_B=\dfrac{15}{2.9}=0,83mol\)
=> n(H2) pư= 1- 0,83 = 0,17 mol
=>\(H=\dfrac{0,17}{1:2}.100\%=34\%\)
Hỗn hợp khí A chứa etilen và hidro có tỉ khối so với hidro là 7,5. Dẫn A qua xúc tác Ni nung nóng thu được hỗn hợp B có tỉ khối so với hidro là 12,5. Tính hiệu suất phản ứng cộng hidro của etilen.

Vì khối lượng của hỗn hợp trước và sau phản ứng là bằng nhau
=> n hh trước phản ứng : n hh sau phản ứng = 25 : 15 = 5 : 3
Coi tổng số mol trước phản ứng là 5 => tổng số mol sau phản ứng là 3 mol
Ta có khối lượng hỗn hợp là : 5 . 15 = 75 g
Ta có hệ :
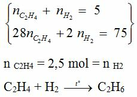
Ban đầu 2,5 2,5
Phản ứng x x
Kết thúc : 2,5 – x 2,5– x x
=> Tổng số mol sau phản ứng là : : 2,5 – x + 2,5– x + x = 5–x
=> 5 – x = 3 => x = 2 mol
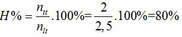
Hỗn hợp khí X gồm H2 và C2H4 có tỉ khối so với H2 là 3,6. Dẫn X qua Ni nung nóng, thu được hỗn hợp khí Y có tỉ khối so với H2 là 4. Hiệu suất của phản ứng hiđro hóa là
A. 25%
B. 20%
C. 50%
D. 40%
Đáp án C
Giả sử hỗn hợp X chứa 1 mol → nH2 = 0,8 mol, nC2H2 = 0,2 mol
Luôn có mX = mY → nY =
1
.
3
,
6
.
2
4
.
2
= 0,9 mol
Nhận thấy nH2 pu = nC2H4 pu = nX - nY = 1- 0,9 = 0,1 mol
→ H = 0 , 1 0 , 2 ×100% = 50%.
Hỗn hợp X gồm etilen và hiđro có tỉ khối so với H2 là 4,25. Dẫn X qua bột Ni, nung nóng (hiệu suất phản ứng 75%), thu được hỗn hợp Y (thể tích các khí đo ở cùng điều kiện). Tỉ khối hơi của Y so với H2 là
A. 5,23
B. 10,4
C. 4,25
D. 5,75
Đáp án A
• Coi hhX ban đầu có x mol CH2=CH2 và y mol H2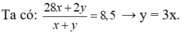
Coi hh ban đầu gồm 1 mol CH2=CH2 và 3 mol H2.
• hhY gồm 0,75 mol C2H6; (1 - 0,75) mol C2H4 và (3 - 0,75) mol H2
→ ∑nY = 0,75 + (1 - 0,75) + (3 - 0,75) = 3,25 mol.
Theo BTKL: mY = mX = 1 x 28 + 3 x 2 = 34 gam
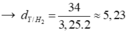
Hỗn hợp X gồm H2 và C2H4 có tỉ khối so với H2 là 7,5. Dẫn X qua Ni nung nóng, thu được hỗn hợp Y có tỉ khối so với H2 là 12,5. Hiệu suất của phản ứng hiđro hóa là
A. 70%.
B. 60%.
C. 50%.
D. 80%.
Đáp án D
hhX gồm H2 và C2H4 có dX/H2 = 7,5.
Dẫn X qua Ni, to → hhY có dY/H2 = 12,5.
• Đặt nH2 = x mol; nC2H4 = y mol.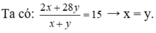
Đặt nH2 = 1 mol; nC2H4 = 1 mol.
Giả sử có x mol C2H6 tạo thành → hhY gồm C2H6 x mol; H2 (1 - x) mol và C2H4 (1 - x) mol.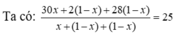
→ x = 0,8 → H = 80%
Hỗn hợp khí X gồm H2 và C2H4 có tỉ khối so với He là 3,75. Dẫn X qua Ni nung nóng, thu được hỗn hợp khí Y có tỉ khối so với He là 5. Hiệu suất của phản ứng hiđro hoá là
A. 20%.
B. 25%.
C. 40%.
D. 50%.
Đáp án D
hhX gồm H2 và C2H4 có dX/He = 3,75.
Dẫn X qua Ni, to → hhY có dY/He = 5.
• Đặt nH2 = x mol; nC2H4 = y mol.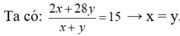
Đặt nH2 = 1 mol; nC2H4 = 1 mol.
Giả sử có x mol C2H6 tạo thành → hhY gồm C2H6 x mol; H2 (1 - x) mol và C2H4 (1 - x) mol.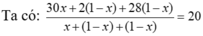
→ x = 0,5 → H = 50%
Hỗn hợp khí X gồm H2 và C2H4 có tỉ khối so với He là 3,75. Dẫn X qua Ni nung nóng, thu được hỗn hợp khí Y có tỉ khối so với He là 5. Hiệu suất của phản ứng hiđro hoá là:
A. 20%.
B. 40%.
C. 25%.
D. 50%.
Đáp án D
MX = 15. Áp dụng qui tắc đường chéo : nC2H4 : nH2 = 1 : 1. Giả sử số mol mỗi chất trong X là 1
C2H4 + H2 ->C2H6
, x -> x -> x
=> nY = 2 – x mol
Bảo toàn khối lượng : mX = mY => 2 + 28 = 4.5.(2 – x)
=> x = 0,5 mol => H% = 50%