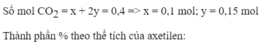Một hỗn hợp gồm C 2 H 2 v à C 2 H 4 có thể tích 5,6 lít khí (đktc) cho qua dung dịch B r 2 dư, dung dịch này nặng thêm 6,8 g. Tính thể tích mỗi khí trong hỗn hợp ban đầu (cho H=1, C=12).

Những câu hỏi liên quan
02: Dẫn 5,6 lít hỗn hợp khí metan CH 4 và axetilen C 2 H 2 (ở đktc) đi qua dung dịch brom dư, thấy có 32 gam brom phản ứng. a. Viết phương trình phản ứng xảy ra. b. Tính thành phần phần trăm theo thể tích các khí có trong hỗn hợp. c. Tính thể tích khí oxi ở đktc cần dùng để đốt cháy hoàn toàn hỗn hợp trên. Cho biết: C = 12, H = 1, Br = 80
n Br2=\(\dfrac{32}{160}\)=0,2 mol
C2H2+2Br2->C2H2Br4
0,1------0,2 mol
=>%VC2H2=\(\dfrac{0,1.22,4}{5,6}\).100=40%
=>%VCH4=100-40=60%
=>n CH4=\(\dfrac{5,6-0,1.22,4}{22,4}\)=0,15 mol
CH4+2O2-to>CO2+2H2O
0,15----0,3
C2H2+\(\dfrac{5}{2}\)O2-to>2CO2+H2O
0,1-----0,25 mol
=>VO2=(0,3+0,25).22,4=12,32l
Đúng 1
Bình luận (0)
Câu 10: Một hỗn hợp gồm metan và etilen có thể tích 8,96 lít (đktc) sục vào dung dịch Br2 dư . Dung dịch nặng thêm 5,6 g. Tìm thể tích khí không khí (đktc) cần để đốt cháy hết hỗn hợp trên (H=1, C=12).
mtăng = mC2H4
=> \(n_{C_2H_4}=\dfrac{5,6}{28}=0,2\left(mol\right)\)
=> \(n_{CH_4}=\dfrac{8,96}{22,4}-0,2=0,2\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,2--->0,4
C2H4 + 3O2 --to--> 2CO2 + 2H2O
0,2---->0,6
=> VO2 = (0,4 + 0,6).22,4 = 22,4 (l)
=> Vkk = 22,4.5 = 112 (l)
Đúng 3
Bình luận (0)
Một hỗn hợp gồm etilen và metan khi cho qua dung dịch brom dư thì dung dịch tăng 5,6 g đồng thời có 5,6 lít chất khí bay ra (đktc).
Thành phần % theo thể tích của etilen ban đầu là (cho H=1, C=12)
A. 55,56%
B. 45,45%
C. 33,33%
D. 44,44%
Cho 0,56 lít (đktc) hỗn hợp khí gồm C2H4, C2H2 tác dụng hết với dung dịch brom dư, khối lượng brom đã tham gia phản ứng là 5,6 gam.
a) Hãy viết phương trình hoá học.
b) Tính phần trăm thể tích của mỗi khí trong hỗn hợp.
Số mol hỗn hợp = 0m56 : 22,4 = 0,025 mol; số mol Br2 = 5,6 : 160 = 0,035 mol.
Gọi x, y lần lượt là số mol của etilen và axetilen.
a) Phương trình hoá học:
C2H4 + Br2 → C2H4Br2
P.ư: x x x (mol)
C2H2 + 2Br2 → C2H2Br4
P.ư: y 2y y (mol)
b) Ta có hệ phương trình: ; Giải hệ ta được y = 0,01 và x = 0,015
% =
x 100% = 60%;
= 100% - 60% = 40%
Đúng 1
Bình luận (1)
Một hỗn hợp X gồm khí c 3 h 4 c 3 h 6 c 3 h 8 đốt cháy hoàn toàn 8,96 lít hỗn hợp X thì phải dùng hết v lít khí oxi thu được m gam CO2 và 19,8 gam nước biết rằng thể tích các khí được đo ở điều kiện tiêu chuẩn a tính m và V
Một hỗn hợp X gồm các khí C\(_3\)H\(_4\), C\(_3\)H\(_6\), C\(_3\)H\(_8\). Đốt cháy 8,96 lít hỗn hợp X cần dùng V lít khí... - Hoc24
Anh có giải bài này ở đây rồi , em tham khảo nhé !
Đúng 1
Bình luận (0)
đốt cháy 3,36 lít hỗn hợp gồm c 2 H 6 và c 3 h 4 cần dùng 61,6 lít không khí (biết VO2 chiếm 20% thể tích không khí) các khí ở đktc. a, tính tỷ lệ phần trăm thể tích mỗi khí b, hỗn hợp khí trên làm mất màu bao nhiêu gam dung dịch Brom 8%
a, \(V_{O_2}=61,6.20\%=12,32\left(l\right)\Rightarrow n_{O_2}=\dfrac{12,32}{22,4}=0,55\left(mol\right)\)
PT: \(2C_2H_6+7O_2\underrightarrow{t^o}4CO_2+6H_2O\)
\(C_3H_4+4O_2\underrightarrow{t^o}3CO_2+2H_2O\)
Ta có: \(n_{C_2H_6}+n_{C_3H_4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\left(1\right)\)
Theo PT: \(n_{O_2}=\dfrac{7}{2}n_{C_2H_6}+4n_{C_3H_4}=0,55\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{C_2H_6}=0,1\left(mol\right)\\n_{C_3H_4}=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_2H_6}=\dfrac{0,1.22,4}{3,36}.100\%\approx66,67\%\\\%V_{C_3H_4}\approx33,33\%\end{matrix}\right.\)
b, \(C_3H_4+2Br_2\rightarrow C_3H_4Br_4\)
Ta có: \(n_{Br_2}=2n_{C_3H_4}=0,1\left(mol\right)\)
\(\Rightarrow m_{Br_2}=0,1.60=16\left(g\right)\Rightarrow m_{ddBr_2}=\dfrac{16}{8\%}=200\left(g\right)\)
Đúng 1
Bình luận (1)
a) Tính tỷ lệ phần trăm có thể phân bổ cho mỗi khí:
Ta có số mol khí của C2H6:
n(C2H6) = V(C2H6)/V(M)
n(C2H6) = 3,36/22,4 = 0,15 mol
Ta có số mol khí của C3H4:
n(C3H4) = V(C3H4)/V(M)
n(C3H4) = 3,36/22,4 = 0,15 mol
Do đó, Tỷ lệ phần trăm có thể tích cho mỗi khí là:
V(M) là khối lượng mol của hỗn hợp khí (đã được tính ở bước trước).
b) Giả sử dung dịch brom 8% là dung dịch brom trong nước có nhiệt độ 8% theo khối lượng. Dung dịch này có khả năng tác dụng với các hợp chất hữu cơ, trong đó có hidrocacbon không no và không.
Phản ứng của Br2 trong dung dịch brom với hidrocacbon không có dạng:
Br2 + C2H6 → 2 HBr + C2H4
Vì cân bằng nhiệt độ mol không khí đã biết rằng, Tỷ lệ phần trăm khối lượng của O2 trong không khí là 0, 20 * 32 g = 6,4 g.
Tính lượng brom cần để phản ứng với C2H4 trong 3,36 lít hỗn hợp:
n(C2H4) = n(C3H4) * (2 mol C2H4 / 3 mol C3H4) = 0,15 * (2/3) = 0,1 mol
Theo phương trình trên 1 mol C2H4 tác dụng với 1 mol Br2
Cần dùng n(Br2) = n(C2H4) = 0,1 mol brom trong phản ứng này.
Do đó, khối lượng brom cần sử dụng là m = n(Br2) * M(Br2) = 0,1 * 159,8 g/mol = 15,98 g brom
Do đó hỗn hợp khí trên làm mất màu 15,98 g dung dịch brom 8%.
Đúng 0
Bình luận (0)
Khối lượng hỗn hợp khí ở đktc gồm có 11,2 lít H2 và 5,6 lít O2
PTHH là : 2H2 + O2 -----) 2H2O
Số mol của \(H_2\) là
\(n_{H_2}=\frac{V_{H_2\left(ĐKTC\right)}}{22,4}=\frac{11,2}{22,4}=0,5\left(mol\right)\)
Số mol của \(O_2\) là :
\(n_{O_2}=\frac{V_{O_2\left(ĐKTC\right)}}{22,4}=\frac{5.6}{22,4}=0,25\left(mol\right)\)
PTHH : 2H2 + O2 -----) 2H2O
Theo PTHH : 2 : 1 : 2 (mol)
Theo bài ra : 0,5---)0,25-----)0,25 (mol)
Khối lượng của hỗn hợp khí H2O là
\(m_{H_2O}=n_{H_2O}\times M_{H_2O}=0,5\times\left(2+16\right)=9\left(g\right)\)
Chúc bạn học tốt =))![]()
Đúng 0
Bình luận (0)
Vì đây chỉ là dang hỗn hợp và không có nhiệt độ => Không có phản ứng
Ta có: nH2 = \(\frac{11,2}{22,4}=0,5\left(mol\right)\)
=> Khối lượng H2: mH2 = 0,5 x 2 = 1 (gam)
nO2 = \(\frac{5,6}{22,4}=0,25\left(mol\right)\)
=> Khối lượng O2: mO2 = 0,25 x 32 = 8 (gam)
=> Khối lượng hỗn hợp: mhỗn hợp = mH2 + mO2 = 1 + 8 = 9 gam
Đúng 0
Bình luận (0)
Cho 5,6 lít hỗn hợp khí (đktc) gồm c2h4 và c2h2 có tỉ lệ thể tích là 3: 2 tác dụng với dung dịch brom dư. khối lượng brom đã tham gia phản ứng là(Biết phản ứng xảy ra hoàn toàn) (Cho NTK: C = 12; H = 1; Br = 80 )
A. 64 gam
B. 24 gam.
C. 16 gam.
D. 56 gam.
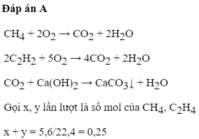
Đốt cháy hết hỗn hợp gồm metan và axetilen có thể tích 5,6 lít (đktc), cho sản phẩm quan một lượng dư dung dịch
C
a
(
O
H
)
2
thu được 40 g
C
a
C
O
3
. Thành phần % theo thể tích của axetilen trong hỗn hợp ban đầu là A. 60% B. 50% C. 40% D. 30%
Đọc tiếp
Đốt cháy hết hỗn hợp gồm metan và axetilen có thể tích 5,6 lít (đktc), cho sản phẩm quan một lượng dư dung dịch C a ( O H ) 2 thu được 40 g C a C O 3 . Thành phần % theo thể tích của axetilen trong hỗn hợp ban đầu là
A. 60%
B. 50%
C. 40%
D. 30%