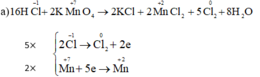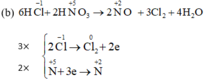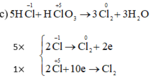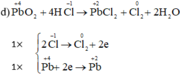Cho phản ứng: KMnO4 + HCl (đặc) ![]() KCl + MnCl2 + Cl2 + H2O
KCl + MnCl2 + Cl2 + H2O
Hệ số cân bằng phản ứng là các số tối giản. Số phân tử HCl đóng vai trò chất khử là:
A. 16
B. 5
C. 10
D. 8
Cho phản ứng: KMnO4 + HCl (đặc) → t ° KCl + MnCl2 + Cl2 + H2O
Hệ số cân bằng phản ứng là các số tối giản. Số phân tử HCl đóng vai trò chất khử là:
A. 16
B. 5
C. 10
D. 8
Cho phương trình: K M n O 4 + H C l → M n C l 2 + C l 2 + K C l + H 2 O . Hệ số phân tử HCl đóng vai trò chất khử và môi trường trong phương trình lần lượt là:
A. 16; 10.
B. 16; 4.
C. 6; 10.
D. 10; 6.
Chọn D.
Hệ số HCl đóng vai trò chất khử chính là hệ số Cl- về Cl0 là 10, hệ số HCl đóng vai trò môi trường là hệ số Cl trong muối là 6.
Cho phản ứng HCl + KMnO4 → KCl + Cl2 + MnCl2 + H2O.
Tổng hệ số (số nguyên, tối giản) tất cả các chất trong phương trình hóa học của phản ứng trên là
A. 35
B. 34
C. 32
D. 37
Chọn A
16HCl + 2KMnO4 → 2KCl + 5Cl2 + 2MnCl2 + 8H2O.
Trong phản ứng
K 2 Cr 2 O 7 + HCl → CrCl 3 + Cl 2 + KCl + H 2 O
Số phân tử HCl đóng vai trò chất khử bằng k lần tổng số phân tử HCl tham gia phản ứng. Giá trị của k là
A. 3/14 B. 4/7
C. 1/7 D. 3/7
Trong phản ứng: K 2 C r 2 O 7 + HCl → C r C l 3 + C l 2 + KCl + H 2 O , số phân tử HCl đóng vai trò chất khử bằng k lần tổng số phân tử HCl tham gia phản ứng. Giá trị của k là
A. 3 7
B. 1 7
C. 3 14
D. 4 7
Chọn đáp án A
K 2 C r 2 O 7 + 14HCl → 2 C r C l 3 + 3 C l 2 + 2KCl + 7 H 2 O
Số phân tử C l 2 là 3 => số phân tử HCl bị khử là 6.
Số phân tử HCl tham gia phản ứng là 14 => k = 6 14 = 3 7
Trong phản ứng:
K2Cr2O7 + HCl→ CrCl3 + Cl2 + KCl + H2O
Số phân tử HCl đóng vai trò chất khử bằng k lần tổng số phân tử HCl tham gia phản ứng. Giá trị của k là
A. 3/14
B. 4/7
C. 1/7
D. 3/7
Đáp án D
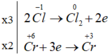
K2Cr2O7 + 14HCl→ 2CrCl3 + 3Cl2 + 2KCl + 7H2O
Số phân tử HCl đóng vai trò chất khử /tổng số phân tử HCl tham gia phản ứng = 6/14 = 3/7
Trong phản ứng: K2Cr2O7 + HCl ® CrCl3 + Cl2 + KCl + H2O
Số phân tử HCl đóng vai trò chất khử bằng k lần tổng số phân tử HCl tham gia phản ứng. Giá trị của k là
A. 4/7.
B. 1/7.
C. 3/14.
D. 3/7.
Chọn D
Trong phản ứng trên, K2Cr2O7 là chất oxi hóa, HCl là chất khử.
Quá trình oxi hóa – khử :
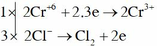
K2Cr2O7 + 14HCl ® 2CrCl3 + 3Cl2 + 2KCl + 7H2O

cho phương trình hóa học: KMnO4 + HCl -> KCl + MnCl2 + Cl2 + H2O. Số phân tử HCl đóng vai trò chất khử, đóng vai trò môi trường là:
A. 10,6
B. 10,16
C. 2,16
D. 6,10
cho phương trình hóa học: KMnO4 + HCl -> KCl + MnCl2 + Cl2 + H2O. Số phân tử HCl đóng vai trò chất khử, đóng vai trò môi trường là:
A. 10,6
B. 10,16
C. 2,16
D. 6,10
Cân bằng các phương trình phản ứng oxi hóa – khử sau bằng phương pháp thăng bằng electron:
a) KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O.
b) HNO3 + HCl → NO + Cl2 + H2O.
c) HClO3 + HCl → Cl2 + H2O.
d) PbO2 + HCl → PbCl2 + Cl2 + H2O
Cân bằng các phản ứng oxi hóa – khử sau bằng phương pháp thăng bằng electron: