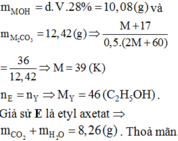Cho 0,1 mol axit axetic vào cốc chứa 30 ml dung dịch MOH 20% (D 1,2 g/ml, M là kim loại kiềm). Cô cạn dung dịch sau phản ứng, thu được m gam chất rắn khan. Đốt cháy hoàn toàn chất rắn thu được 9,54 gam M2CO3 và hỗn hợp khí, dẫn hỗn hợp qua dung dịch nước vôi trong dư thì khối lượng dung dịch thay đổi như thế nào? A. Giảm 5,70 gam B. Tăng 5,70 gam C. Giảm 2,74 gam D. Tăng 2,74 gam
Đọc tiếp
Cho 0,1 mol axit axetic vào cốc chứa 30 ml dung dịch MOH 20% (D = 1,2 g/ml, M là kim loại kiềm). Cô cạn dung dịch sau phản ứng, thu được m gam chất rắn khan. Đốt cháy hoàn toàn chất rắn thu được 9,54 gam M2CO3 và hỗn hợp khí, dẫn hỗn hợp qua dung dịch nước vôi trong dư thì khối lượng dung dịch thay đổi như thế nào?
A. Giảm 5,70 gam
B. Tăng 5,70 gam
C. Giảm 2,74 gam
D. Tăng 2,74 gam