Hợp chất X1 gồm 2 nguyên tố có công thức phân tử dạng M2On, trong đó nguyên tố oxi chiếm 74,07% về khối lượng. X2 là axit tương ứng của X1. Biết rằng, cứ 1 mol X1 phản ứng với 1 mol nước tạo ra 2 mol X2. Tìm công thức của X1, X2.

Những câu hỏi liên quan
Cho các phản ứng sau theo đúng tỉ lệ số mol:((1) C9H20N2O4 + 2NaOH ® X1 + X2 + X3 (bay hơi) + H2O(2) X1 + 3HCl ® X4 + 2NaCl(3) X2
→
H
2
SO
4
,
170
o
C
C2H4 + H2O(4) X2 + O2
→...
Đọc tiếp
Cho các phản ứng sau theo đúng tỉ lệ số mol:
((1) C9H20N2O4 + 2NaOH ® X1 + X2 + X3 (bay hơi) + H2O
(2) X1 + 3HCl ® X4 + 2NaCl
(3) X2 → H 2 SO 4 , 170 o C C2H4 + H2O
(4) X2 + O2 → men X5 + H2O
(5) X5 + X3 ® X6
Biết X3 có cùng số nguyên tử cacbon với X2. Cho các phát biểu sau:
(a) X6 có công thức phân tử là C4H11NO2.
(b) Đốt cháy hoàn toàn 1 mol X1 thu được 8 mol hỗn hợp khí và hơi gồm CO2, H2O và N2.
(c) Tổng số nguyên tử trong phân tử X4 là 22.
(d) Đốt cháy hoàn toàn 1 mol X1 cần dùng 5,5 mol khí oxi.
Số phát biểu đúng là
A. 1.
B. 3.
C. 4.
D. 2.
Cho các phản ứng sau theo đúng tỉ lệ số mol: (1) C9H20N2O4 + 2NaOH ® X1 + X2 + X3 + H2O (2) X1 + 3HCl ® X4 + 2NaCl (3) X2
→
H
2
SO
4
,
170
o
C2H4+H2O (4) X2 + O2
→
men
X5 + H2O (5) X5 + X3 ® X6 Biết X3 có c...
Đọc tiếp
Cho các phản ứng sau theo đúng tỉ lệ số mol:
(1) C9H20N2O4 + 2NaOH ® X1 + X2 + X3 + H2O
(2) X1 + 3HCl ® X4 + 2NaCl
(3) X2 → H 2 SO 4 , 170 o C2H4+H2O
(4) X2 + O2 → men X5 + H2O
(5) X5 + X3 ® X6
Biết X3 có cùng số nguyên tử cacbon với X2. Cho các phát biểu sau:
(a) X6 có công thức phân tử là C4H11NO2.
(b) Đốt cháy hoàn toàn 1 mol X1 thu được 8 mol hỗn hợp khí và hơi gồm CO2, H2O và N2.
(c) Tổng số nguyên tử trong phân tử X4 là 22.
(d) Đốt cháy hoàn toàn 1 mol X1 cần dùng 5,5 mol khí oxi.
Số phát biểu đúng là
A. 1.
B. 3.
C. 4.
D. 2.
Chọn D.
(3) C2H5OH (X2) → H 2 SO 4 , 170 o C2H4 + H2O
(4) C2H5OH (X2) + O2 → men CH3COOH (X5)
+ H2O
(1) C2H5OOC-(CH2)2-CH(NH2)-COONH3C2H5
+ 2NaOH ® NaOOC-(CH2)2-CH(NH2)-COONa (X1)
+ C2H5OH (X2) + C2H5NH2 (X3) + H2O
(2) NaOOC-(CH2)2-CH(NH2)-COONa (X1) + 3HCl
® HOOC-(CH2)2-CH(NH3Cl)-COOH (X4) + 2NaCl
(5) CH3COOH + C2H5NH2 ® CH3COONH3C2H5(X6)
(c) Sai, Tổng số nguyên tử trong phân tử X4 là 21.
(d) Sai, Đốt cháy hoàn toàn 1 mol X1 cần dùng 5,25
mol khí oxi.
Đúng 0
Bình luận (0)
có hai nguyên tố A và B tạo thành hai loại hợp chất X1 và X2. Trong X1 nguyên tố A chiếm 75% về khối lượng, nguyên tố B chiếm 25% ; Trong X2, nguyên tố A chiếm 90% về khối lượng, nguyên tố B chiếm 10% về khối lượng. Nếu công thức của chúng trong X1 là AB4 thì công thức hóa học của X2 là gì?
*Trong hợp chất A:
\(\%X_1=75\%\)
\(\Rightarrow\dfrac{X_1}{X_1+4X_2}\cdot100\%=75\%\)
\(\Rightarrow100X_1=75X_1+300X_2\)
\(\Rightarrow25X_1=300X_2\Rightarrow X_1=12X_2\)
*Trong hợp chất B:
Gọi CTHH là \(A_aB_b\)
\(a:b=\dfrac{90\%}{X_1}:\dfrac{10\%}{X_2}=\dfrac{90\%}{12X_2}:\dfrac{10\%}{X_2}=3:4\)
Vậy CTHH là \(A_3B_4\)
Đúng 3
Bình luận (0)
Hợp chất x có khối lượng mol phân tử là 62g/mol . Trong phân tử của hợp chất, nguyên tố oxi chiếm 25,8% theo khối lượng,còn lại là nguyên tố Na . Lập công thức hoá học của x
\(Đặt:CTTQ:Na_xO_y\left(x,y:nguyên,dương\right)\\ x=\dfrac{62.\left(100\%-25,8\%\right)}{23}=2\\ y=\dfrac{62.25,8\%}{16}=1\\ \Rightarrow CTHH:Na_2O\)
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn hỗn hợp X gồm hai amin đơn chức X1, X2 (đều bậc I, cùng số nguyên tử cacbon trong phân tử, X1 là amin no mạch hở và phân tử X1 nhiều hơn phân tử X2 hai nguyên tử H) thu được 0,1 mol CO2. Mặt khác cho toàn bộ lượng X trên tác dụng với dung dịch HNO2 sinh ra 0,05 mol N2. Trong các khẳng định sau có bao nhiêu khẳng định đúng? (1) Trong phân tử X2 có 7 liên kết σ và 1 liên kết π.(2) Cả X1 và X2 phản ứng được với HNO2 cho sản phẩm hữu cơ tham gia phản ứng tráng bạc.(3) Lực bazơ củ...
Đọc tiếp
Đốt cháy hoàn toàn hỗn hợp X gồm hai amin đơn chức X1, X2 (đều bậc I, cùng số nguyên tử cacbon trong phân tử, X1 là amin no mạch hở và phân tử X1 nhiều hơn phân tử X2 hai nguyên tử H) thu được 0,1 mol CO2. Mặt khác cho toàn bộ lượng X trên tác dụng với dung dịch HNO2 sinh ra 0,05 mol N2. Trong các khẳng định sau có bao nhiêu khẳng định đúng?
(1) Trong phân tử X2 có 7 liên kết σ và 1 liên kết π.
(2) Cả X1 và X2 phản ứng được với HNO2 cho sản phẩm hữu cơ tham gia phản ứng tráng bạc.
(3) Lực bazơ của X2 lớn hơn lực bazơ của X1.
(4) X1 và X2 đều có hai nguyên tử cacbon trong phân tử.
A. 1
B. 2
C. 3
D. 4
Cho hợp chất hữu cơ A gồm 2 nguyên tố, trong đó H chiếm 25% về khối lượng. Xác định công thức phân tử A, biết khối lượng mol của A bằng 16 g/mol
Xem chi tiết
mH=25%.16=4(g) -> nH=4/1=4(mol)
Hợp chất hữu cơ luôn có C -> Nguyên tố còn lại C -> mC=16-4=12(g)
=>nC=12/12=1(mol)
Vì: nC:nH=1:4 -> A: CH4 (Metan)
Đúng 1
Bình luận (0)
Trinitrotoluen là một loại thuốc nổ, có công thức phân tử C7H5N3O6, khi nổ tạo thành hỗn hợp khí cacbon monoxid, hơi nước, nitơ và muội than. (a) Viết phản ứng nổ của TNT. Lưu ý phản ứng nổ không phải là phản ứng cháy. (b) Hexanit là một loại chất nổ có chứa theo khối lượng 60% TNT và 40% HND (có công thức phân tử C12H5N7O12). Tính thành phần % theo khối lượng và theo số mol của các nguyên tố có trong Hexanit. Từ tỷ lệ số mol các nguyên tố, đề nghị các chất có thể tạo thành từ quá trình nổ Hexan...
Đọc tiếp
Trinitrotoluen là một loại thuốc nổ, có công thức phân tử C7H5N3O6, khi nổ tạo thành hỗn hợp khí cacbon monoxid, hơi nước, nitơ và muội than.
(a) Viết phản ứng nổ của TNT. Lưu ý phản ứng nổ không phải là phản ứng cháy.
(b) Hexanit là một loại chất nổ có chứa theo khối lượng 60% TNT và 40% HND (có công thức phân tử C12H5N7O12). Tính thành phần % theo khối lượng và theo số mol của các nguyên tố có trong Hexanit. Từ tỷ lệ số mol các nguyên tố, đề nghị các chất có thể tạo thành từ quá trình nổ Hexanit và tính hàm lượng % theo số mol của các chất đó.
(a) Phản ứng nổ của TNT: 2C7H5N3O6 → 3N2 + 5H2O + 7CO + 7C
(b) 100 gam thuốc nổ Hexanit có chứa 60 gam TNT và 40 gam HND.
Số mol của từng chất là:
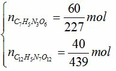
Áp dụng định luật bảo toàn nguyên tố ta có:
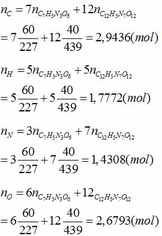
- Phần trăm khối lượng mỗi nguyên tố trong Hexanit:
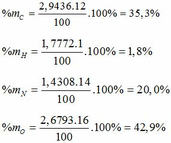
- Sản phẩm nổ của Hexanit là N2, H2O, CO, C
- Áp dụng định luật bảo toàn nguyên tố ta tính được số mol của các chất trong hỗn hợp sau khi nổ:
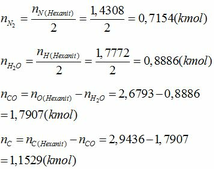
Phần trăm số mol của các chất trong hỗn hợp sau khi nổ:
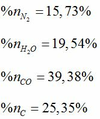
Đúng 0
Bình luận (0)
Đề 15:1) Nguyên tử Y nặng gấp hai lần nguyên tử Canxi. Tính nguyên tử khối của Y và cho biết Y thuộc nguyên tố nào ? Viết kí hiệu hóa học của nguyên tố đó.2) Thế nào là đơn chất ? Cố những loại đơn chất nào ? Cho VD. Nêu đặc điểm cấu tạo của đơn chất ?3) Thế nào là khối lượng mol ? Tính khối lượng mol của:a) Khí metan biết phan tử gồm 2C và 4H.b) khí sunfua biết phân tử gồm 2H và 1S.4) Đốt cháy m gam kim loại ngôm trong không khí cần tiêu tốn 9,6g oxi người ta thu được 20,4g nhôm oxita) Viết phư...
Đọc tiếp
Đề 15:
1) Nguyên tử Y nặng gấp hai lần nguyên tử Canxi. Tính nguyên tử khối của Y và cho biết Y thuộc nguyên tố nào ? Viết kí hiệu hóa học của nguyên tố đó.
2) Thế nào là đơn chất ? Cố những loại đơn chất nào ? Cho VD. Nêu đặc điểm cấu tạo của đơn chất ?
3) Thế nào là khối lượng mol ? Tính khối lượng mol của:
a) Khí metan biết phan tử gồm 2C và 4H.
b) khí sunfua biết phân tử gồm 2H và 1S.
4) Đốt cháy m gam kim loại ngôm trong không khí cần tiêu tốn 9,6g oxi người ta thu được 20,4g nhôm oxit
a) Viết phương trình phản ứng
b) Tìm khối lượng
Đề 16:
1) Hòa tan hoàn toàn 5,6g sắ ( Fe) vào dung dịch Axit clohidric ( HCl ) thu được sắt ( II ) clorua ( FeCl2 ) và khí Hidro ( H2)
a) Tính khối lượng của FeCl2 tạo thành sau phản ứng ?
b) Tính thể tích khí Hidro ( ở đktc ) tạo thành sau phản ứng ?
2) Để đốt cháy 16g chất X cần dùng 44,8 lít oxi ( ở đktc ) Thu được khí Co2 vào hơi nước theo tỉ lệ số mol 1:2. Tính khối lượng khí CO2 và hơi nước tạo thành ?
3) Thế nào là nguyên tử khối ? Tính khối lượng bằng nguyên tử cacbon của 5C, 11Na, 8Mg
4)Nguyên tử X nặng gấp 1,25 lần nguyên tử oxi. Tính nguyên tử khối của X và cho biết X thuộc nguyên tố nào? Viết kí hiệu hóa học của nguyên tố đó.
5) Hãy so sánh xem nguyên tử oxi nặng hay nhẹ hơn, bằng bao nhiêu lần so với :
a) Nguyên tử đồng
b) Nguyên tử C
6) Cho 5,6g sắt tác dụng hết với dung dịch axit clohidric ( HCl). Sau phản ứng thu được 12,7g sắt (II) clorua ( FeCl2) và 0,2g khí hidro ( đktc)
a) Lập PTHH của phản ứng trên.
b) Viết phương trình khối lượng của Phản ứng đã xảy ra
c) Tính khối lượng của axit sunfuric đã phản ứng theo 2 cách
Đề 15:
1) Theo đề bài , ta có:
NTK(Y)= 2.NTK(Ca)= 2.40=80 (đvC)
=> Nguyên tố Y là brom, KHHH là Br.
2) - Đơn chất là chất do 1nguyên tố tạo thành.
VD: O3; Br2 ; Cl2;......
- Hợp chất là những chất do 2 hay nhiều nguyên tố hóa học trở lên tạo thành.
VD: NaCl, KMnO4, CuSO4, H2O;....
3) Khôi lượng mol? tự trả lời đi !
a) Khối lượng mol của phân tử gồm 2C và 4H
Có nghĩa là khối lượng mol của C2H4
\(M_{C_2H_4}\)= 2.12+4.1=28 (g/mol)
\(M_{H_2S}\)=2.1+32=34(g/mol)
Đúng 1
Bình luận (0)
Hợp chất X có công thức C12H14O4. Từ X thực hiện các phản ứng (theo đúng tỉ lệ mol) (a) X + 2NaOH ® X1 + 2X2 (b) X1 + H2SO4 ® X3 + Na2SO4 (c) nX3 + nX4 ® poli(etylen terephtalat) + 2nH2O (d) X2 + X3 ® X5 + H2O Có các phát biểu: (1) Khi đốt cháy hoàn toàn 1 mol X1 cho 7 mol CO2. (2) Các chất X1, X2, X3 đều tác dụng được với Na. (3) Phân tử khối của X5 bằng 222. (4) Các chất X3 và X4 đều là hợp chất đa chức. (5) Phản ứng (c) thuộc loại ph...
Đọc tiếp
Hợp chất X có công thức C12H14O4. Từ X thực hiện các phản ứng (theo đúng tỉ lệ mol)
(a) X + 2NaOH ® X1 + 2X2
(b) X1 + H2SO4 ® X3 + Na2SO4
(c) nX3 + nX4 ® poli(etylen terephtalat) + 2nH2O
(d) X2 + X3 ® X5 + H2O
Có các phát biểu:
(1) Khi đốt cháy hoàn toàn 1 mol X1 cho 7 mol CO2.
(2) Các chất X1, X2, X3 đều tác dụng được với Na.
(3) Phân tử khối của X5 bằng 222.
(4) Các chất X3 và X4 đều là hợp chất đa chức.
(5) Phản ứng (c) thuộc loại phản ứng trùng hợp.
(6) Phân tử X5 có 3 liên kết π.
Số phát biểu đúng là
A. 4.
B. 2.
C. 5.
D. 3.













