Đề hidro hóa hỗn hợp A gồm: C2H6, C3H8 , C4H10. Sau một thời gian thu được hỗn hợp khí B, dA/B =1,75. % ankan bị đề hidro hóa là:
A. 50%
B. 75%
C. 25%
D. 90%
Hỗn hợp khí gồm etan và propan có tỉ khối hơi so với hidro là 20,25 được nung trong bình kín với chất xúc tác để thực hiện phản ứng đề hidro hóa. Sau một thời gian thu được hỗn hợp khí có tỉ khối hơi so với hidro là 16,2 gồm ankan, anken và hidro. Biết rằng tốc độ phản ứng của etan và propan như nhau, hiệu suất phản ứng đề hidro hóa là?
A. 25%
B. 30%
C. 40%
D. 50%
Hoàn toàn tương tự bài toán trước. Có thể tự chọn lượng chất rồi bảo toàn khối lượng cho phản ứng, hoặc một cách nhanh hơn là áp dụng công thức:

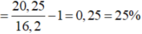
Vậy đáp án đúng là A
Hỗn hợp khí gồm etan và propan có tỉ khối so với hidro là 20,25 được nung trong bình với chất xúc tác để thực hiện phản ứng đề hidro hóa. Sau 1 thời gian thu được hỗn hợp khí có tỉ khối so với hidro là 16,2 gồm các ankan, anken và hidro. Tính hiệu suất phản ứng đề hidro hóa biết rằng tốc độ phản ứng của etan và propan là như nhau?
A. 30%
B. 50%
C. 25%
D. 40%
Đáp án : C
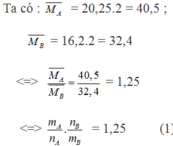
Áp dụng định luật bảo toàn khối lượng ta có: mA = mB
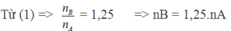
Giả sử ban đầu có 1 mol hỗn hợp A => nB = 1,25.1 = 1,25 mol
Trong phản ứng đề hidro hóa: số mol hỗn hợp sau phản ứng tăng, số mol tăng của hỗn hợp B so với hỗn hợp A chính là số mol các chất phản ứng
=> H = (1,25-1) .100% = 25%
Hỗn hợp khí gồm etan và propan có tỉ khối so với hidro là 20,25 được nung trong bình với chất xúc tác để thực hiện phản ứng đề hidro hóa. Sau một thời gian thu được hỗn hợp khí có tỉ khối so với hidro là 16,2 gồm có các ankan, anken và hidro. Tính hiệu suất phản ứng đề hidro biết rằng tốc độ phản ứng của etan và propan là như nhau?
A. 30%
B. 50%
C. 25%
D. 40%
Đáp án C
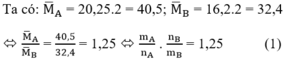
Áp dụng định luật bảo toàn khối lượng ta có: mA = mB
![]()
Giả sử ban đầu có 1 mol hỗn hợp A => nB = 1,25.1 = 1,25 mol
Trong phản ứng đề hidro hóa: số mol hỗn hợp khí sau phản ứng tăng, số mol tăng của hỗn hợp B so với hỗn hợp A chính là số mol các chất phản ứng.
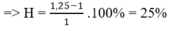
Đốt cháy hoàn toàn 8,8 g hỗn hợp 2 ankan X,Y ở thể khí ,cho 13,44 lít CO2 (đktc), biết thể tích 2 ankan trong hỗn hợp bằng nhau. X,Y có công thức phân tử là :
A. C2H6 và C4H10 B. C2H6 và C3H8 C. CH4 và C4H10 D. Kết quả khác
Đặt :
nX = nY = x (mol)
CT : CnH2n+2 , CmH2m+2
nCO2 = 13.44/22.4 = 0.6 (mol)
BT C :
x(n+m) = 0.6 (1)
mhh = x(14n + 2) + x(14m + 2) = 8.8
=> 14x(n+m) + 4x = 8.8
=> 14*0.6 + 4x = 8.8
=> x = 0.1
Từ (1) => n + m = 0.6/0.1 = 6
BL : n = 2 , m = 4 => C2H6 , C4H8
n = 1 , m = 5 => CH4 , C5H12
hỗn hợp A gồm CH4 và o2, biết tỉ khối của A so với hidro là 12. a) tính % theo số mol của mỗi chất khí trong hỗn hợp. b) đốt hỗn hợp A thấy có tiếng nổ. Sau một thời gian làm lạnh sản phẩm thu được hỗn hợp khí B và chất lỏng C biết H=60% -tính % theo thể tích chất trong B -tính khối lượng chất lỏng C
a, Gọi: \(\left\{{}\begin{matrix}n_{CH_4}=x\left(mol\right)\\n_{O_2}=y\left(mol\right)\end{matrix}\right.\)
Có: \(d_{A/H_2}=12\Rightarrow\dfrac{16x+32y}{x+y}=12.2\)
\(\Rightarrow x=y\)
\(\Rightarrow\%n_{CH_4}=\%n_{O_2}=50\%\)
b, PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
Coi x = y = 1 (mol)
Xét tỉ lệ: \(\dfrac{1}{1}>\dfrac{1}{2}\), ta được CH4 dư nếu pư hoàn toàn.
Theo PT: \(\left\{{}\begin{matrix}n_{CH_4\left(pư\right)\left(LT\right)}=n_{CO_2\left(LT\right)}=\dfrac{1}{2}n_{O_2}=0,5\left(mol\right)\\n_{H_2O\left(LT\right)}=n_{O_2}=1\left(mol\right)\end{matrix}\right.\)
Mà: H = 60%
\(\Rightarrow\left\{{}\begin{matrix}n_{CH_4\left(pư\right)\left(TT\right)}=n_{CO_2\left(TT\right)}=0,5.60\%=0,3\left(mol\right)\\n_{H_2O\left(TT\right)}=1.60\%=0,6\left(mol\right)\end{matrix}\right.\)
B gồm: CH4 (dư): 1 - 0,3 = 0,7 (mol); CO2: 0,3 (mol), O2: 1 - 1.60% = 0,4 (mol)
Ở cùng điều kiện nhiệt độ, áp suất thì %V cũng là %n
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,7}{0,7+0,3+0,4}.100\%=50\%\\\%V_{CO_2}=\dfrac{0,3}{0,7+0,3+0,4}.100\%\approx21,4\%\\\%V_{O_2}\approx28,6\%\end{matrix}\right.\)
mH2O = 0,6.18 = 10,8 (g)
1. Phần trăm khối lượng C trong phân tử của Ankan Y là 83,33%. Công thức phân tử của Y là
A. C2H6
B. C3H8
C. C4H10
D. C5H12
2. Đốt cháy hoàn toàn một hỗn hợp hidro cacbon thu được 2,24 lít khí CO2 đktc và 2,7g H2O. Tính Thể tích Oxi đã tham gia phản ứng cháy
3. Đốt hỗn hợp X gồm 2 ankan kế tiếp trong dãy đồng đẳng được 24,2g CO2 và 12,6g H2O. Tìm CTPT của 2 ankan
Câu 1:
Gọi CTTQ của ankan là CnH2n+2
Ta có
12n/14n+2=83,33%
=> n=5
Vậy CTPT của Y là C5H12
Câu 2:
Ta có:
nCO2 = 0,1 mol
nH2O = 0,15 mol
Bảo toàn nguyên tố O:
2.nO2 = 2.nCO2 + nH2O
=> nO2 = (2nCO2 + nH2O)/ 2 = 0,175 mol
=> VO2 = 0,175.22,4 = 3,92l
Câu 3:
Gọi CTQT là CnH2n+2
Ta có:
nCO2 = 0,55mol
nH2O = 0,7mol
=> nhh = 0,7 - 0,55 = 0,15mol
n = nCO2 / nhh = 3,667
Vậy CTPT của 2 ankan là C3H8 và C4H10
Khi crackinh nhiệt đối với 1 mol octan, thu được hỗn hợp X gồm CH4 15%; C2H4 50%; C3H6 25% còn lại là C2H6, C3H8, C4H10 (theo thể tích). Thể tích dung dịch Br2 1M cần phản ứng vừa hỗn hợp X là
A. 3 mol
B. 1 mol
C. 2 mol.
D. 4 mol
Hỗn hợp khí A gồm hidro, oxi và khí NOx. Trong đó hidro chiếm 50%, oxi chiếm 25% ,NOx chiếm 25% về thể tích (ở đktc). Biết trong 1 mol hỗn hợp A có 11,5 gam khí NOx. Tính:
a) Số mol mỗi chất có trong 1 mol hỗn hợp A? Xác định công thức hóa học và đọc tên của NOx?
b) Tỉ khối của A đối với không khí?
a) Trong 1 mol A có 0,25 mol NOx, 0,25 mol O2, 0,5 mol H2
Có \(M_{NO_x}=\dfrac{11,5}{0,25}=46\left(g/mol\right)\)
=> x = 2
=> NOx là NO2 (Nito đioxit)
b) \(\overline{M}_A=\dfrac{0,5.2+0,25.32+0,25.46}{1}=20,5\left(g/mol\right)\)
=> \(d_{A/kk}=\dfrac{20,5}{29}=0,707\)
a)Giả sử có 1mol hhA.
\(\%V_{H_2}=50\%=\%n_{H_2}\)\(\Rightarrow n_{H_2}=1\cdot50\%=0,5mol\)
\(\%V_{O_2}=25\%=\%n_{O_2}\Rightarrow n_{O_2}=1\cdot25\%=0,25mol\)
\(n_{NO_x}=1-0,5-0,25=0,25mol\)
\(M_{NO_x}=\dfrac{m}{n}=\dfrac{11,5}{0,25}=46đvC\)
\(\Rightarrow14+16x=46\Rightarrow x=2\)
Vậy CTHH cần tìm là \(NO_2:nitođioxit\)
b)\(\overline{M_A}=\dfrac{m_{H_2}+m_{O_2}+m_{NO_x}}{n_{H_2}+n_{O_2}+n_{NO_x}}=\dfrac{0,5\cdot2+0,25\cdot32+0,25\cdot46}{0,5+0,25+0,25}=20,5đvC\)
\(d_A\)/KK=\(\dfrac{20,5}{29}=0,71\)
Nung hỗn hợp rắn A gồm a mol Mg và 0,25 mol Cu(NO3)2 sau một thời gian thu được chất rắn B và 10,08 lit khí hỗn hợp D gồm NO2 và O2. Hòa tan hoàn tòa B vào dung dịch chứa 1,3 mol HCl (vừa đủ), thu được dung dịch X chỉ chứa m gam hỗn hợp muối clorua và 1,12 lit hỗn hợp khí Y gồm N2 và H2 có tỉ khối so với hidro là 11,4. Biết các thể tích đều ở dktc. Giá trị của m gần nhất với :
A. 70,5
B. 71,0
C. 71,5
D. 72,0
Đáp án D
nD = 0,45 => nO(D) = 0,9 mol
nY = 0,05 mol
Đặt nN2 = x => nH2 = 0,05 – x
=> 28x + 2(0,05 – x) = 0,05.11,4.2 = 1,14
=> x = 0,04 mol
=> nN2 = 0,04 mol và nH2 = 0,01 mol
Trong Y chứa khí H2 chứng tỏ NO3- hết
Hỗn hợp muối clorua gồm : a mol MgCl2 ; 0,25 mol CuCl2 ; NH4Cl
Bảo toàn Clo : nNH4Cl = 1,3 – 2a – 0,5 = 0,8 – 2a
Bảo toàn H : nH2 = ½ (nHCl + 4nNH4Cl – 2nH2) = 4a – 0,96
Bảo toàn O : nO (Cu(NO3)2) = nO(D) + nO(H2O) => 0,25.6 = 0,9 + 4a – 0,96
=> a = 0,39 mol
=> m = 0,39.95 + 0,25.135 + (0,8 – 2.0,39). 53,5 = 71,87g