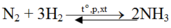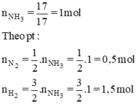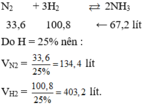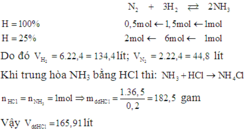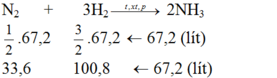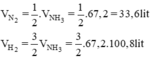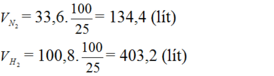Phải dùng bao nhiêu lít khí nitơ và bao nhiêu lít khí hiđro để điều chế 17,0 gam NH3? Biết rằng hiệu suất chuyển hóa thành amoniac là 25%?
A. 22,4 lít N2 và 67,2 lít H2
B. 22,4 lít N2 và 134,4 lít H2
C. 44,8 lít N2 và 67,2 lít H2
D. 44,8 lít N2 và 134,4 lít H2