Cho 0,2 gam một muối canxi halogen (A) tác dụng với một lượng dư dung dịch A g N O 3 thì thấy thu được 0,376 gam kết tủa bạc halogenua. Công thức của muối A là
A. C a F 2 .
B. C a C l 2 .
C. C a B r 2 .
D. C a I 2 .
Chất A là muối Canxi halogenua. Dung dịch chứa 0,200 gam A tác dụng với lượng dư dung dịch bạc nitrat thì thu được 0,376 gam kết tủa bạc halogenua. Công thức phân tử của chất A là
A. CaF2
B. CaCl2
C. CaBr2
D. CaI2
Đáp án C
Gọi công thức muối là CaX2
CaX2 + 2AgNO3 → Ca(NO3)2 +2AgX
40+2X 2.(108+X)
0,2 0,376
Ta có → X=80 (Br)
Công thức. CaBr2
Cho A là muối canxi halogenua.Cho dung dịch chứa 0,2 g A tác dụng lượng dư thừa bạc nitrat thì thu được 0,376 g kết tủa bạc halogenua .Hãy xác định công thức của A
Cho 3,09 gam muối natri halogenua (X) tác dụng với dung dịch A g N O 3 dư thì thu được một kết tủa, kết tủa này sau khi phân hủy hoàn toàn cho 3,24 gam bạc. Công thức của muối X là
A. NaF
B. NaBr
C. NaI
D. NaCl
Chọn đáp án B
NaY + A g N O 3 → A g N O 3 + AgY
2AgY → 2Ag + Y 2
n N a Y = n A g Y = n A g = = 0,03 (mol
0,03(23+ M Y ) = 3,09 => M Y = 80 (Br)
Cho 1,03 gam muối natri halogenua (X) tác dụng với dung dịch A g N O 3 dư thì thu được một kết tủa, kết tủa này sau khi phân hủy hoàn toàn cho 1,08 gam bạc. Công thức của muối X là
A. NaF
B. NaBr
C. NaI
D. NaCl
Chọn đáp án B
NaY + A g N O 3 → N a N O 3 + AgY
2AgY → 2Ag + Y 2
n N a Y = n A g Y = n A g = = 0,01 (mol)
=> 0,01(23 + M Y ) = 1,03 => M Y = 80 (Br)
Cho 1,03 gam muối natri halogenua (A) tác dụng với dung dịch AgNO3 dư thì thu được một kết tủa, kết tủa này sau khi phân hủy hoàn toàn cho 1,08 gam bạc. Xác định tên muối A.
nAg = 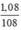 = 0,01 mol
= 0,01 mol
Phương trình hóa học của phản ứng:
Đặt X là kí hiệu, nguyên tử khối của halogen
NaX + AgNO3 → AgX↓ + NaNO3
0,01mol 0,01mol
2AgX → 2 Ag + X2
0,01mol 0,01mol
Theo pt: nNaX = nAgX = nAg = 0,1 mol
MNaX = 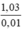 = 103 → X = 103 – 23 = 80 (Br)
= 103 → X = 103 – 23 = 80 (Br)
Muối A có công thức phân tử là NaBr
Cho 14,9 gam muối kali halogenua (X) tác dụng với dung dịch A g N O 3 dư thì thu được 28,7 gam một kết tủa. Công thức của muối X là
A. KF
B. KBr
C. KI
D. KCl
Chọn đáp án D
KY + A g N O 3 → K N O 3 + AgY ↓
n K Y = n A g Y => 14 , 9 39 + Y = 28 , 7 108 + Y => Y = 35,5 (Cl) => Muối X là KCl
cho 1,03 gam muối natri halogenua (A) tác dụng với dung dịch AgNO3 dư thì thu được 1 kết tủa , kết tủa này sau khi phân hủy hoàn toàn cho 1,08 gam bạc . Xác định tên của muối A .
nAg=0,01 mol
NaX+AgN03------->NaN03+AgX,áp dụng bảo toàn nguyên tố Ag,nAg sau=nAg truoc
0,01--------------------------------0,01
MNaX=1,03/0,01=103------------------->X=80------->Br
từ đâu bạn lại suy ra nAg là 0,01 mol và nAg sau lại bằng nAg trước
Cho 1,5 gam muối natri halogenua tác dụng với 10 ml dung dịch bạc nitrat, sau khi phản ứng xảy ra người ta thu được 2,35 gam kết tủa. Xác định công thức của muối natri halogenua và nồng độ mol của dung dịch AgNO3
Tăng giảm khối lượng ta có; $n_{NaX}=\frac{2,35-1,5}{108-23}=0,01(mol)$
$\Rightarrow M_{NaX}=150\Rightarrow X=127$
Vậy CTHH của muối là NaI
Bảo toàn nguyên tố X và Ag ta có: $n_{AgNO_3}=n_{AgI}=0,01(mol)\Rightarrow C_{M}=1M$
PTHH: \(NaX+AgNO_3\rightarrow NaNO_3+AgX\downarrow\)
Theo PTHH: \(n_{NaX}=n_{AgX}\)
\(\Rightarrow\dfrac{1,5}{23+X}=\dfrac{2,35}{108+X}\) \(\Leftrightarrow X=127\) (Iot)
\(\Rightarrow\) Công thức: NaI
Ta có: \(n_{AgNO_3}=n_{NaI}=\dfrac{1,5}{150}=0,01\left(mol\right)\)
\(\Rightarrow C_{M_{AgNO_3}}=\dfrac{0,01}{0,01}=1\left(M\right)\)
1)Dung dịch HI không phản ứng được với dung dịch
A. NaOH B. Na2O3 C. H2SO4 D. NaCl
2)Hoà tan 6,5gam kim loại R trong dung dịch HCl dư thì thu được 2,24 lít khí H2. R là:
A. Fe B. Zn C. Mg D. Al
3)Trộn 0,2 lít dung dịch HCl 1M với 0,3 lít dung dịch HCl 2M thì thu được dung dịch có nồng độ mol/lít là:
A. 1,5M B. 1,2M C. 1,6M D. 0,15M
4)Chất M là muối canxi halogenua. Cho dung dịch chứa 0,2 gam M tác dụng với lượng dư bạc nitrat thì thu được 0,376 gam kết tủa thu được là:
A. CaF2 B. CaCl2 C. CaBr2 D. CaI2
5)Cho lượng dung dịch AgNO3 tác dụng với 100ml dung dịch chứa hỗn hợp NaF 0,05M và NaCl 0,2M. Khối lượng kết tủa thu được là:
A. 2,56 gam B. 2,72 gam C.2,87 gam D. 2,93 gam
giải ra giúp mình với
1)
2) Có: \(n_{H_2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
Gỉa sử R có hóa trị n.
PTHH:
\(2R+2nHCl\rightarrow2RCl_n+nH_2\)
\(\frac{0,2}{n}--------->0,1\)
\(\Rightarrow R=\frac{6,5}{\frac{0,2}{n}}=32,5n\)
Biện luận R theo n ta được: R = 65 (Kẽm - Zn) khi n = 2.
==> Chọn B.
3) Ta có: \(n_{HCl}=0,2.1+0,3.2=0,8\left(mol\right);V_{HCl}=0,2+0,3=0,5\left(l\right)\)
\(\Rightarrow C_MHCl=\frac{0,8}{0,5}=1,6\left(M\right)\)
==> Chọn C.
4) PTHH:
\(CaX_2+2AgNO_3\rightarrow Ca\left(NO_3\right)_2+2AgX\downarrow\)
\(1--------------->2\)
Theo phương trình: \(n_{AgX}=2n_{CaX_2}\)
Hay: \(2.\frac{0,2}{40+2X}=\frac{0,376}{108+X}\Leftrightarrow X=80\left(Brom\right)\)
Vậy M là: \(CaBr_2\)