Cho 46,4g sắt oxit phản ứng hoàn toàn với khí CO nung nóng thu được hỗn hợp khí A. Dẫn hỗn hợp A vào 500ml dung dịch Ba(OH)2 1M thu được 39,4g kết tủa. Hãy xác định công thức sắt oxit

Những câu hỏi liên quan
Cho 47,4g sắt oxit phản ứng hoàn toàn với khí CO nung nóng thu được hỗn hợp khí A. Dẫn hỗn hợp A vào 500ml dung dịch Ba(OH)2 1M thu được 39,4g kết tủa. Hãy xác định công thức sắt oxit
Nung nóng 18,56 gam hỗn hợp A gồm FeCO3 và một oixt sắt FexOy trong không khí tới khi phản ứng xảy ra hoàn toàn, thu được khí CO2 và 16 gam một oxit sắt duy nhất. Cho khí CO2 hấp thụ hết vào dung dịch Ba(OH)2 dư thu được 15,76 gam kết tủa. Vậy công thức oxit FexOy là: A. FeO B. Fe3O4 C. Fe2O3 D. Fe2O3 hoặc FeO
Đọc tiếp
Nung nóng 18,56 gam hỗn hợp A gồm FeCO3 và một oixt sắt FexOy trong không khí tới khi phản ứng xảy ra hoàn toàn, thu được khí CO2 và 16 gam một oxit sắt duy nhất. Cho khí CO2 hấp thụ hết vào dung dịch Ba(OH)2 dư thu được 15,76 gam kết tủa. Vậy công thức oxit FexOy là:
A. FeO
B. Fe3O4
C. Fe2O3
D. Fe2O3 hoặc FeO
Các oxit sắt, nung ngoài không khí đến khối lượng không đổi luôn tạo thành Fe2O3 16 gam oxit sắt duy nhất là Fe2O3.
Cách 1: Phương pháp đại số
Đặt số mol các chất trong 18,56 gam A F e C O 3 : n ; F e x O y : m
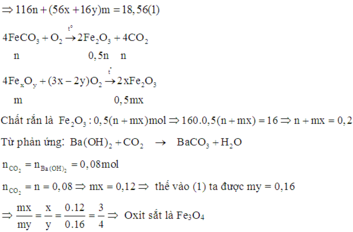
Cách 2: Phương pháp bảo toàn
Đặt số mol các chất trong 18,56 gam A F e C O 3 : n ; F e x O y : m
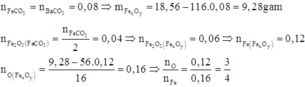
Cách 3: Bảo toàn nguyên tử C và O:
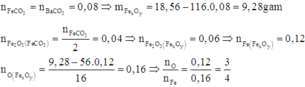
⇒ Oxit của sắt là Fe3O4
Cách 4: Bảo toàn nguyên tử và khối lượng:
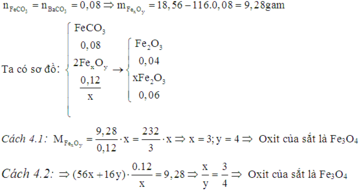
Đáp án B.
Đúng 0
Bình luận (0)
Bài 1: Cho 3,6g một oxit sắt vào dung dịch HCl dư. Sau khi phản ứng xảy ra hoàn toàn thu được một muối sắt clorua. Hãy xác định công thức phân tử của oxit sắtBài 2: Dẫn 5,61 lít (đktc) hỗn hợp 2 khí CO và H2 từ từ qua hỗn hợp 2 oxit CuO và FeO nung nóng lấy dư, sau phản ứng thấy khối lượng hỗn hợp giảm a gama) Viết các PTHHb) Tính ac) Tính % theo thể tích của cá khí, biết tỉ khối hỗn hợp khí so với khí CH4 là 0,4
Đọc tiếp
Bài 1: Cho 3,6g một oxit sắt vào dung dịch HCl dư. Sau khi phản ứng xảy ra hoàn toàn thu được một muối sắt clorua. Hãy xác định công thức phân tử của oxit sắt
Bài 2: Dẫn 5,61 lít (đktc) hỗn hợp 2 khí CO và H2 từ từ qua hỗn hợp 2 oxit CuO và FeO nung nóng lấy dư, sau phản ứng thấy khối lượng hỗn hợp giảm a gam
a) Viết các PTHH
b) Tính a
c) Tính % theo thể tích của cá khí, biết tỉ khối hỗn hợp khí so với khí CH4 là 0,4
Xem thêm câu trả lời
Hỗn hợp A gồm sắt và oxit sắt có khối lượng 2,6 gam. Cho khí CO đi qua A đun nóng, rồi dẫn toàn bộ khí thu được vào dung dịch nước vôi trong dư thì thu được 10gam kết tủa. Hãy xác định oxit sắt?
Nung 9,28 gam hỗn hợp A gồm FeCO3 và một oxit sắt trong không khí đến khối lượng không đổi. Sau khi phản ứng xảy ra hoàn toàn, thu được 8 gam một oxit sắt duy nhất và khí CO2. Hấp thụ hết lượng khí CO2 vào 300 ml dung dịch Ba(OH)2 0,1M, kết thúc phản ứng thu được 3,94 gam kết tủa. Tìm công thức hoá học của oxit sắt. A. FeO B. Fe2O3 C. Fe3O4 D. FeO hoặc Fe2O3
Đọc tiếp
Nung 9,28 gam hỗn hợp A gồm FeCO3 và một oxit sắt trong không khí đến khối lượng không đổi. Sau khi phản ứng xảy ra hoàn toàn, thu được 8 gam một oxit sắt duy nhất và khí CO2. Hấp thụ hết lượng khí CO2 vào 300 ml dung dịch Ba(OH)2 0,1M, kết thúc phản ứng thu được 3,94 gam kết tủa. Tìm công thức hoá học của oxit sắt.
A. FeO
B. Fe2O3
C. Fe3O4
D. FeO hoặc Fe2O3
Đáp án C
Gọi công thức tổng quát của oxit sắt là FxOy ( x, y ∈ N*)
PTHH: 4FeCO3 + O2 → t 0 2Fe2O3 + 4CO2 (1)
2FxOy + 3 x - 2 y 2 O2 → t 0 xFe2O3 (2)
n F e 2 O 3 = 8 160 = 0 , 05 m o l n B a ( O H ) 2 = 0 , 3 . 0 , 1 = 0 , 03 m o l n B a C O 3 = 3 , 94 197 = 0 , 02 m o l
Cho CO2 vào dung dịch Ba(OH)2
PTHH: CO2 + Ba(OH)2 → BaCO3 (3)
Có thể: 2CO2 + Ba(OH)2 → Ba(HCO3)2 (4)
Trường hợp 1: Xảy ra các phản ứng 1, 2, 3
Theo PT(1), (3): n F e C O 3 = n C O 2 = n B a C O 3 = 0 , 02 m o l
Theo (1):
n
F
e
2
O
3
=
1
2
n
F
e
C
O
3
=
0
,
01
m
o
l
⇒
n
F
e
2
O
3
(
p
ư
2
)
=
0
,
05
-
0
,
01
=
0
,
04
m
o
l
Theo PT(2): n F e x O y = 2 x n F e C O 3 = 2 x . 0 , 04 = 0 , 08 x m o l
Theo bài ra: mhỗn hợp = m F e C O 3 + m F e x O y = 9 , 28 g a m
⇔ 0 , 02 . 116 + 0 , 08 x . 56 x + 16 y = 9 , 28 ⇔ x y = 16 31 ( l o ạ i )
Trường hợp 2: Xảy ra các phản ứng 1, 2, 3, 4
Theo PT (3):
n C O 2 = n B a C O 3 = 0 , 02 m o l n C O 2 ( p ư 4 ) = 2 ( 0 , 03 - 0 , 02 ) = 0 , 02 m o l ⇒ ∑ n C O 2 = 0 , 04 m o l
Theo PT(1), (3): n F e C O 3 = n C O 2 = 0 , 04 m o l
Theo (1): n F e 2 O 3 = 1 2 n F e C O 3 = 0 , 02 m o l
⇒ n F e 2 O 3 ( 2 ) = 0 , 05 - 0 , 02 = 0 , 03 m o l
Theo PT(2): n F e x O y = 2 x n F e 2 O 3 = 2 x . 0 , 03 = 0 , 06 x m o l
Theo bài ra: mhỗn hợp = m F e C O 3 + m F e x O y = 9 , 28 g a m
⇔ 0 , 04 . 116 + 0 , 06 x . ( 56 x + 16 y ) = 9 , 28 ⇔ x y = 3 4 ⇒ x = 3 ; y = 4
Vậy công thức oxit sắt là Fe3O4 ( sắt từ oxit)
Đúng 0
Bình luận (0)
Cho V lít khí CO đktc đi qua ống sứ chứa 2,32g oxit sắt kim loại nung nóng đến phản ứng hoàn toàn thu được m gam kim loại và hỗn hợp khí có tỉ khối so với H2 bằng 18.Dẫn toàn bộ lượng khí này vào bình chứa 2000ml dung dịch Ca(OH)2 0,015M.Kết thúc phản ứng thu được 2g kết tủa và dung dịch A.Lọc tách kết tủa rồi cho dung dịch Ba(OH)2 dư vào dung dịch A ta thu được p gam kết tủa.Cho toàn bộ lượng kim loại thi được ở trên vào bình chứa dung dịch HCl dư,phản ứng kết thúc ta thu được 0,672 lít khí H2...
Đọc tiếp
Cho V lít khí CO đktc đi qua ống sứ chứa 2,32g oxit sắt kim loại nung nóng đến phản ứng hoàn toàn thu được m gam kim loại và hỗn hợp khí có tỉ khối so với H2 bằng 18.Dẫn toàn bộ lượng khí này vào bình chứa 2000ml dung dịch Ca(OH)2 0,015M.Kết thúc phản ứng thu được 2g kết tủa và dung dịch A.Lọc tách kết tủa rồi cho dung dịch Ba(OH)2 dư vào dung dịch A ta thu được p gam kết tủa.Cho toàn bộ lượng kim loại thi được ở trên vào bình chứa dung dịch HCl dư,phản ứng kết thúc ta thu được 0,672 lít khí H2 đktc.Viết các PTHH xảy ra.Tính C,m,p và xác định CT của oxit kim loại
Thổi 8,96 lít CO (đktc) qua 16 gam một oxit sắt nung nóng. Dẫn toàn bộ khí sau phản ứng qua dung dịch Ca(OH)2 dư, thấy tạo ra 30 gam kết tủa trắng CaCO3, các phản ứng xảy ra hoàn toàn.
1) Tính khối lượng Fe thu được.
2) Xác định công thức oxit sắt.
a) nCaCO3 = 0.3 (mol)
CO + O => CO2
=> nO = 0.3 (mol)
mFe = moxit - mO = 16 - 0.3*16 = 11.2 (g)
nFe = 11.2/56 = 0.2 (mol)
nFe : nO = 0.2 : 0.3 = 2 : 3
CT oxit : Fe2O3
Đúng 1
Bình luận (1)
nCO= 0,4(mol)
yCO + FexOy \(\rightarrow\) xFe + yCO2 (phản ứng có nhiệt độ) (1)
CO2 + Ca(OH)2 \(\rightarrow\) CaCO3 + H2O (2)
nCaCO3= nCO2(2) = nCO2(1) = 0,3(mol)
nCO2 = nCO = 0,3(mol) => CO dư (0,4-0,3=0,1(mol))
1, Áp dụng định luật bảo toàn khối lượng, ta có:
mCO + mFexOy = mFe + mCO2
=> mfe = mCO + mfexOy - mCO2
\(\Leftrightarrow\) mfe = 0,3.28+ 16 - 0.3.44 = 11,2 (g)
2, Áp dụng định luật bảo toàn nguyên tố Fe, ta có
nFe(sau phản ứng) = nfe(fexOy) = \(\dfrac{11,2}{56}\)= 0,2(mol)
=> mFe(FexOy) = 11,2(g) => mO(fexOy) = 16-11,2= 4,8(g)
=> ta có: \(\dfrac{56x}{16y}\) = \(\dfrac{11,2}{4,8}\)\(\Rightarrow\)\(\dfrac{x}{y}\)=\(\dfrac{2}{3}\)
Vậy công thức oxit sắt là Fe2O3
Thấy ok là phải tích cho tui đó nhá=.=
Đúng 1
Bình luận (1)
Khử một oxit sắt bằng khí CO trong binh kín sau khi phản ứng kết thúc thu được chất rắn A và hỗn hợp khí B. Hòa tan chất rắn A trong 300g dung dịch axit H2SO4 49%, để kết tủa hoàn toàn dung dịch muối thu được cần dùng 500ml dung dịch Ba(OH)2 3M, đem kết tủa nung đến khối lượng không đổi thu được 376,5 g chất rắn. Mặt khác dẫn hỗn hợp khí B qua 500ml dung dịch Ca(OH)2 3,5M thì thu được 150 g kết tủa. Tìm công thức hóa học và tên gọi oxit sắt.
Đọc tiếp
Khử một oxit sắt bằng khí CO trong binh kín sau khi phản ứng kết thúc thu được chất rắn A và hỗn hợp khí B. Hòa tan chất rắn A trong 300g dung dịch axit H2SO4 49%, để kết tủa hoàn toàn dung dịch muối thu được cần dùng 500ml dung dịch Ba(OH)2 3M, đem kết tủa nung đến khối lượng không đổi thu được 376,5 g chất rắn. Mặt khác dẫn hỗn hợp khí B qua 500ml dung dịch Ca(OH)2 3,5M thì thu được 150 g kết tủa. Tìm công thức hóa học và tên gọi oxit sắt.
Cho V lít CO (ở đktc) từ từ đi qua ống sứ nung nóng đựng 23,2 gam một oxit sắt đến khi phản ứng xảy ra hoàn toàn thu được hỗn hợp khí A có tỉ khối so với hiđro bằng 18. Dẫn hỗn hợp khí A đi qua dung dịch nước vôi trong dư thu được 40 gam kết tủa. Tìm công thức của oxit sắt và tính V
\(M_A=18.2=36\left(g/mol\right)\)
Áp dụng sơ đồ đường chéo:
\(\dfrac{n_{CO}}{n_{CO_2}}=\dfrac{44-36}{36-28}=\dfrac{1}{1}\)
\(n_{CaCO_3}=\dfrac{40}{100}=0,4\left(mol\right)\)
Đặt CTHH của oxit sắt là \(Fe_xO_y\)
PTHH:
\(Fe_xO_y+yCO\xrightarrow[]{t^o}xFe+yCO_2\) (1)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\) (2)
Theo PT (2): \(n_{CO_2}=n_{CaCO_3}=0,4\left(mol\right)\)
\(\Rightarrow n_{CO\left(d\text{ư}\right)}=n_{CO_2}=0,4\left(mol\right)\)
Theo PT (1): \(n_{Fe_xO_y}=\dfrac{1}{y}.n_{CO_2}=\dfrac{0,4}{y}\left(mol\right);n_{CO\left(p\text{ư}\right)}=n_{CO_2}=0,4\left(mol\right)\)
\(\Rightarrow M_{Fe_xO_y}=\dfrac{23,2}{\dfrac{0,4}{y}}=86y\left(g/mol\right)\\ \Rightarrow56x+16y=86y\\ \Leftrightarrow\dfrac{x}{y}=\dfrac{3}{4}\)
=> CT của oxit là Fe3O4
V = (0,4 + 0,4).22,4 = 17,92 (l)
Đúng 1
Bình luận (0)


















