Hợp chất A chứa nguyên tố: Fe và O. Trong phân tử A có 7 nguyên tử và M A = 232 (g/mol). Tìm công thức hoá học của A?
(Cho biết : S = 32 ; O = 16; Al = 27; H = 1; Fe = 56; C = 12)
Câu 3 (1 điểm): Hợp chất A chứa nguyên tố: Fe và O . Trong phân tử A có 7 nguyên tử và MA = 232 (g/mol). Tìm công thức hoá học của A? (Cho biết : S = 32 ; O = 16; Al = 27; H = 1; Fe = 56; C = 12)
CTHH của A : $Fe_xO_y$
Ta có : $x + y = 7$
$M_A = 56x + 16y = 232$
Suy ra : x = 3 ; y = 4
Vậy CTHH là $Fe_3O_4$
câu 1 công thức hóa học của nguyên tố A với O là A2O ; công thức hóa học của nguyên tố B với H là BH2. Tìm công thức hóa học của hợp chất gồm nguyên tố A và B
Câu 2 trong 1 hợp chất được tạo bởi 2 nguyên tử nguyên tố R và 5 nguyên tử nguyên tố OXI .Tìm nguyên tử khối và tên nguyên tố R .Biết hợp chất này nặng hơn phân tử Hidro 71 lần
(cho biết H=1;C=12;O=16;P=31;S=32;Ca=40;Fe=56;Cu=64)
Câu 6. Công thức hoá học của hợp chất tạo bởi S (IV) và O là A. S2O. B. S2O3. C. SO3. D. SO2. Câu 7. Công thức hoá học của hợp chất tạo bởi Al (III) và nhóm (SO4) (II) là A. Al2SO4. B. Al2(SO4)3. C. Al3(SO4)2. D. AlSO4. Câu 8. Công thức hoá học của hợp chất tạo bởi K (I) và nhóm (PO4) (III) là A. KPO4. B. K2PO4. C. K(PO4)3. D. K3PO4. Câu 9. Cho biết công thức hóa học hợp chất của nguyên tố X với oxi và hợp chất của nguyên tố Y với H như sau (X, Y là những nguyên tố nào đó): X2O3, YH3. Công thức hóa học đúng cho hợp chất giữa X và Y là A. X2Y B. XY2 C. XY D. X2Y3 Câu 10. Hai nguyên tử X kết hợp với 3 nguyên tử Oxi tạo ra phân tử chất A. Trong phân tử, X chiếm 70% khối lượng. Kí hiệu hóa học của nguyên tố X là A. Al. B. Fe. C. Cr. D. P. -------- ( tự luận nha)
Cho biết thành phần theo khối lượng của một số hợp chất, hãy tìm công thức hóa học của chúng:
- Hợp chất A: 0,2 mol hợp chất có chứa 4,6g Na và 7,1g Cl.
- Hợp chất B: 0,03 mol hợp chất có chứa 0,36g C và 0,96g O.
- Hợp chất C: 0,02 mol hợp chất có chứa 4,14g Pb và 0,32g O.
- Hợp chất D: 0,04 mol hợp chất có chứa 0,08 mol nguyên tử Fe và 0,12 mol nguyên tử O.
- Hợp chất E: 0,02 mol hợp chất có 0,04 mol nguyên tử Na, 0,02mol nguyên tử C và 0,06 mol nguyên tử O.
- Hợp chất A:
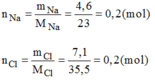
Cứ 0,2 mol hợp chất A có chứa 0,2 mol Na và 0,2 mol Cl.
Suy ra 1 mol hợp chất A có chứa 1 mol Na và 1 mol Cl.
Vậy công thức hóa học đơn giản của A là NaCl.
- Hợp chất B:
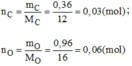
Vậy 0,03mol phân tử B có chứa 0,03 mol phân tử C và 0,06 mol nguyên tử O.
Suy ra 1 mol phân tử B có chứa 1 mol nguyên tử C và 2 mol nguyên tử O.
→Công thức hóa học của B là C O 2
- Hợp chất C:
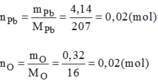
Vậy 0,02 mol phân tử C có chứa 0,02 mol nguyên tử Pb và 0,02 mol nguyên tử O.
Suy ra 1 mol phân tử C có chứa 1 mol nguyên tử Pb và 1 mol nguyên tử O.
→Công thức của phân tử C là: PbO.
- Hợp chất D:
Theo đề bài: 0,04 mol phân tử D có 0,08 mol Fe và 3 mol O.
Vậy 1 mol phân tử D có: 2 mol Fe và 0,12 mol O.
→ Công thức hóa học của D là F e 2 O 3
- Hợp chất E:
Cho biết: 0,02 mol phân tử E có 0,04 mol Na kết hợp 0,02 mol C và 0,06 mol nguyên tử O.
Vậy 1 mol phân tử E co 2 mol Na kết hợp 1 mol C và 3 mol O.
Công thức hóa học của E là N a 2 C O 3 .
a) Phân tử của hợp chất A gồm: 1 nguyên tử của nguyên tố X liên kết với 4 nguyên tử H và nặng gấp 8 lần phân tử hiđro. Xác định nguyên tố X và viết công thức hoá học của hợp chất A.
b) Hợp chất Fe(OH)x có phân tử khối gấp 7,5 lần nguyên tử khối của nguyên tử cacbon. Tìm x.
c) Một oxit có công thức hóa học CuxO có phân tử khối là 144. Tìm x.
d) Cho công thức hóa học của X với Cl là XCl, công thức hóa học của Y với H là HY. Tìm công thức của hợp chất giữa X và Y
a. Gọi CTHH của A là: XH4
Theo đề, ta có: \(d_{\dfrac{XH_4}{H_2}}=\dfrac{M_{XH_4}}{M_{H_2}}=\dfrac{M_{XH_4}}{2}=8\left(lần\right)\)
=> \(M_{XH_4}=16\left(g\right)\)
Ta có: \(M_{XH_4}=NTK_X+1.4=16\left(g\right)\)
=> NTKX = 12(đvC)
=> X là cacbon (C)
=> CTHH của A là: CH4
b. Theo đề, ta có: \(d_{\dfrac{Fe\left(OH\right)_x}{C}}=\dfrac{M_{Fe\left(OH\right)_x}}{M_C}=\dfrac{M_{Fe\left(OH\right)_x}}{12}=7,5\left(lần\right)\)
=> \(M_{Fe\left(OH\right)_x}=90\left(g\right)\)
Ta có: \(M_{Fe\left(OH\right)_x}=56+\left(16+1\right).x=90\left(g\right)\)
=> x = 2
c.
Ta có: \(PTK_{Cu_xO}=64.x+16=144\left(đvC\right)\)
=> x = 2
d. Ta có: \(\overset{\left(a\right)}{X}\overset{\left(I\right)}{Cl}\)
Ta có: a . 1 = I . 1
=> a = I
Vậy hóa trị của X là (I)
Ta lại có: \(\overset{\left(I\right)}{H}\overset{\left(b\right)}{Y}\)
Ta có: I . 1 = b . 1
=> b = I
Vậy hóa trị của Y là I
=> CT của hợp chất giữa X và Y là: XY
0,5 mol phân tử của hợp chất A có chứa:1 mol nguyên tử H ;0,5 mol nguyên tử S và 2 mol nguyên tử O.xác định công thức hóa học của hợp chất A
HxSyOz 0,15 mol là sao bạn mình không hiểu ở đâu ra 0,15
Bạn ơi
0.5mol mà.... Đó là số mol của A đó bạn
1. Các khái niệm nguyên tử, nguyên tố, phân tử khối, cách tích phân tử khối
2. Ý nghĩa của công thức hoá học, công thức hoá học của đơn chất và hợp chất
3. Quy tắc hoá trị. Vận dụng quy tắc hoá trị:
- Xác định hoá trị của mỗi nguyên tố trong các hợp chất H2S , CH4 , Fe2O3 , Ag2O , H2SO4
Lập công thức hoá học các hợp chất 2 nguyên tố : P(III) và H ; Fe(III) và O ; Al(III) và SO4(II) ; Ca(II) và PO4(III)
3.
H2S= II
CH4= IV
Fe2O3= III
Ag2O= I
H2SO4= i
Bài 2. Một hợp chất X gồm các nguyên tố Fe, O, S có tỉ lệ khối lượng mFe : mO : mS = 7: 12 : 6. Hãy xác định:
a) Công thức hóa học và gọi tên của hợp chất X biết khối lượng mol của X là 400 g/mol.
b) Số mol nguyên tử của mỗi nguyên tố có trong 60 gam hợp chất X.
a)
Gọi CTHH là $Fe_xS_yO_z$
Ta có :
\(\dfrac{56x}{7}=\dfrac{32y}{6}=\dfrac{16z}{12}=\dfrac{400}{7+6+12}\)
Suy ra x = 2 ; y = 3; z = 12
Vậy CTHH là $Fe_2(SO_4)_3$ :Sắt III sunfat
b)
$n_X = \dfrac{60}{400} =0,15(mol)$
Số nguyên tử Fe = 0,15.2.6.1023 = 1,8.1023 nguyên tử
Số nguyên tử S = 0,15.3.6.1023 = 2,7.1023 nguyên tử
Số nguyên tử O = 0,15.12.6.1023 = 10,8.1023 nguyên tử
Một hợp chất A có phân tử gồm 1 nguyên tử của nguyên tố X liên kết với 2 nguyên tử O và nặng hơn phân tử hidro là 32 lần.
a) Tính phân tử khối của hợp chất
b) Tính nguyên tử khối của X, cho biết tên và kí hiệu của nguyên tố.
c) Viết công thức hóa học của hợp chất A.
a) PTKA = 32.2 = 64 (đvC)
b) PTKA = NTKX + 2.16 = 64 (đvC)
=> NTKX = 32 (đvC)
=> X là Lưu huỳnh (S)
c) CTHH: SO2