Xác định số prôton trong hạt nhân nguyên tử, số electron ở lớp vỏ nguyên tử, số lớp electron và số lớp electron lớp ngoài cùng của nguyên tử photpho

Những câu hỏi liên quan
Một nguyên tử X có 2 lớp electron, biết lớp ngoài cùng có 4 electron. Trong nguyên tử X, số hạt mang điện hơn số hạt ko mang điện 6 hạt.a)xác định số hạt proton, electron, nơtron, NTK (đvC) và kí hiệu hóa học của Xb) Vẽ sơ đồ phân bố lớp vỏ electron vủa nguyên tử X, tính khối lượng nuyên tử X theo đơn vị gamc) Biết rằng 8 nguyên tử X nặng bằng 3 nguyên tử Y; 2 nguyên tử Y nặng bằng 4 nguyên tử Z. Xác định phân tử khối của các hợp chất XY2; XZ2 và YZ3
Đọc tiếp
Một nguyên tử X có 2 lớp electron, biết lớp ngoài cùng có 4 electron. Trong nguyên tử X, số hạt mang điện hơn số hạt ko mang điện 6 hạt.
a)xác định số hạt proton, electron, nơtron, NTK (đvC) và kí hiệu hóa học của X
b) Vẽ sơ đồ phân bố lớp vỏ electron vủa nguyên tử X, tính khối lượng nuyên tử X theo đơn vị gam
c) Biết rằng 8 nguyên tử X nặng bằng 3 nguyên tử Y; 2 nguyên tử Y nặng bằng 4 nguyên tử Z. Xác định phân tử khối của các hợp chất XY2; XZ2 và YZ3
a)
X có 6 electron
=> pX = eX = 6
nX = 2pX - 6 = 6
X là Cacbon(C), có NTK = 12 (đvC)
b)

Khối lượng của 1 nguyên tử C = 1,9926.10-23 (g)
c)
\(NTK_Y=\dfrac{8.12}{3}=32\left(đvC\right)\)
PTKXY2 = 12 + 32.2 = 76 (đvC)
\(NTK_Z=\dfrac{2.32}{4}=16\left(đvC\right)\)
PTKXZ2 = 12 + 16.2 = 44 (đvC)
PTKYZ3 = 32 + 16.3 = 80 (đvC)
Đúng 8
Bình luận (2)
ta có lớp ngoài có 4 lớp => tổng số e là : 4+2=6 hạt
=> p=e=6
2p - n = 6
<=> 12 - n = 6
<=> n=6
=> X là Cacbon : C
c) ta lại có : 8X = 3Y => 48 = 3Y => Y = 16 => Y là S
có : 2Y = 4Z => 32 = 4Z = Z= 8 => Z là O
=> CTHH : XY2 : CS2 , XZ2 : CO2 , YZ3 : SO3
Đúng 3
Bình luận (0)
ta có lớp ngoài có 4 lớp => tổng số e là : 4+2=6 hạt
=> p=e=6
2p - n = 6
<=> 12 - n = 6
<=> n=6
=> X là Cacbon : C
c) ta lại có : 8X = 3Y => 48 = 3Y => Y = 16 => Y là S
có : 2Y = 4Z => 32 = 4Z = Z= 8 => Z là O đơn giản cũng hỏi
Đúng 0
Bình luận (0)
Nguyên tử agon có kí hiệu là
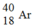
- Hãy xác định số proton, số proton trong hạt nhân và số electron ở vỏ electron của nguyên tử.
- Hãy xác định sự phân bố electron trên các lớp.
Z= 18 suy ra trong hạt nhân Ar có 18p và 22n (40 – 18), lớp vỏ electron của nguyên tử có 18e được phân bố như sau: 1s22s22p63s23p6.
Đúng 0
Bình luận (0)
nguyên tử z có tổng số proton là 12 . Xác định số electron , số lớp electron , số đơn vị điện tích hạt nhân và số hạt electron lớp ngoài cùng . vẽ lại mô hình nguyên tử x
Số electron : 12
Số đơn vị điện tích hạt nhân : + 12
Số hạt electron lớp ngoài cùng : 2
Đúng 0
Bình luận (0)
Số electron : 12
Số đơn vị điện tích hạt nhân : + 12
Số hạt electron lớp ngoài cùng : 2
Đúng 0
Bình luận (0)
số electron:12
số lớp electron:3
số hạt electron lớp ngoài cùng:2
số đơn vị điện tích hạt nhân :?
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Cho biết sơ đồ một số nguyên tử sau:

Hãy chỉ ra số proton trong hạt nhân, số electron trong nguyên tử, số lớp electron và số electron lớp ngoài cùng của mỗi nguyên tử.
(Lập bảng như trong SGK)
| Nguyên tử | Số p trong hạt nhân | Số e trong nguyên tử | Số lớp electron | Số e lớp ngoài cùng |
|---|---|---|---|---|
Nitơ Neon Silic Kali |
7 10 14 19 |
7 10 14 19 |
2 2 3 4 |
5 8 4 1 |
Đúng 0
Bình luận (0)
Có thể vẽ sơ đồ đơn giản gồm vòng tròn con là hạt nhân, mỗi vòng cung nhỏ là một lớp với số electron của lớp ghi ở chân. Thí dụ sơ đồ đơn giản của nguyên tử sillic trong bài tập 4.3 như sau:Biết rằng, trong nguyên tử các electron có ở lớp 1 (tính từ hạt nhân) tối đa là 2e, ở lớp 2 tối đa là 8e, ở lớp 3 tạm thời cũng là 8e, nếu còn electron sẽ ở lớp 4.Mấy nguyên tử có số electron ở lớp ngoài cùng bằng 5, mấy nguyên tử có số electron ở lớp ngoài cùng bằng 7 ?
Đọc tiếp
Có thể vẽ sơ đồ đơn giản gồm vòng tròn con là hạt nhân, mỗi vòng cung nhỏ là một lớp với số electron của lớp ghi ở chân. Thí dụ sơ đồ đơn giản của nguyên tử sillic trong bài tập 4.3 như sau:
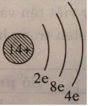
Biết rằng, trong nguyên tử các electron có ở lớp 1 (tính từ hạt nhân) tối đa là 2e, ở lớp 2 tối đa là 8e, ở lớp 3 tạm thời cũng là 8e, nếu còn electron sẽ ở lớp 4.
Mấy nguyên tử có số electron ở lớp ngoài cùng bằng 5, mấy nguyên tử có số electron ở lớp ngoài cùng bằng 7 ?
- Hai nguyên tử có số eletron lớp ngoài cùng là 5.
- Hai nguyên tử có số electron ngoài cùng 7.
Đúng 0
Bình luận (0)
(1)Các electron chuyển động rất nhanh trong khu vực xung quanh hạt nhân nguyên tử theo 1 quỹ đạo xác định tạo nên lớp vỏ nguyên tử. (2) Số electron tối đa trên lớp L là 8e (3) Nguyên tố s là nguyên tố mà nguyên tử có electron cuối cùng điền vào lớp s (4)Nếu hình dung nguyên tử như một quả cầu, thì nó có đường kính khoảng 1 angstrom Số phát biểu đúng là: A 2 B 1 C 3 D 4
X không phải là khí hiếm, nguyên tử nguyên tố X có phân lớp electron ngoài cùng là 3p. Nguyên tử nguyên tố Y có phân lớp electron ngoài cùng là 3s. Tổng số electron ở hai phân lớp ngoài cùng của X và Y là 7. Xác định số hiệu nguyên tử của X và Y A. X (Z 18); Y (Z 10). B. X (Z 17); Y (Z 11). C. X (Z 17); Y (Z 12). D. X (Z 15); Y (Z 13).
Đọc tiếp
X không phải là khí hiếm, nguyên tử nguyên tố X có phân lớp electron ngoài cùng là 3p. Nguyên tử nguyên tố Y có phân lớp electron ngoài cùng là 3s. Tổng số electron ở hai phân lớp ngoài cùng của X và Y là 7. Xác định số hiệu nguyên tử của X và Y
A. X (Z = 18); Y (Z = 10).
B. X (Z = 17); Y (Z = 11).
C. X (Z = 17); Y (Z = 12).
D. X (Z = 15); Y (Z = 13).
Đáp án C
TH1: Y có phân lớp ngoài cùng là 3s1
→ Y có cấu hình electron là 1s22s22p63s1
→ Y có 11e → Y có Z = 11.
X có số electron ở phân lớp ngoài cùng = 7 - 1 = 6
→ X có phân lớp ngoài cùng là 3p6 → X là khí hiếm → loại.
• TH2: Y có phân lớp ngoài cùng là 3s2 → tương tự ta có Y có Z = 12.
Khi đó, X có lớp ngoài cùng là 3p5
→ X có cấu hình electron là 1s22s22p63s23p5
→ X có 17 e → Z = 17.
Đúng 0
Bình luận (0)
X không phải là khí hiếm, nguyên tử nguyên tố X có phân lớp electron ngoài cùng là 3p. Nguyên tử nguyên tố Y có phân lớp electron ngoài cùng là 3s. Tổng số electron ở hai phân lớp ngoài cùng của X và Y là 7. Xác định số hiệu nguyên tử của X và Y A. X (Z 18); Y (Z 10) B. X (Z 17); Y (Z 11) C. X (Z 17); Y (Z 12) D. X (Z 15); Y (Z 13)
Đọc tiếp
X không phải là khí hiếm, nguyên tử nguyên tố X có phân lớp electron ngoài cùng là 3p. Nguyên tử nguyên tố Y có phân lớp electron ngoài cùng là 3s. Tổng số electron ở hai phân lớp ngoài cùng của X và Y là 7. Xác định số hiệu nguyên tử của X và Y
A. X (Z = 18); Y (Z = 10)
B. X (Z = 17); Y (Z = 11)
C. X (Z = 17); Y (Z = 12)
D. X (Z = 15); Y (Z = 13)
C
TH1: Y có phân lớp ngoài cùng là 3 s 1 → Y có cấu hình electron là 1 s 2 2 s 2 2 p 6 3 s 1
→ Y có 11e → Y có Z = 11.
X có số electron ở phân lớp ngoài cùng = 7 - 1 = 6 → X có phân lớp ngoài cùng là 3 p 6 → X là khí hiếm → loại.
• TH2: Y có phân lớp ngoài cùng là 3 s 2 → Y có cấu hình electron là 1 s 2 2 s 2 2 p 6 3 s 2
→ Y có 12 electron → Y có Z = 12.
Khi đó, X có lớp ngoài cùng là 3 p 5 → X có cấu hình electron là 1 s 2 2 s 2 2 p 6 3 s 2 3 p 5
→ X có 17 e → Z = 17.
Đúng 0
Bình luận (0)
Nguyên tử agon có kí hiệu là 4018Ar
a) Hãy xác định số proton, số nơtron trong hạt nhân và số electron ở vỏ electron của nguyên tử.
b) Hãy xác định sự phân bố electron trên các lớp.
a) Từ kí hiệu ta thấy nguyên tử Ar có số đơn vị điện tích hạt nhân là 18; vậy Ar có 18 prôtn, 18 electron và có 40-18= 22 nơtron
b) Lớp vỏ electron của nguyên tử có 18e được phân bố như sau : 1s2 2s2 2p6 3s2 3p6.
Đúng 0
Bình luận (0)
















