Để đốt cháy hoàn toàn a gam cacbon thì cần vừa đủ 1 , 5 . 10 24 phân tử khí oxi. Giá trị của a là
A. 25
B. 30
C. 20
D. 21
Để đốt cháy hoàn toàn a gam cacbon thì cần vừa đủ 1 , 5 . 10 24 phân tử khí oxi. Hãy tính giá trị của a.
Đốt cháy hoàn toàn a gam triglixerit (một chất béo) X cần vừa đủ 3,26 mol khí oxi, thu được 2,28 mol khí cacbonic và 39,6 gam nước. Mặt khác thủy phân hoàn toàn gam X trên trong dung dịch NaOH dư thì thu được dung dịch chứa b gam muối. Giá trị của b là
A. 40,40
B. 31,92
C. 36,72.
D. 35,60
Đốt cháy hoàn toàn a gam triglixerit (một chất béo) X cần vừa đủ 3,26 mol khí oxi, thu được 2,28 mol khí cacbonic và 39,6 gam nước. Mặt khác thủy phân hoàn toàn gam X trên trong dung dịch NaOH dư thì thu được dung dịch chứa b gam muối. Giá trị của b là:
A. 40,40.
B. 31,92.
C. 36,72.
D. 35,60.
Chọn đáp án C
Ta có nCO2 = nC = 2,28 mol
nH = 2nH2O = 4,4 mol.
⇒ nC:nH = 55:110 ⇒ X là tristearin
⇒ ntristearin = 2,28 ÷ 57 = 0,04 mol
⇒ mC17H35COONa = 0,04×3×306 = 36,72 gam
Amino axit X no, mạch hở, phân tử chứa n nguyên tử cacbon, một nhóm amino và một nhóm cacboxyl. Đốt cháy hoàn toàn 1 mol X cần vừa đủ a mol khí O2, thu được CO2, H2O và N2. Giá trị của a là
A. 2 n + 3 2
B. 6 n - 3 4
C. 3 n - 3 2
D. 4 n + 3 4
Đáp án B
công thức phân tử của X là CnH2n + 1NO2. Phản ứng đốt cháy
C n H 2 n + 1 + 6 n - 3 4 O 2 → t 0 C nCO 2 + 2 n + 1 2 H 2 O + 1 2 N 2
=> a = 6 n - 3 4
Đốt cháy hoàn toàn 4,8 gam lưu huỳnh thành lưu huỳnh đioxit thì cần vừa đủ V lít không khí (đktc), biết trong không khí thì oxi chiếm 20% thể tích. Giá trị của V là
A. 17,8
B. 18,8
C. 15,8
D. 16,8
Hợp chất hữu cơ X được tạo bởi glixerol và axit axetic. Trong phân tử X, số nguyên tử hiđro bằng tổng số nguyên tử cacbon và oxi. Đốt cháy hoàn toàn 38,368 gam X cần vừa đủ V lít khí O2 (đktc) thu được sản phẩm chỉ có CO2 và H2O. Giá trị của V là
A. 36,624
B. 37,453
C. 35,840.
D. 39,200
Hợp chất hữu cơ X được tạo bởi glixerol và axit axetic. Trong phân tử X, số nguyên tử hiđro bằng tổng số nguyên tử cacbon và oxi. Đốt cháy hoàn toàn 38,368 gam X cần vừa đủ V lít khí O2 (đktc) thu được sản phẩm chỉ có CO2 và H2O. Giá trị của V là
A. 36,624.
B. 37,453.
C. 35,840.
D. 39,200.
Đốt cháy hoàn toàn a gam hỗn hợp gồm: eten, propen,but – 2 – en cần dùng vừa đủ b lít khí oxi ở đktc thu được 5,376 lít CO 2 ở đktc và 4,32 gam nước. Giá trị của b là:
A. 9,24
B. 9,42.
C. 8,064.
D. 2,49
- Bảo toàn nguyên tố O ta có:
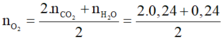
= 0,36(mol)
- Vậy b = 0,36.22,4 = 8,064 lít.
- Chọn đáp án C.
Khối lượng oxi cần dùng để đốt cháy vừa đủ hỗn hợp gồm 6 gam C và 8 g S là ( C = 12. S = 32) A. 20 gam B. 24 gam C. 26 gam D. 30 gam
\(pthh:C+O_2\overset{t^o}{--->}CO_2\left(1\right)\)
\(S+O_2\overset{t^o}{--->}SO_2\left(2\right)\)
Ta có: \(\left\{{}\begin{matrix}n_C=\dfrac{6}{12}=0,5\left(mol\right)\\n_S=\dfrac{8}{32}=0,25\left(mol\right)\end{matrix}\right.\)
Theo pt(1): \(n_{O_2}=n_C=0,5\left(mol\right)\)
Theo pt(2): \(n_{O_2}=n_S=0,25\left(mol\right)\)
\(\Rightarrow m_{O_{2_{cần.dùng}}}=0,5.32+0,25.32=24\left(g\right)\)
Chọn B