Cho 4,48 lít khí CO (đktc) tác dụng với FeO ở nhiệt độ cao. Sau phản ứng thu được chất rắn A có khối lượng nhỏ hơn 1,6g so với lượng FeO ban đầu. Tính khối lượng Fe thu được và % V các chất (cùng trạng thái) sau phản ứng?

Những câu hỏi liên quan
Cho 4,48 lít khí CO (đktc) tác dụng với FeO ở nhiệt độ cao. Sau phản ứng thu được chất khí A có khối lượng bé hơn 1,6g so với lượng FeO ban đầu. Tính khối lượng Fe thu được và % thể tích hỗn hợp khios sau phản ứng?
nCO phản ứng = nCO2 = nFe = nO = 0,1
→ mFe = 5,6g
nCO2 dư = 0,2 - 0,1 = 0,1
→ %VCO2 = 50%
Đúng 0
Bình luận (2)
FeO + CO -> Fe + CO2
nCO=0,2(mol)
Đặt nFeO tham gia PƯ=a
Ta có:
72a-56a=1,6
=>a=0,1
Theo PTHH ta có:
nFe=nCO2=nFeO tham gia PƯ=0,1(mol)
mFe=56.0,1=5,6(g)
%VCO2=\(\dfrac{0,1}{0,2}.100\%=50\%\)
%VCO=100-50=50%
Đúng 0
Bình luận (2)
Cho 4,48l CO (đktc) tác dụng với FeO sau phản ứng thu được chất rắn X có khối lượng nhỏ hơn 1,6g so với khối lượng FeO ban đầu. Tính khối lượng Fe thu được và %V hỗn hợp khí sau phản ứng
Đặt :
nFeO = x mol
FeO + CO -to-> Fe + CO2
x_____x_______x_____x
m giảm = mFeO - mFe = 1.6
<=> 72x - 56x = 1.6
=> x = 0.1
mFe = 0.1*56 = 5.6 g
nCO dư = 0.2 - 0.1 = 0.1 mol
nCO2 = 0.1 mol
Vì : %V = %n
%CO = %CO2 = 0.1/0.2 *100% = 50%
Đúng 0
Bình luận (0)
Đặt \(n_{FeO}=x\left(mol\right)\)
\(FeO+CO\underrightarrow{t^o}Fe+CO_2\)
x → x
\(m_{giảm}=m_{FeO}-m_{Fe}=1,6\)
\(\Leftrightarrow72x-56x=1,6\)
\(\rightarrow x=0,1\)\(\rightarrow m_{Fe}=0,1.56=5,6\left(g\right)\)
\(n_{CO}dư=0,2-0,1=0,1\left(mol\right)\)
→\(n_{CO_2}=0,1\left(mol\right)\)
mà \(\%V=\%n\)
%CO=%CO2\(\frac{0,1}{0,2}\).100%=50%
Đúng 0
Bình luận (0)
FeO + CO -> Fe + CO2
x............x........x.......x (mol)
Gọi số mol Fe phan ứng là x mol
nCO = 0,2 (mol)
Theo bài ra : \(\Delta m=72x-56x=16x=1,6\left(g\right)\)
=> x = 0,1 (mol)
mFe = 5,6 (g)
CO sau phản ứng dư 0,1 (mol)
=> %VCO = %VCO2 = 50%
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Cho 4,72 gam hỗn hợp bột gồm các chất Fe, FeO và Fe2O3 tác dụng với CO ở nhiệt độ cao. Phản ứng xong thu được 3,92 gam Fe. Nếu ngâm cùng lượng hỗn hợp các chất trên trong dung dịch CuSO4 dư, phản ứng xong khối lượng chất rắn thu được là 4,96 gam. Khối lượng (gam) Fe, Fe2O3 và FeO trong hỗn hợp ban đầu lần lượt là A. 1,68; 1,44; 1,6 B. 1,6; 1,54; 1,64 C. 1,6; 1,44; 1,64 D. 1,68; 1,6; 1,44
Đọc tiếp
Cho 4,72 gam hỗn hợp bột gồm các chất Fe, FeO và Fe2O3 tác dụng với CO ở nhiệt độ cao. Phản ứng xong thu được 3,92 gam Fe. Nếu ngâm cùng lượng hỗn hợp các chất trên trong dung dịch CuSO4 dư, phản ứng xong khối lượng chất rắn thu được là 4,96 gam. Khối lượng (gam) Fe, Fe2O3 và FeO trong hỗn hợp ban đầu lần lượt là
A. 1,68; 1,44; 1,6
B. 1,6; 1,54; 1,64
C. 1,6; 1,44; 1,64
D. 1,68; 1,6; 1,44
Đáp án D
Các phản ứng xảy ra:
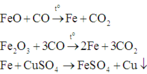
Hỗn hợp rắn thu được khi cho hỗn hợp phản ứng với dung dịch CuSO4 gồm Cu, FeO và Fe2O3.
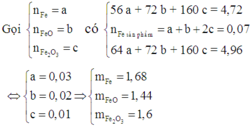
Đúng 0
Bình luận (0)
Hoà tan hoàn toàn 57,6 gam hỗn hợp X gồm ,
Fe
2
O
3
, FeO và Fe trong dung dịch HCl thì cần dùng 360 gam dung dịch HCl 18,25% để tác dụng vừa đủ. Sau phản ứng thu được V lít khí
H
2
và dung dịch Y.Cho toàn bộ
H
2
sinh ra tác dụng hết với CuO dư ở nhiệt độ cao, sau phản ứn...
Đọc tiếp
Hoà tan hoàn toàn 57,6 gam hỗn hợp X gồm , Fe 2 O 3 , FeO và Fe trong dung dịch HCl thì cần dùng 360 gam dung dịch HCl 18,25% để tác dụng vừa đủ. Sau phản ứng thu được V lít khí H 2 và dung dịch Y.
Cho toàn bộ H 2 sinh ra tác dụng hết với CuO dư ở nhiệt độ cao, sau phản ứng thu được hỗn hợp rắn gồm Cu và CuO có khối lượng nhỏ hơn khối lượng CuO ban đầu là 3,2 gam. Nếu cô cạn dung dịch Y thì thu được bao nhiêu gam muối khan ?
n HCl = 360 x 18,25/(100x36,5) = 1,8 mol
H 2 + CuO → t ° Cu + H 2 O
n CuO = x
Theo đề bài
m CuO (dư) + m Cu = m CuO (dư) + m Cu p / u - 3,2
m Cu = m Cu p / u - 3,2 => 64x = 80x - 3,2
=> x= 0,2 mol → m H 2 = 0,4g
Fe + 2HCl → FeCl 2 + H 2
Số mol HCl tác dụng với Fe 3 O 4 , Fe 2 O 3 , FeO là 1,8 - 0,4 = 1,4 mol
Phương trình hóa học của phản ứng:
Fe 3 O 4 + 8HCl → 2 FeCl 3 + FeCl 2 + 4 H 2 O (1)
Fe 2 O 3 + 6HCl → 2 FeCl 3 + 3 H 2 O (2)
FeO + 2HCl → FeCl 2 + H 2 O (3)
Qua các phản ứng (1), (2), (3) ta nhận thấy n H 2 O = 1/2 n HCl = 1,4:2 = 0,7 mol
Áp dụng định luật bảo toàn khối lượng, ta có:
m hỗn hợp + m HCl = m muối + m H 2 O + m H 2
57,6 + 1,8 x 36,5 = m muối + 0,7 x 18 +0,4
m muối = 57,6 + 65,7 - 12,6 - 0,4 = 110,3 (gam)
Đúng 1
Bình luận (0)
Đốt cháy hh CuO và FeO với C có dư thì được chất rắn và khí B. Cho B tác dụng với nước vôi trong có dư thu được 8g kết tủa. Chất rắn A cho tác dụng vớidd HCl với nồng độ 10% thì cần dùng một lượng axit là 73g sẽ vừa đủ. Tính khối lượng CuO và FeO trong hh ban đầu và thể tích khí B ( các khí đo ở đktc)
Bài của bạn sai cái gì ấy, mk làm không ra....
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 57,6 gam hỗn hợp gồm fe3o4, fe203, feo, fe vào dung dịch hcl cần 360 gam dung dich hcl 18,25% để tác dụng vừa đủ . Sau phản ứng thu đươc V(l) h2 và dung dich b.a)Cho toàn bộ h2 sinh ra tác dụng với cuo dư ở nhiệt độ cao thu được hỗn hợp chất rắn có khối lương nhỏ hơn khối lượng cuo ban đầu là 3,2 gam a, nếu cô cạn dung dịch b thì thu bao nhiêu gam muối khan b,b)nếu hỗn hợp a ban đầu có tỉ lệ mol n(fe2o3) : n ( feo) 1: 1. Tính C% các chất trong dung dich bc)hỗn hợp x cũng chứa...
Đọc tiếp
Hòa tan hoàn toàn 57,6 gam hỗn hợp gồm fe3o4, fe203, feo, fe vào dung dịch hcl cần 360 gam dung dich hcl 18,25% để tác dụng vừa đủ . Sau phản ứng thu đươc V(l) h2 và dung dich b.
a)Cho toàn bộ h2 sinh ra tác dụng với cuo dư ở nhiệt độ cao thu được hỗn hợp chất rắn có khối lương nhỏ hơn khối lượng cuo ban đầu là 3,2 gam a, nếu cô cạn dung dịch b thì thu bao nhiêu gam muối khan b,
b)nếu hỗn hợp a ban đầu có tỉ lệ mol n(fe2o3) : n ( feo) = 1: 1. Tính C% các chất trong dung dich b
c)hỗn hợp x cũng chứa Fe3O4 ; Fe2O3 ; FeO ; Fe nếu dùng 100g (x ) cho tác dugnj với 2 lít dd hcl 2M . chứng minh rằng hỗn hợp x tan hết
Cho 15,6g hỗn hợp gồm bột Fe và bột Cu tác dụng vừa đủ với 100g dung dịch HCl, thu được 4,48 lít khí H2 (đktc).a. Viết phương trình hóa học của phản ứng xảy ra ?b. Tính khối lượng các chất rắn ban đầu ?
Đọc tiếp
Cho 15,6g hỗn hợp gồm bột Fe và bột Cu tác dụng vừa đủ với 100g
dung dịch HCl, thu được 4,48 lít khí H2 (đktc).
a. Viết phương trình hóa học của phản ứng xảy ra ?
b. Tính khối lượng các chất rắn ban đầu ?
a)
$Fe + 2HCl \to FeCl_2 + H_2$
b)
Theo PTHH : $n_{Fe} = n_{H_2} = \dfrac{4,48}{22,4} = 0,2(mol)$
$\Rightarrow m_{Fe} = 0,2.56 = 11,2(gam)$
$\Rightarrow m_{Cu} = 15,6 - 11,2 = 4,4(gam)$
Đúng 1
Bình luận (0)
Để 1 lượng bột sắt ngoài không khí. Sau một thời gian thu được chất rắn X gồm FeO Fe3O4 Fe2O3 và Fe có khối lượng nặng hơn lượng bột sắt ban đầu là 3,2g. Nếu cho toàn bộ X tác dụng với dung dịch H2SO4 đậm đặc, nóng, dư thu được 2,24 l khí SO2 (đktc) duy nhất thoát ra. Viết ptpư có thể xảy ra. Tính khối lượng bột sắt ban đầu
a, \(2Fe+O_2\underrightarrow{t^o}2FeO\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
\(4Fe+3O_2\underrightarrow{t^o}2Fe_2O_3\)
\(2Fe+6H_2SO_{4\left(đ\right)}\underrightarrow{t^o}Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
\(2FeO+4H_2SO_{4\left(đ\right)}\underrightarrow{t^o}Fe_2\left(SO_4\right)_3+SO_2+4H_2O\)
\(2Fe_3O_4+10H_2SO_{4\left(đ\right)}\underrightarrow{t^o}3Fe_2\left(SO_4\right)_3+SO_2+10H_2O\)
\(Fe_2O_3+3H_2SO_{4\left(đ\right)}\underrightarrow{t^o}Fe_2\left(SO_4\right)_3+3H_2O\)
b, Ta có: mO2 = 3,2 (g) \(\Rightarrow n_{O_2}=\dfrac{3,2}{32}=0,1\left(mol\right)\)
\(n_{SO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
BT e, có: 3nFe = 4nO2 + 2nSO2
⇒ nFe = 0,2 (mol)
⇒ mFe = 0,2.56 = 11,2 (g)
Đúng 3
Bình luận (2)
Cho 9,2g hỗn hợp Fe và FeO phản ứng với 200g dung dịch H2SO419,6 dư thu được 2,24 lít khí ở đktc.
a. Tính % khối lượng mỗi chất trong hỗn hợp đầu.
b. Tính C % dung dịch sau phản ứng
























