Cho m gam Mg tác dụng với HNO3 loãng , dư thu được 4,48 lít khí không màu hóa nâu trong không khí (đktc) . Giá trị của m là

Những câu hỏi liên quan
Đốt cháy m gam CuS trong khí oxi dư thu được chất rắn X có khối lượng bằng (m – 4,8) gam. Nung X với khí
NH
3
dư tới khi khối lượng không đổi được chất rắn Y. Hòa tan hoàn toàn Y trong dung dịch
HNO
3
loãng dư, thu được V lít khí Z (đktc) không màu, hóa nâu trong không khí. Giá trị của m và V là A. 19,2 gam; 1,12 lít B. 28,8 gam; 4,48 lít C. 24,0 gam; 4,48 lít D. 28,8 gam; 1,12 lít
Đọc tiếp
Đốt cháy m gam CuS trong khí oxi dư thu được chất rắn X có khối lượng bằng (m – 4,8) gam. Nung X với khí NH 3 dư tới khi khối lượng không đổi được chất rắn Y. Hòa tan hoàn toàn Y trong dung dịch HNO 3 loãng dư, thu được V lít khí Z (đktc) không màu, hóa nâu trong không khí. Giá trị của m và V là
A. 19,2 gam; 1,12 lít
B. 28,8 gam; 4,48 lít
C. 24,0 gam; 4,48 lít
D. 28,8 gam; 1,12 lít
Cho 6,84 gam hỗn hợp Mg và Al có tỉ lệ mol tương ứng là 5: 4 tác dụng với lượng dư dung dịch
H
N
O
3
loãng, thu được dung dịch X và 0,896 lít (đktc) hỗn hợp hai khí không màu, không hóa nâu trong không khí, có tỉ khối so với
H
2
bằng 18. Số mol
H
N
O...
Đọc tiếp
Cho 6,84 gam hỗn hợp Mg và Al có tỉ lệ mol tương ứng là 5: 4 tác dụng với lượng dư dung dịch H N O 3 loãng, thu được dung dịch X và 0,896 lít (đktc) hỗn hợp hai khí không màu, không hóa nâu trong không khí, có tỉ khối so với H 2 bằng 18. Số mol H N O 3 bị khử trong quá trình trên là
A. 0,1375 mol
B. 0,81 mol
C. 0,66 mol
D. 0,18 mol
Đáp án A
n M g = 0 , 15 m o l ; n A l = 0 , 12 m o l Hai khí thu được là N 2 , N 2 O
Đặt n N 2 = x ; n N 2 O = y
⇒ n k h i = x + y = 0 , 04 m o l ; m k h í = 28 x + 44 y = 0 , 04 . 18 . 2
Giải hệ cho x-y=0,02 mol
Bảo toàn electron:
2 n M g + 3 n A l = 10 n N 2 + 8 n N H 4 +
⇒ n N H 4 + = 0 , 0375 m o l
n H N O 3 b i k h u = 2 n N 2 + 2 n N 2 O + n N H 4 + = 0 , 1175 m o l bị khửa
Đúng 0
Bình luận (0)
Cho 5,04 gam hỗn hợp Mg và Al có tỉ lệ mol tương ứng là 3:2 tác dụng với dung dịch HNO3 loãng, dư thu được dung dịch X và 0,896 lít (đktc) hỗn hợp hai khí không màu, không hóa nâu trong không khí có tỉ khối hơi so với H2 bằng 18. Số mol HNO3 bị khử trong quá trình trên là A. 0,095 mol B. 0,11mol C. 0,1 mol D. 0,08 mol
Đọc tiếp
Cho 5,04 gam hỗn hợp Mg và Al có tỉ lệ mol tương ứng là 3:2 tác dụng với dung dịch HNO3 loãng, dư thu được dung dịch X và 0,896 lít (đktc) hỗn hợp hai khí không màu, không hóa nâu trong không khí có tỉ khối hơi so với H2 bằng 18. Số mol HNO3 bị khử trong quá trình trên là
A. 0,095 mol
B. 0,11mol
C. 0,1 mol
D. 0,08 mol
Cho 5,04 gam hỗn hợp Mg và Al có tỉ lệ mol tương ứng là 3:2 tác dụng với dung dịch HNO3 loãng, dư thu được dung dịch X và 0,896 lít (đktc) hỗn hợp hai khí không màu, không hóa nâu trong không khí có tỉ khối hơi so với H2 bằng 18. Số mol HNO3 bị khử trong quá trình trên là: A. 0,095 mol B. 0,11 mol C. 0,1 mol D. 0,08 mol
Đọc tiếp
Cho 5,04 gam hỗn hợp Mg và Al có tỉ lệ mol tương ứng là 3:2 tác dụng với dung dịch HNO3 loãng, dư thu được dung dịch X và 0,896 lít (đktc) hỗn hợp hai khí không màu, không hóa nâu trong không khí có tỉ khối hơi so với H2 bằng 18. Số mol HNO3 bị khử trong quá trình trên là:
A. 0,095 mol
B. 0,11 mol
C. 0,1 mol
D. 0,08 mol
Ta đặt nMg= 3x, nAl= 2x mol → mhh= 24.3x+ 27.2x=126x= 5,04 →x=0,04 mol→ nMg= 0,12 mol; nAl= 0,08 mol
Sản phẩm khử gồm 2 khí không màu, không hóa nâu ngoài không khí. Đó là N2 (a mol) và N2O (b mol)
Ta có a+b= 0,896/22,4= 0,04
Và mhh= 28a+ 44b= 18.2.0,04
Giải hệ trên có a= 0,02, b=0,02
QT cho e:
Mg→ Mg2++ 2e
0,12 0,24
Al→ Al3++ 3e
0,08 0,24
Tổng số mol e cho ne cho= 0,24+ 0,24= 0,48 mol
Quá trình nhận e:
2NO3-+ 10e+ 12H+ → N2 + 6H2O (2)
0,2 ← 0,02 mol
2NO3-+ 8e+ 10H+ → N2O + 5H2O (3)
0,16 ← 0,02mol
Tổng số mol e nhận ở (2) và (3) là ne nhận= 0,2+ 0,16= 0,36mol <0,48 mol
Do đó còn xảy ra quá trình nhận e: ne nhận ở (4)= 0,48- 0,36= 0,12 mol
NO3-+ 8e+ 10H+ → NH4++ 3H2O (4)
0,12 → 0, 015 mol
Theo các bán phản ứng (2), (3), (4) thì
nNO3-bị khử= 2.nN2+ 2. nN2O+nNH4+= 2.0,02+2.0,02+0,015= 0,095 mol
=nHNO3 bị khử
Đáp án A
Đúng 0
Bình luận (0)
Cho hỗn hợp X gồm Mg và Al. Nếu cho hỗn hợp X tác dụng vs dung dịch HCl dư thu đc 3,36lit H2. Nếu cho hỗn hợp X hào tan hết trong HNO3 loãng dư thu đc V lít một khí không màu, hóa nâu trong không khí (các thể tích khí đều đo ở đktc). Giá trị của V là?
Cho m gam Mg tác dụng hoàn toàn với dung dịch
H
2
SO
4
loãng, dư thu được 4,48 lít khí
H
2
(đktc). Giá trị của m là A. 7,2. B. 4,8. C. 16,8. D. 3,6.
Đọc tiếp
Cho m gam Mg tác dụng hoàn toàn với dung dịch H 2 SO 4 loãng, dư thu được 4,48 lít khí H 2 (đktc). Giá trị của m là
A. 7,2.
B. 4,8.
C. 16,8.
D. 3,6.
Cho 6,84 gam hỗn hợp Mg và Al có tỉ lệ mol tương ứng là 5: 4 tác dụng với lượng dư dung dịch
H
N
O
3
loãng, thu được dung dịch X và 0,896 lít (đktc) hỗn hợp hai khí không màu, không hóa nâu trong không khí, có tỉ khối so với
H
2
bằng 18. Số mol bị khử trong quá trình trên là A. 0,1375 mol B. 0,81 mol C. 0,66 mol D. 0,18 mol.
Đọc tiếp
Cho 6,84 gam hỗn hợp Mg và Al có tỉ lệ mol tương ứng là 5: 4 tác dụng với lượng dư dung dịch H N O 3 loãng, thu được dung dịch X và 0,896 lít (đktc) hỗn hợp hai khí không màu, không hóa nâu trong không khí, có tỉ khối so với H 2 bằng 18. Số mol bị khử trong quá trình trên là
A. 0,1375 mol
B. 0,81 mol
C. 0,66 mol
D. 0,18 mol.
Hòa tan hoàn toàn 7,15 gam kim loại M hóa trị 2 vào lượng dư dung dịch HNO3 loãng, thu được 0,448 lít(đktc) hỗn hợp 2 khí không màu, không hóa nâu trong không khí (số mol hai khí bằng nhau) và dung dịch chứa 21,19 gam muối. Kim loại M là:
A. Fe
B. Ca
C. Mg
D. Zn
2 khí không màu, không hóa nâu trong không khí và là sản phẩm khử của N+5 chỉ có thể là N2 và N2O
-TH1: 21,19 gam muối không có muối NH4NO3
Theo bảo toàn nguyên tố M ta có: nM= nM(NO3)2
→ m M m M ( N O 3 ) 2 = M M M M ( N O 3 ) 2 → 7 , 15 21 , 19 = M M + 62 , 2
→M= 63,148 Loại
Do đó trường hợp này loại
-TH2: 21,19 gam muối có muối NH4NO3
QT cho e:
M → M2++ ne (1)
7,15/M 7,15.2/M
QT nhận e : nkhí= 0,02 mol. Mà số mol hai khí bằng nhau nên n N 2 O = n N 2 =0,01mol
2NO3-+ 8e+ 10H+ → N2O + 5H2O (2)
0,08 0,1 ← 0,01 mol
2NO3-+ 10e+12H+→ N2+ 6H2O (3)
0,1 0,12← 0,01 mol
NO3-+ 8e + 10H+ → NH4+ + 3H2O (4)
8x xmol
Đặt số mol muối NH4+ là x mol
Theo ĐL BT e: ne cho= ne nhận nên 7,15.2/M= 0,08 + 0,1+8x (*1)
Mặt khác : mmuối= mM(NO3)2+ mNH4NO3= 7,15/M. (M+124)+80x= 21,19 (*2)
Từ (*1) và (*2) ta có: x= 5.10-3 và M=65. M là Zn
Đáp án D
Đúng 0
Bình luận (0)
Đốt cháy m gam đồng (II) sunfua trong khí oxi dư, thu được chất rắn X có khối lượng bằng (m – 4,8) gam. Nung X trong khí CO dư tới khối lượng không đổi, thu được chất rắn Y. Hoà tan Y trong dung dịch
HNO
3
loãng dư, thu được V lít một chất khí Z (đktc) không màu, hóa nâu đỏ trong không khí. Các phản ứng xảy ra hoàn toàn. Giá trị của m và V lần lượt là A. 28,80 và 4,48. B. 19,20 và 2,24. C. 19,20 và 4,48. D. 28,80 và 2,24.
Đọc tiếp
Đốt cháy m gam đồng (II) sunfua trong khí oxi dư, thu được chất rắn X có khối lượng bằng (m – 4,8) gam. Nung X trong khí CO dư tới khối lượng không đổi, thu được chất rắn Y. Hoà tan Y trong dung dịch HNO 3 loãng dư, thu được V lít một chất khí Z (đktc) không màu, hóa nâu đỏ trong không khí. Các phản ứng xảy ra hoàn toàn. Giá trị của m và V lần lượt là
A. 28,80 và 4,48.
B. 19,20 và 2,24.
C. 19,20 và 4,48.
D. 28,80 và 2,24.
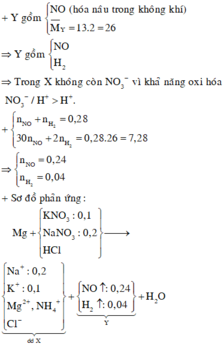
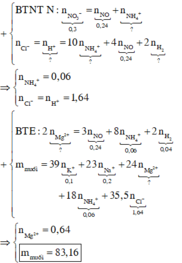
Cho lượng dư Mg tác dụng với dung dịch gồm HCl, 0,1 mol KNO3 và 0,2 mol NaNO3. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X chứa m gam muối và 6,272 lít hỗn hợp khí Y (đktc) gồm hai khí không màu, trong đó có một khí hóa nâu trong không khí. Tỉ khối của Y so với H2 là 13. Giá trị của m là A. 83,16 B. 60,34 C. 84,76 D. 58,74
Đọc tiếp
Cho lượng dư Mg tác dụng với dung dịch gồm HCl, 0,1 mol KNO3 và 0,2 mol NaNO3. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X chứa m gam muối và 6,272 lít hỗn hợp khí Y (đktc) gồm hai khí không màu, trong đó có một khí hóa nâu trong không khí. Tỉ khối của Y so với H2 là 13. Giá trị của m là
A. 83,16
B. 60,34
C. 84,76
D. 58,74