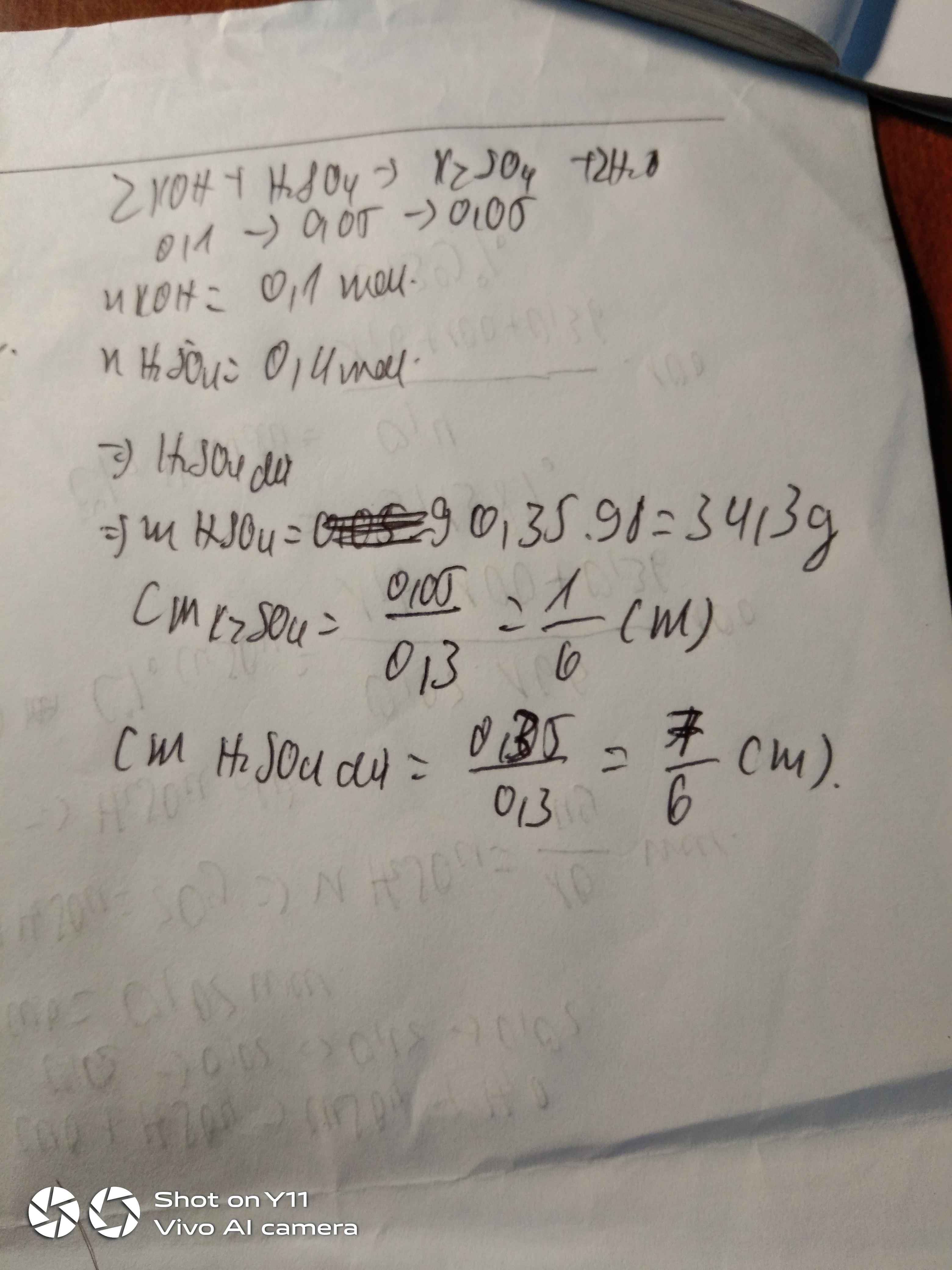Cho 0,01 mol alanin phản ứng với 200ml dd HCl 0,1 M có d=1,02 g/ml. Nồng độ C% các chất sau phản ứng là.

Những câu hỏi liên quan
cho 200 ml dung dịch HCl 1M tác dụng với 200ml dd Barihidroxit 1M. Tính nồng độ mol chất tan trong dd sau phản ứng
nHCl = 1 . 0,2 = 0,2 mol
nBa(OH)2 = 1 . 0,2 = 0,2 mol
Pt: Ba(OH)2 + 2HCl --> BaCl2 + H2O
........0,1.............0,2...........0,1
Xét tỉ lệ mol giữa Ba(OH)2 và HCl:
\(\dfrac{0,2}{1}>\dfrac{0,2}{2}\)
Vậy Ba(OH)2 dư
V dd sau pứ = 0,2 + 0,2 = 0,4 mol
CM Ba(OH)2 dư = \(\dfrac{\left(0,2-0,1\right)}{0,4}=0,25M\)
CM BaCl2 = \(\dfrac{0,1}{0,4}=0,25M\)
Đúng 0
Bình luận (0)
cho 18.25 gam HCl tác dụng với 200ml dung dịch ca(oh)2 0,5 M .Biết D= 1,25 g/ml
a)tính khối lượng các chất sau phản ứng.
b) tính nồng độ %các chất còn lại sau phản ứng .
c) nồng độ mol các chất còn lại sau phản ứng.
Cho 4,8 gam Mg valf 200ml dd HCl 3M ( D= 1,2 g (ml)). Sau phản ứng thu đc dd A và khí H2
a) tính thể tích khí H2 ở đkc
b) Tính nòng độ % và nồng độ mol/l của từng chất trong dd A
\(n_{Mg}=\dfrac{4,8}{24}=0,2mol\)
\(m_{ddHCl}=200\cdot1,2=240g\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
0,2 0,4 0,2 0,2
a)\(V_{H_2}=0,2\cdot22,4=4,48l\)
b)\(m_{MgCl_2}=0,2\cdot95=19g\)
\(m_{H_2}=0,2\cdot2=0,4g\)
\(m_{ddMgCl_2}=4,8+240-0,4=244,4g\)
\(C\%=\dfrac{19}{244,4}\cdot100\%=7,77\%\)
\(C_M=\dfrac{0,2}{0,2}=1M\)
Đúng 5
Bình luận (0)
Cho 1,02 gam hỗn hợp gồm Al và Mg vào 100ml dung dịch HCl. Sau khi kết thúc phản ứng, làm bay hơi hết nước thu được 3,86 gam chất rắn khan. Nếu cho 1,02 gam hỗn hợp trên vào 200ml dd HCL cùng loại. Sau khi kết thúc phản ứng, làm bay hơi hết nước thu được 4,57 gam chất rắn khan. Tính khối lượng kim loại trong hỗn hợp và nồng độ mol/l của dd HCl
Khi lượng HCl gấp đôi thì lượng chất rắn thu đc không gấp đôi thí nghiệm 1 nên suy ra trong 2 trường hợp kim loại tan hết và HCl dư.
2 trường hợp->trường hợp 2
Gọi số mol của Mg và Al trong hh là x và y, ta có:
=> \(\left\{{}\begin{matrix}\text{24x+27y=1,02
}\\\text{95x+133.5y=4,57}\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}x=0,02\\y=0,02\end{matrix}\right.\)
=>\(\left\{{}\begin{matrix}m_{Mg}=0,02.24=0,48g\\m_{Al}=0,02.27=0,54g\end{matrix}\right.\)
Tính nồng độ mol/1 của dung dịch HCl
- Xét TN1: gọi số mol Al đã pứ là a còn dư là 0,02.-a (Mg đã pư hết)
Khối lg chất rắn = 0,02.95+133,5a+27(0,02.-a)=3,86 => a=0,0133
Số mol HCl hòa tan Mg và Al là (0,02.2)+3.0,133=0,08 mol
Nồng độ mol/1 của HCl là 0,08/0,1=0,8 M
Đúng 0
Bình luận (0)
Cho 200ml dd có chứa 0.05 mol HCl tham gia phản ứng hoàn toàn với 300ml dd gồm 0.01 mol NaOH và 0.02 mol KOH. Tính nồng độ mol của chất trong dd sau phản ứng.
Cho 25,2g sắt phản ứng hoàn toàn với 200ml dd HCL 𝐚) Tính thể tích khí thoát ra (đktc) 𝐛) Tính nồng độ mol dd HCL đã dùng 𝐜) Tính nồng độ mol dd thu được sau phản ứng.
\(a)n_{Fe}=\dfrac{25,2}{56}=0,45mol\\ Fe+2HCl\rightarrow FeCl_2+H_2\)
0,45 0,9 0,45 0,45
\(V_{H_2\left(đktc\right)}=0,45.22,4=10,08l\\ b)C_{M\left(HCl\right)}=\dfrac{0,9}{0,2}=4,5M\\ c)C_{M\left(FeCl_2\right)}=\dfrac{0,45}{0,2}=2,25M\)
Đúng 2
Bình luận (0)
cho 100ml dd KOH 1M phản ứng với 200ml dd H2SO4 nồng độ 2M a) hỏi sau phản ứng chất nào dư, dư bao nhiêu b) tính nồng độ mol của dd sau phản ứng
cho 4,6g Na\(_2\)O sau phản ứng thu đc 200ml dd bazơ(NaOH)
a)Tính nồng độ mol của dd bazơ thu đc
c)Tính nồng độ % của dd bazơ trên biết dd này có d=1,12(g/ml)
`n_{Na_2O}={4,6}/{62}\approx 0,074(mol)`
`Na_2O+H_2O->2NaOH`
`0,074->0,074->0,148(mol)`
`a)\ C_{M\ NaOH}={0,148}/{0,2}=0,74M`
`b)\ C\%_{NaOH}={0,148.40}/{200.1,12}.100\%\approx 2,64\%`
Đúng 2
Bình luận (0)
Hòa tan 32,5 gam Zn bằng 250 ml dd HCl, sau phản ứng tạo ra kẽm clorua ZnCl2 và khí H2 a/ tính khối lượng muối ZnCl2 b/ tính thể tích H2 tạo thành sau phản ứng (đktc) c/ tính nồng độ mol dd HCl đã dùng d/ tính nồng độ mol dd sau phản ứng ( thể tích dd không đổi) Lập tóm tắt
Zn + 2HCl --> ZnCl2 + H2
0,5 1 0,5 0,5
nZn=\(\dfrac{32,5}{65}\)=0,5(mol)
mZnCl2=0,5.136=68(g)
VH2=0,5.22,4=11,2(l)
c) CM HCl=\(\dfrac{1}{0,25}=4M\)
Đúng 8
Bình luận (3)