X là dung dịch HCl 0,04M, Y là dung dịch Ca(OH)2 0,04M. Trộn dung dịch X với dung dịch Y thu được dung dịch Z có pH=2. Cho rằng thể tích dung dịch Z bằng tổng thể tích dung dịch X và Y đem trộn. Tỉ lệ thể tích dung dịch X và Y tương ứng là:

Những câu hỏi liên quan
Dung dịch X chứa NaHCO3 0,15M và Ba(HCO3)2 0,45M. Dung dịch Y chứa Ca(OH)2 0,5M. Trộn dung dịch X và dung dịch Y với thể tích bằng nhau, thu được 400 ml dung dịch Z và m gam kết tủa. Giả sử tổng thể tích dung dịch không đổi khi pha trộn. Giá trị của m là A. 19,00 B. 29,70 C. 39,40 D. 27,73
Đọc tiếp
Dung dịch X chứa NaHCO3 0,15M và Ba(HCO3)2 0,45M. Dung dịch Y chứa Ca(OH)2 0,5M. Trộn dung dịch X và dung dịch Y với thể tích bằng nhau, thu được 400 ml dung dịch Z và m gam kết tủa. Giả sử tổng thể tích dung dịch không đổi khi pha trộn. Giá trị của m là
A. 19,00
B. 29,70
C. 39,40
D. 27,73
X là dung dịch HCl 0,3M. Y là dung dịch HCl 0,6M. Nếu trộn dung dịch X và Y theo tỉ lệ thể tích là 2:3 thu được dung dịch Z.Tính nồng độ mol của dung dịch Z
\(Coi : V_X = 2(lít) \to V_Y = 3(lít) \Rightarrow V_Z = 2 + 3 =5(lít)\\ n_{HCl} = 0,3.2 + 0,6.3 = 2,4(mol) \\ \Rightarrow C_{M_{HCl\ trong\ Z}} = \dfrac{2,4}{5} = 0,48M\)
Đúng 1
Bình luận (0)
Cho A là dung dịch H2SO4 ; B1, B2 là ha dung dịch NaOH có nồng độ khác nhau. Trộn B1 với B2 theo tỉ lệ thể tịch 1: 1 thu được dung dịch X. Trung hòa 20 ml dung dịch X cần dùng 20 ml dung dịch A. Trộn B1 với B2 theo tỉ lệ thể tích tương ứng 2: 1 thu được dung dịch Y. Trung hòa 30 ml dung dịch Y cần dùng 32,5 ml dung dịch A. Trộn B1 với B2 theo tỉ lệ thể tích tương ứng a: b thu được dung dịch Z. Trung hòa 70 ml dung dịch Z cần dùng 67,5 ml dung dịch A. Tìm giá trị a : b.
Đọc tiếp
Cho A là dung dịch H2SO4 ; B1, B2 là ha dung dịch NaOH có nồng độ khác nhau. Trộn B1 với B2 theo tỉ lệ thể tịch 1: 1 thu được dung dịch X. Trung hòa 20 ml dung dịch X cần dùng 20 ml dung dịch A. Trộn B1 với B2 theo tỉ lệ thể tích tương ứng 2: 1 thu được dung dịch Y. Trung hòa 30 ml dung dịch Y cần dùng 32,5 ml dung dịch A. Trộn B1 với B2 theo tỉ lệ thể tích tương ứng a: b thu được dung dịch Z. Trung hòa 70 ml dung dịch Z cần dùng 67,5 ml dung dịch A. Tìm giá trị a : b.
A: H2SO4 : CA (M)
B1: NaOH : C1 (M)
B2: NaOH: C2 (M)
TH1: VB1: VB2 = 1: 1 => gọi thể tích của mỗi chất là V
Nồng độ của NaOH sau khi trộn là: CM = n : V
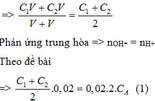
TH2: VB1 : VB2 = 2 : 1 => Đặt VB2 = V (lít) thì VB1 = 2V (lít)
Nồng độ của NaOH sau khi trộn là:

Ta có:
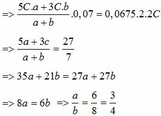
Đúng 0
Bình luận (0)
Tính pH của các dung dịch sau :
a.Trộn 100 ml dung dịch HCl 0,12M với 100 ml dung dịch H2SO4 0,04M. Tính pH của dung dịch X thu được .
b. Trộn 100 ml dung dịch KOH 0,12M với 100 ml dung dịch Ba(OH)2 0,04M. Tính pH của dung dịch thu được .
a) \(n_{H^+}=n_{HCl}+2n_{H_2SO_4}=0,1\cdot0,12+0,1\cdot0,04=0,016\)
\(C_M=\dfrac{0,016}{0,2}=0,08M\)
\(\Rightarrow pH=-log\left(0,08\right)=1,1\)
b) \(n_{OH^-}=n_{KOH}+2n_{Ba\left(OH\right)_2}=0,012+2\cdot0,004=0,02\)
\(C_M=\dfrac{0,02}{0,2}=0,1\)
\(\Rightarrow pH=-log\left(\dfrac{10^{-14}}{0,1}\right)=13\)
Đúng 0
Bình luận (0)
Dung dịch X là dung dịch H2SO4, dung dịch Y là dung dịch NaOH. Nếu trộn X và Y theo tỉ lệ thể tích tương ứng là 3 : 2 thì thu được dung dịch A có tính axit. Để trung hoà 1 lít dung dịch A cần dùng 40 gam NaOH 20%. Nếu trộn X và Y theo tỉ lệ thể tích tương ứng 2 : 3 thì thu được dung dịch B có tính kiềm. Để trung hoà 1 lít dung dịch B cần dùng 29,2 gam HCl 25%. Tính nồng độ các dung dịch X và Y.
Đọc tiếp
Dung dịch X là dung dịch H2SO4, dung dịch Y là dung dịch NaOH. Nếu trộn X và Y theo tỉ lệ thể tích tương ứng là 3 : 2 thì thu được dung dịch A có tính axit. Để trung hoà 1 lít dung dịch A cần dùng 40 gam NaOH 20%. Nếu trộn X và Y theo tỉ lệ thể tích tương ứng 2 : 3 thì thu được dung dịch B có tính kiềm. Để trung hoà 1 lít dung dịch B cần dùng 29,2 gam HCl 25%. Tính nồng độ các dung dịch X và Y.
Đụ má đăng gần 5 tháng dell ai trả lời, web dead mẹ r
Đúng 0
Bình luận (0)
Trộn hai dung dịch H2SO4 0,1M và HCl 0,3M với những thể tích bằng nhau thu được dung dịch X. Lấy 450ml dung dịch X cho tác dụng với V (lít) dung dịch Y (gồm NaOH 0,15M và KOH 0,05M), thu được dung dịch Z có pH 1. Giá trị của V là: A. 0,225 B. 0,155 C. 0,450 D. 0,650
Đọc tiếp
Trộn hai dung dịch H2SO4 0,1M và HCl 0,3M với những thể tích bằng nhau thu được dung dịch X. Lấy 450ml dung dịch X cho tác dụng với V (lít) dung dịch Y (gồm NaOH 0,15M và KOH 0,05M), thu được dung dịch Z có pH = 1. Giá trị của V là:
A. 0,225
B. 0,155
C. 0,450
D. 0,650
Chọn A
450 ml X do trộn 225 ml HCl và 225 ml H2SO4 => nH+ = 0,1125 mol
nOH = 0,2V (mol)
Do Z có pH = 1 (axit) => axit dư => nH+ dư = 10-pH.(0,45 + V) = 0,1125 – 0,2V
=> V = 0,225 lit
Đúng 0
Bình luận (0)
Trộn cùng thể tích dung dịch KOH 0,03M; dung dịch NaOH 0,02M và dung dịch H2SO4 0,04M thu được dung dịch có pH là
Trộn dung dịch X (NaOH 0,1M và Ba(OH)2 0,2M) với dung dịch Y (HCl 0,2M và H2SO4 0,1M) theo tỉ lệ nào về thể tích để được dung dịch có pH = 13
A. 5:3
B. 4:5
C. 5:4
D. 3:2
Trộn dung dịch X (NaOH 0,1M và Ba(OH)2 0,2M) với dung dịch Y (HCl 0,2M và H2SO4 0,1M) theo tỉ lệ nào về thể tích để được dung dịch có pH = 13
A 5:3
B. 4:5
C. 5:4
D. 3:2












