Cho hỗn hợp A gồm 16g Fe2O3 và 6,4g CuO vào 160ml dung dịch H2SO4 2M. Sau phản ứng thấy còn m gam rắn không tan.
a. Tính m.
b. Tính thể tích dung dịch hỗn hợp gồm axit HCl 1M và axit H2SO4 0,5M cần dùng để phản ứng hết hỗn hợp A.
Cho hỗn hợp A gồm 16g \(Fe_2O_3\) và 6,4g CuO vào 160ml dung dịch \(H_2SO_4\) 2M Sau phản ứng thấy còn m gam rắn không tan a) tính m b) tính thể tích dung dịch hỗn hợp gồm axit HCl 1M và axit\(H_2SO_4\) 0.5M cần dùng để phản ứng hết hỗn hợp A
a) \(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right);n_{CuO}=\dfrac{6,4}{80}=0,08\left(mol\right)\)
\(n_{H_2SO_4}=0,16.2=0,32\left(mol\right)\)
TH1 Fe2O3 phản ứng trước CuO dư
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
0,1------------->0,3
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
0,02<-------0,32-0,3=0,02
=> \(m_{cr}=\left(0,08-0,02\right).80=4,8\left(g\right)\)
TH2: CuO phản ứng trước Fe2O3 dư
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)0,08------->0,08
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
0,08<----------0,32-0,08=0,24
=> \(m_{cr}=\left(0,1-0,08\right).160=3,2\left(g\right)\)
b) Gọi V là thể tích cần tìm của hỗn hợp
=> \(n_{H^+}=V.1+V.2.0,5=2V\) (1)
\(Fe_2O_3+3H^+\rightarrow Fe^{3+}+3H_2O\)
\(CuO+2H^+\rightarrow Cu^{2+}+H_2O\)
Theo PT => \(n_{H^+}=3n_{Fe_2O_3}+2n_{CuO}=0,46\left(mol\right)\) (2)
Từ (1),(2) => V=0,23(l)
Cho hỗn hợp A gồm 16g Fe2O3 và 6,4g CuO vào 160ml dung dịch H2SO4 2M Sau phản ứng thấy còn m gam chất rắn không tan Tính m Tính thể tích dung dịch hỗn hợp gồm axit HCl 1M và axit H2SO4 0,5M cần dùng để phản ứng hết hỗn hợp A
Cho hỗn hợp A gồm 16g Fe2O3 và 6,4g CuO vào 160ml dung dịch H2SO4 2M. Sau phản ứng thấy còn m gam rắn không tan.
a. Tính m.
b. Tính thể tích dung dịch hỗn hợp gồm axit HCl 1M và axit H2SO4 0,5M cần dùng để phản ứng hết hỗn hợp A.
cho hỗn hợp A gồm 16g Fe2O3 và 6,4g CuO vào 160ml dd H2SO4 2M. tính thể tích dd hỗn hợp gồm HCl 1M và axit H2SO4 0,5M cần dùng để phanr ứng hết hỗn hợp A
em sửa lại đề : cho hỗn hợp A gồm 16g Fe2O3 và 6,4g CuO vào 160ml dd H2SO4 2M. sau phản ứng có m chất rắn không tan
a/tính m
b/tính thể tích dd hỗn hợp gồm HCl 1M và axit H2SO4 0,5M cần dùng để phản ứng hết hỗn hợp A
để hoà tan 3,2 g hỗn hợp A gồm CuO và Fe2O3 cần vừa đủ 50 ml dung dịch B chứa HCl 1M và H2SO4 0,5M
a) Tính khối lượng từng chất trong A
b) Cô cạn dung dịch sau phản ứng thu được m gam chất rắn. Tính m
Để hoà tan hoàn toàn 20 gam hỗn hợp Fe2O3 và CuO (tỷ lệ mol tương ứng 1:4) cần vừa đủ V ml dung dịch chứa đồng thời HCl 1M và H2SO4 0,5M, sau phản ứng thu được dung dịch X chứa m gam muối. Tính giá trị của V và m?
Cho hỗn hợp A gồm 16g Fe2O3 và 6.4g CuO vào 160ml dung dịch H2SO4 2M sau phản ứng thấy còn m gam rắn không tan
a) tính m
b) tính thể tích dung dịch hỗn hợp gồm axit HCl 1M và axit H2SO4 0.5M cần dùng để phản ứng hết hỗn hợp A
n(CuO)= 6,4/80=0,08 mol
n(Fe2O3)= 16/160 = 0,1 mol
n(H2SO4) = 0,16x 2=0,32 mol
hoa tan hon hop hai oxit nay bang H2SO4 co cac PU xay ra:
CuO + H2SO4 = CuSO4 + H20
Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O
ta xet hai truong hop sau:
gia su CuO tan het truoc.
so mol acid PU voi CuO = n(CuO) = 0,08 mol
=> so mol acid PU voi Fe2O3 = 0,32 - 0,08 = 0,24 mol
=> so mol Fe2O3 tan = 0,24/3 = 0,08 mol
=> m(Fe2O3)du= (0,1 - 0,08)x160 = 3,2 g
gia su Fe2O3 tan het truoc.
n(acid PU voi Fe2O3)= 0,1x3=0,3 mol
=>n(acid PU voi CuO)= 0,32 - 0,3 = 0,02 mol
=>n(CuO PU) = 0,02 mol
=>m(CuO)du = (0,08 - 0,02)x80=4,8 g
vay m bien thien trong khoang 3,2 < m < 4,8 g.
làm tiếp!
Cho 3,87 gam hỗn hợp A gồm Al và Mg vào 250 ml dung dịch X chứa HCl 1M và H2SO4 0,5M. Sau phản ứng thu được dung dịch B và 4,368 lít khí H2 đktc. Các phản ứng xảy ra hoàn toàn
a, Chứng minh rằng dung dịch B vẫn còn dư axit
b, Tính % khối lượng mỗi kim loại trong hỗn hợp A
a.Ta có n HCl = 1 . 0,25 = 0,25 mol
nH2SO4 = 0,5.0.25 = 0,125 mol
==> nH(X) = 0,25 + 0,125.2 = 0,5 mol
nH2 = 4,368/22,4 = 0,195 mol <=> nH= 0,195. 2 = 0,39 mol < 0,5 mol
Vậy sau phản ứng dung dịch B vẫn còn axit dư
b. Gọi số mol của Al và Mg lần lượt là x và y mol
Ta có phương trình 27x + 24y =3,87 (1)
Áp dụng định luật bảo toàn eletron ==> 3x + 2y = 0,195.2 (2)
Từ (1) , (2) ==> \(\left\{{}\begin{matrix}x=0,09\\y=0,06\end{matrix}\right.\)
mAl = 0,09 .27 = 2,43 gam , %mAl trong A = \(\dfrac{2,43}{3,87}\).100=62,8%
==> %mMg trong A = 100 - 62,8 = 37,2%
Cho a gam hỗn hợp A gồm Fe2O3, Fe3O4 và Cu vào dung dịch HCl dư thấy có 1 mol axit phản ứng và còn lại 0,256a gam chất rắn không tan. Mặt khác khử hoàn toàn a gam hỗn hợp A bằng H2 thu được 42g chất rắn. Tính phần trăm khối lượng Cu trong hỗn hợp A.
A.44,8%
B.50%
C.32%
D.25,6%
Đáp án A:
Còn lại 1 phần chất rắn không tan => Cu dư

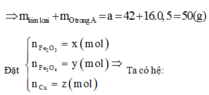
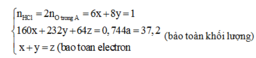
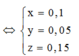
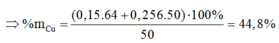
Cho a gam hỗn hợp X gồm Fe2O3, Fe3O4, Cu vào dung dịch HCl dư thấy có 1 mol axit phản ứng và còn lại 0,256a gam chất rắn không tan. Mặt khác, khử hoàn toàn a gam hỗn hợp X bằng H2 dư, thu được 42 gam chất rắn. Tính % khối lượng Cu trong hỗn hợp X
A. 25,6%.
B. 50%.
C. 44,8%.
D. 32%.